Un extraño mecanismo cancerĂgeno de sĂntesis proteica
El cáncer sigue siendo un problema predominante a nivel mundial, sin embargo, los procesos por los cuales la identidad celular es alterada durante el desarrollo tumoral aĂşn no son completamente entendidos. Actualmente, se han centrado muchos esfuerzos en comprender cĂłmo la alteraciĂłn de la transcripciĂłn de los genes da forma al crecimiento del cáncer. En un reciente estudio,  se explorĂł otro nivel de regulaciĂłn gĂ©nica, y se identificĂł un interruptor en la maquinaria de traducciĂłn que tiene implicancia en la formaciĂłn de tumores. Los hallazgos del estudio revelan cĂłmo exclusivamente las cĂ©lulas cancerĂgenas utiliza los extremos presentes en la regiĂłn 5' de los ARNm (5' UTR) para llevar a cabo la traducciĂłn y sĂntesis de sus proteĂnas. Lo anterior, brinda nuevo conocimiento sobre la maquinaria proteica tumoral y pone de manifiesto nuevos objetivos para nuevas intervenciones terapĂ©uticas.
Cambio traduccional
El carcinoma de cĂ©lulas escamosas es una forma de cáncer de piel que con frecuencia involucra la activaciĂłn de la señalizaciĂłn RAS-MAPK y la posterior expresiĂłn del gen SOX2. Para estudiar esta enfermedad, Ataman Sendoel y colaboradores (Nature. 2017 Jan 26;541(7638):494-499 ) usaron un modelo de ratĂłn que es propenso al desarrollo del tumor debido a la sobreexpresiĂłn de Sox2 en la capa externa de la piel (epidermis). Los autores se enfocaron en las cĂ©lulas de la piel en estadĂos pre-neoplásicos, antes de la formaciĂłn de tumores.
Para determinar el panorama instantáneo de la traducciĂłn en la epidermis mutante, determinaron el perfil completo de secuencias de ARN mensajeros unidas por la sĂntesis de proteĂnas de la maquinaria celular (los ribosomas). Complementaron este perfil con un análisis de los niveles globales de ARNm, lo que permitiĂł determinar el estado transcripcional de las cĂ©lulas.
Los investigadores encontraron que las diferencias en la transcripciĂłn y traducciĂłn entre la piel pre-neoplásica y la normal no siempre se correlacionaban. En general, la traducciĂłn parecĂa estar reducida en cĂ©lulas pre-neoplásicas. Sin embargo, los datos de perfiles sugirieron que algunos ARNm se tradujeron más eficientemente (habĂa más ribosomas unidos por transcrito) en cĂ©lulas preneoplásicas que en las normales. Cabe destacar que muchos de estos ARNm codificaron proteĂnas asociadas con la progresiĂłn tumoral.
Otros análisis revelaron un aumento pre-neoplásico en de la ocupaciĂłn ribosĂłmica de las regiones 5 ' no traducibles (UTR), zonas reguladoras en el ARNm que preceden a la codificaciĂłn de secuencia de la proteĂna normal. Alrededor del 50% de las 5' UTR contienen secuencias que por sĂ solas pueden codificar proteĂnas, tal como lo realizan los marcos de lectura abiertos presentes rĂo arriba (uORF, del inglĂ©s upstream open reading frames). La traducciĂłn de uORFs puede resultar en la sĂntesis de pĂ©ptidos, que pueden tener estabilidad variable. Alternativamente, el inicio de la traducciĂłn dentro de las 5' UTRs puede conducir a la generaciĂłn de proteĂnas extendidas (Figura 1).
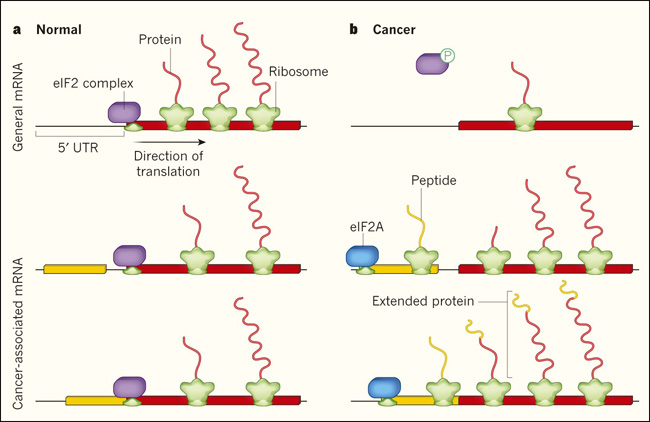
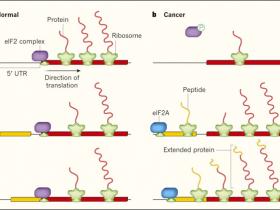
Figura 1: Un cambio traduccional durante la progresiĂłn tumoral.Â
a, los ARN mensajeros contienen regiones no traducidas en el extremo 5'(5' UTR por sus siglas en inglĂ©s) rĂo arriba de su secuencia principal codificadora de proteĂnas (rojo). Muchas de estas UTRs 5' (incluyendo aquellas encontradas en ciertos ARNm asociados al cáncer) tambiĂ©n contienen secuencias con potencial de codificaciĂłn (amarillo). En condiciones normales, el complejo de proteĂnas eIF2 y factores asociados, en combinaciĂłn con una subunidad de la maquinaria de traducciĂłn de la cĂ©lula (el ribosoma), controlan el inicio de la traducciĂłn desde el comienzo de la secuencia codificante principal. Los ribosomas entonces dirigen la sĂntesis de proteĂnas. b, Durante el desarrollo del cáncer, eIF2 puede ser inactivado por fosforilaciĂłn (P), lo que conduce a una disminuciĂłn general de la traducciĂłn. Sendoel y colegas demostraron que, en un modelo de ratĂłn de carcinoma de cĂ©lulas escamosas, el factor de iniciaciĂłn alternativo eIF2A promueve la traducciĂłn de un subconjunto de ARNm asociados al cáncer a partir de sitios de iniciaciĂłn presentes en las regiones 5' UTRs. Esto puede conducir a la sĂntesis de proteĂnas pequeñas (pĂ©ptidos) o proteĂnas extendidas además del producto proteico principal. Este cambio de la traducciĂłn es un evento temprano y esencial durante la formaciĂłn del tumor en este modelo de ratĂłn de cáncer de piel.
Actualmente, no está claro cuántos  5' UTR codifican productos fisiolĂłgicamente relevantes. Sin embargo, el compromiso ribosomal con uORFs afecta la traducciĂłn de secuencias en rĂo abajo. Bajo condiciones de estrĂ©s, los uORF promueven traducciĂłn de algunos ARNm. En condiciones normales generalmente se asocian con la sĂntesis alterada de proteĂnas.Â
El patrĂłn de ocupaciĂłn de ribosomas observado por Sendoel y colegas sugiere que muchos de los uORF se traducen en la epidermis pre-neoplásica, a menudo desde sitios de iniciaciĂłn que tienen un cĂłdigo genĂ©tico no convencional. Cabe destacar que muchos ARNm relacionados con el cáncer muestran una distribuciĂłn alterada de los ribosomas, con una mayor proporciĂłn de uniĂłn a la regiĂłn 5' UTR en el caso de cĂ©lulas pre-neoplásicas. El mayor uso traduccional de estos sitios de iniciaciĂłn es frecuentemente observado en ARNm que tienen alta eficacia de traducciĂłn, lo que implica que los dos fenĂłmenos están mecanĂsticamente vinculados.
En busca del mecanismo que subyace a estos cambios en la traducciĂłn, los investigadores inhibieron la expresiĂłn de genes que codifican reguladores traduccionales en la piel de embriones de ratĂłn y se identificaron aquellos requeridos para el crecimiento celular. Encontraron que la depleciĂłn del complejo de proteĂnas eIF2 - un factor central para el inicio de la traducciĂłn en cĂ©lulas normales - tuvo menos efecto sobre la proliferaciĂłn en epidermis pre-neoplásica que en el tejido normal. El crecimiento en tejido pre-neoplásico parece basarse en el factor de iniciaciĂłn alternativo eIF2A (figura 1). Esta proteĂna ha sido vinculada a la traducciĂłn de uORF y por el uso de sitios de inicio no convencionales.
Para confirmar la relevancia de eIF2A en el desarrollo de tumores, los autores realizaron suprimieron el gen Eif2a en las cĂ©lulas de la piel que albergaban mutaciones causantes de cáncer en los genes codificantes para las proteĂnas H-Ras y Tgfbr2, y se injertaron estas cĂ©lulas en ratones. Esto revelĂł que eIF2A es necesaria para el crecimiento tumoral in vivo.
A continuación, los investigadores demostraron que la pérdida de Eif2a reduce el enlace ribosómico a la región 5' UTR en células de cáncer de piel. Finalmente, proporcionaron pruebas de que el uso de sitios de inicio  5' UTR por eIF2A está vinculado a la traducción eficiente de un subconjunto de ARNm asociados al cáncer bajo condiciones de estrés in vitro como tumorales in vivo.
Actualmente, se conoce que varias vĂas de estrĂ©s conducen a la fosforilaciĂłn e inactivaciĂłn del complejo eIF2, lo que se vincula al desarrollo del cáncer. DespuĂ©s de incorporar los hallazgos de Sendoel y colegas emerge un nuevo modelo en el que, la inhibiciĂłn de eIF2 da paso a la actividad eIF2A para la traducciĂłn a travĂ©s del uso de las regiones 5' UTR presentes en los transcritos. Esto, se relaciona con la el potenciamiento de los procesos tumorales. Sorprendentemente, la mutaciĂłn del uORF del gen Ctnnb1, que es necesaria para el desarrollo del cáncer de piel, tambiĂ©n alterĂł el desarrollo del tumor. Por lo tanto, se  proporciona pruebas sĂłlidas de que un cambio en la traducciĂłn dependiente de eIF2A y el uso de los sitios de iniciaciĂłn rĂo arriba puede ser temprano y constituir eventos importantes en la formaciĂłn de tumores.
Por lo tanto, el estudio actual extiende el cuerpo de evidencia que apoya el cambio en el mecanismo traduccional como un actor central en el desarrollo del cáncer. El mecanismo de traducciĂłn atĂpica tiene el potencial de dar forma el proteoma del cáncer y, por ende afecta el desarrollo del tumor de mĂşltiples maneras que son relevantes para el conocimiento del establecimiento del cáncer.
Fuente bibliográfica
Cell biology: Unconventional translation in cancer
Marianne Terndrup Pedersen and Kim B. Jensen
Biotech Research and Innovation Centre, University of Copenhagen, DK-2200 Copenhagen, Denmark.
doi:10.1038/nature21115