Reprogramaciû°n celular de la retina
La degeneraciû°n de las neuronas de la retina es el punto final de la mayorûÙa de lasô causas mûÀs comunes de ceguera irreversible, que afecta a mûÀs de 50 millones de personas en todo el mundo. En vertebrados no mamûÙferos como los peces, la lesiû°n de la retina es seguida por una desdiferenciaciû°n y posterior proceso de reprogramaciû°nen en el que la glia endû°gena de Mû¥ller prolifera y se diferencia en todos los tipos celulares de la retina, incluyendo fotorreceptores, interneuronas y cûˋlulas ganglionares. De esta forma se restaura la funciû°n visual. Sin embargo, este potencial de regeneraciû°n y reprogramaciû°n es casi inexistente en mamûÙferos. Pese a lo anterior, un estudio reciente muestra que este evento puede ser llevado a cabo en ratones.ô
Conversiû°n celular
En peces, el proceso de desdiferenciaciû°n y reprogramaciû°n de la glûÙa de Mû¥ller en neuronas de la retina implica la reactivaciû°n de un perfil de expresiû°n gûˋnica neurogûˋnica similar al de progenitores multipotentes de cûˋlulas de la retina, que dan lugar a todas las neuronas de la retina durante el desarrollo embrionario. Hace un tiempo no estaba claro quûˋ restringe la desdiferenciaciû°n de la glûÙa de Mû¥ller en mamûÙferos, aunque ha sido establecido que la activaciû°n de ciertas vûÙas moleculares pueden reprogramar fibroblastos o a la misma glia en neuronas funcionales y restaurar la pluripotencia de cûˋlulas diferenciadas terminalmente en ratones y humanos (por ejemplo, en la generaciû°n de cûˋlulas madre pluripotentes inducidas). Nikolas Jorstad y colaboradores investigaron si molûˋculas especûÙficas podrûÙan estimular la reprogramaciû°n de la glûÙa de Mû¥ller en neuronas de la retina, ambas de las cuales derivadas de linajes celulares relacionados. (doi: 10.1038/nature23283)
Estudios previos han mostrado que la expresiû°n del factor de transcripciû°n proneural Ascl1 se incrementa en la glûÙa de Mû¥ller tras el daûÝo a la retina en pez cebra y ratones jû°venes y que esa glûÙa es la fuente de las neuronas regeneradas. Sin embargo, incluso con la sobreexpresiû°n continua de Ascl1, esta capacidad neurogûˋnica se pierde a los 16 dûÙas post nacimiento en ratones, lo que sugiere que otros factores son necesarios para este proceso. Para superar esta barrera de regeneraciû°n, los autores modificaron la expresiû°n de Ascl1 en la glûÙa de Mû¥ller en las retinas daûÝadas de ratones adultos, y luego inyectaron, en el cuerpo vûÙtreo, un inhibidor de la histona deacetilasa (molûˋcula que abre la estructura terciaria de la cromatina).
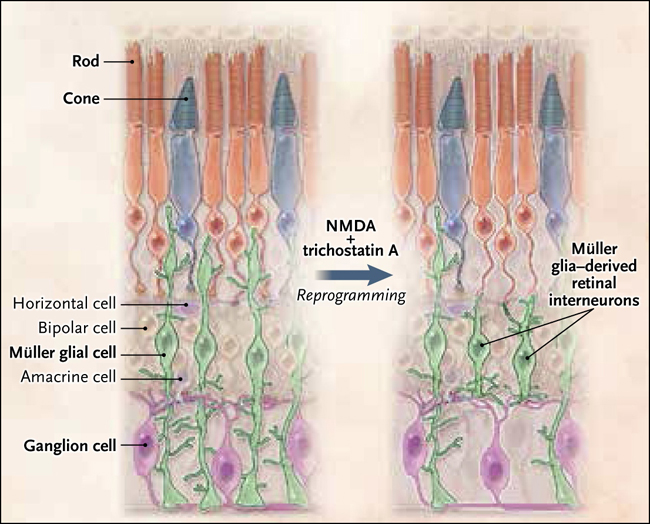
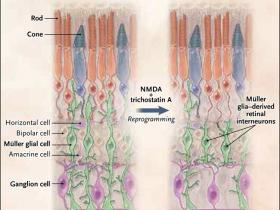
Figura 1. Conversiû°n celular en la retina.
La pûˋrdida de tipos especûÙficos de cûˋlulas en la retina conduce a la enfermedad oftûÀlmica. Los enfoques experimentales para la terapia implican el trasplante de cûˋlulas o parches de cûˋlulas de fuentes alogûˋnicas (en modelos animales y humanos) y el estûÙmulo de la regeneraciû°n endû°gena in situ (en modelos animales). Un estudio reciente realizado por Jorstad y colaboradores (doi: 10.1038/nature23283) mostrû° que con el uso de ratones que la cûˋlula glial Mû¥ller puede someterse a reprogramaciû°n por medio de la expresiû°n forzada de un factor de transcripciû°n, Ascl1, junto con la exposiciû°n a un factor modificador de la cromatina (tricostatina A). NMDA denota ûcido N-metil-d-aspûÀrtico.
El inhibidor de la histona deacetilasa promueve el acceso de factores de transcripciû°n a genes especûÙficos clave (como Ascl1) en la glûÙa de Mû¥ller y permite una reprogramaciû°n y diferenciaciû°n mûÀs eficiente de la glûÙa de Mû¥ller en interneuronas de retina. Los autores observaron que la reprogramaciû°n y diferenciaciû°n de la glûÙa de Mû¥ller en interneuronas de la retina, que incluyen cûˋlulas bipolares y cûˋlulas amacrinas (figura 1). AdemûÀs, encontraron que estas interneuronas reprogramadas se integraban en los circuitos de la retina haciendo sinapsis con neuronas existentes en esta estructura ocular. AdemûÀs, generaron potenciales elûˋctricos tras la estimulaciû°n luminosa.
Sin embargo, es la pûˋrdida de cûˋlulas fotorreceptoras lo que causa la mayorûÙa de las formas de degeneraciû°n de la retina (retinitis pigmentosa, degeneraciû°n miû°pica y degeneraciû°n macular) y la pûˋrdida de cûˋlulas ganglionares de la retina lo que causa glaucoma. En un contexto amplio, in vivo, la reprogramaciû°n celular in situ tiene ventajas sobre el trasplante tradicional basado en terapia con cûˋlulas madre, incluyendo un riesgo reducido de infecciû°n, rechazo y formaciû°n de tumores.
Una aplicaciû°n alternativa de reprogramaciû°n celular la conversiû°n es la conversiû°n in vivo de un tipo celular diferenciado terminal (por ejemplo, de las cûˋlulasô fotorreceptoras bastones) en otro (por ejemplo, conos) para preservar la funciû°n y crear resistencia a las mutaciones heredadas. Los esfuerzos se centran actualmente en la mejor manera de obtener una reprogramaciû°n celular segura y eficiente que entregue funcionalidad apropiada. Debido a que la anatomûÙa de la retina es û¤nica en humanos, los modelos de primate pueden ser considerados para estudios preclûÙnicos de seguridad y eficacia
Fuente bibliográfica
Cellular Reprogramming in the Retina ã Seeing the Light
Eye Institute and Department of Ophthalmology, Eye and ENT Hospital, Fudan University, Shanghai, China.
Yi Lu, M.D., Ph.D., & Kang Zhang, M.D., Ph.D.
DOI: 10.1056/NEJMcibr1713887