Cuestionamiento a la neurogÃĐnesis humana
Durante la vida de mamÃferos adultos, siguen generÃĄndose nuevas neuronas en la zona subgranular del giro dentado del hipocampo. Este proceso se ha relacionado con el aprendizaje y memoria, y se piensa que estÃĄ alterado en patologÃas neurolÃģgicas. En adultos, algunos estudios sugieren que cientos de neuronas nuevas se agregan al giro dentado cada dÃa, mientras que otros han encontrado menos neuronas nuevas putativas. A pesar de estas discrepancias, generalmente se considera que el hipocampo humano continÚa generando nuevas neuronas. Recientemente, se ha definido que una poblaciÃģn especÃfica de cÃĐlulas progenitoras no confluye en la zona subgranular durante el desarrollo fetal o postnatal humano. TambiÃĐn se ha observado que el nÚmero de progenitores proliferantes y de neuronas jÃģvenes en el giro dentado disminuye bruscamente durante el primer aÃąo de vida y sÃģlo se observan unas pocas neuronas jÃģvenes aisladas entre los 7 y 13 aÃąos de edad. La disminuciÃģn temprana de la neurogÃĐnesis del hipocampo plantea interrogantes acerca de cÃģmo difiere la funciÃģn del giro dentado entre los humanos y otras especies en las que se preserva el rol productor neuronal del hipocampo adulto.
Edad y declive neuronal
Si se analiza cualquier artÃculo sobre el desarrollo neuronal en la edad adulta, es muy probable que se advierta que el nacimiento de nuevas neuronas ocurre en la regiÃģn hipocÃĄmpica del cerebro de todas las especies de mamÃferos. Esta idea subyace a la opiniÃģn, muy extendida entre los neurocientÃficos, de que el anÃĄlisis de dicha neurogÃĐnesis en animales puede beneficiar nuestra comprensiÃģn del aprendizaje, los trastornos emocionales y las enfermedades neurodegenerativas en humanos. Pero recientemente se ha reportado que diferencia de otros mamÃferos, las Últimas neuronas nuevas en el hipocampo humano se generan en la niÃąez, hallazgos ciertamente controversiales (DOI: 10.1038/nature25975).
Actualmente, es sabido que el cerebro puede cambiar de acuerdo a las necesidades y demandas. Pero no siempre fue asÃ. En la dÃĐcada de 1960, el biÃģlogo Joseph Altman informÃģ que se generan nuevas neuronas en el cerebro adulto, especÃficamente en subregiones del hipocampo llamadas giros cerebrales dentados, que ahora se sabe que es crucial para la memoria. Sin embargo, la investigaciÃģn adicional se debilitÃģ debido al escepticismo sobre la capacidad del cerebro para tal plasticidad tan radical. No fue hasta la dÃĐcada de 1990, con el desarrollo de tÃĐcnicas mÃĄs avanzadas para visualizar cÃĐlulas cerebrales, que se generalizÃģ la aceptaciÃģn de la neurogÃĐnesis en adultos.
Aunque el alcance y funciÃģn de la neurogÃĐnesis siguen siendo discutibles, ha habido un consenso general de que el hipocampo es una regiÃģn en la que la neurogÃĐnesis adulta existe tanto en humanos como en animales. Esto se basa en varios estudios. Por ejemplo, un estudio en pacientes a los que se les administrÃģ un nucleÃģsido sintÃĐtico llamado bromodeoxiuridina (BrdU) mostrÃģ que habÃa sido incorporada en el ADN de cÃĐlulas en divisiÃģn del giro dentado. Otro encontrÃģ que los marcadores proteicos de neurogÃĐnesis en animales estaban presentes en el tejido cerebral humano post-mortem, y un tercero utilizÃģ la dataciÃģn por radiocarbono para identificar la rotaciÃģn hipocampal-neurona. Sin embargo, los desafÃos metodolÃģgicos dificultan la interpretaciÃģn de los estudios en seres humanos y se requieren mÃĄs investigaciones para llegar a conclusiones definitivas.
Shawn Sorrells y colaboradores (DOI: 10.1038/nature25975) se propusieron abordar esta necesidad utilizando tÃĐcnicas inmunohistoquÃmicas clÃĄsicas en las que anticuerpos especÃficos se unen a proteÃnas de interÃĐs, revelando su ubicaciÃģn tisular. Los autores utilizaron esta estrategia para contar cÃĐlulas precursoras neuronales, cÃĐlulas proliferantes y neuronas inmaduras en muestras de 59 personas, desde el desarrollo fetal hasta la vejez (figura 1). Encontraron corrientes de los tres tipos de cÃĐlulas migrando de una "zona germinal" embrionaria al giro dentado en desarrollo a las 14 semanas de gestaciÃģn.
A las 22 semanas, la migraciÃģn se redujo, y las neuronas inmaduras se restringieron en gran medida al giro dentado. HabÃa muchas menos neuronas inmaduras en un aÃąo de vida que en etapas anteriores. La muestra mÃĄs antigua que contenÃa neuronas inmaduras fue tomada de un individuo de 13 aÃąos. Estos hallazgos contrastan fuertemente la opiniÃģn predominante de que la neurogÃĐnesis del hipocampo humano se extiende a lo largo de la vida adulta.
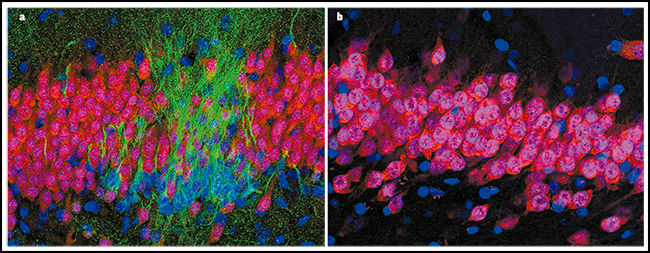
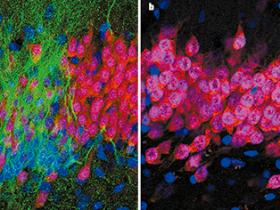
Figura 1. DisminuciÃģn de la neurogÃĐnesis con la edad.
Shawn Sorrells y colaboradores (DOI: 10.1038/nature25975) examinaron secciones del hipocampo humano en varias etapas de la vida, para investigar cuÃĄndo se generan nuevas neuronas. El color verde indica la ubicaciÃģn de la proteÃna DCX, que se produce en cÃĐlulas nuevas; el rojo indica la proteÃna NeuN, que se produce en neuronas maduras; el azul indica un marcador fluorescente llamado DAPI, que marca todos los nÚcleos celulares. a, Al nacer, muchas neuronas nuevas pueden ser vistas. b, Por el contrario, los autores no observaron nuevas neuronas en el hipocampo adulto.
ÂŋEs posible conciliar los hallazgos con datos humanos previos? Aunque las comparaciones directas son difÃciles, Sorrells y sus colegas ofrecen algunas explicaciones. Por ejemplo, encontraron que DCX y PSA-NCAM, dos marcadores proteicos que identifican de manera confiable neuronas inmaduras en animales, pueden tambiÃĐn hacerlo con neuronas maduras y cÃĐlulas gliales no neuronales en humanos. De hecho, los autores muestran que estos dos marcadores identifican inequÃvocamente las neuronas inmaduras sÃģlo si ambas se expresan en una cÃĐlula. Del mismo modo, el grupo demostrÃģ que es posible obtener marcaje inmunohistoquÃmicos similares a BrdU en el tejido que no contienen este nucleÃģsido. El etiquetado inespecÃfico podrÃa, por lo tanto, haber dado lugar a falsos positivos en estudios previos.
El enfoque cuidadoso de los investigadores tambiÃĐn habla de los desafÃos de realizar trabajos sobre neurogÃĐnesis en humanos. Los estudios en animales muestran que la PSA-NCAM es modificada por experiencias previas y que DCX se degrada si el tejido no se preserva rÃĄpidamente. Por lo tanto, una pÃĐrdida aparente de neurogÃĐnesis podrÃa reflejar cambios en la expresiÃģn de marcadores, especialmente si se usan criterios estrictos para definir nuevas neuronas. Dado que hay debates acerca de cuÃĄl es el precursor celular del hipocampo incluso en roedores tambiÃĐn es posible que simplemente no se sepa dÃģnde buscar en humanos.
Los autores minimizaron estos problemas de varias maneras. Primero, observaron neurogÃĐnesis en el hipocampo de bebÃĐs y niÃąos, que sirviÃģ como un control positivo. Segundo, usaron una variedad de muestras de adultos para minimizar la posibilidad de que los problemas con la salud de los tejidos o la preservaciÃģn pudieran confundir sus resultados. En tercer lugar, utilizaron diversos marcadores de neurogÃĐnesis para obtener mÚltiples lÃneas de evidencia. No obstante, se necesitan mÃĄs investigaciones para determinar si estas conclusiones resistirÃĄn la prueba del tiempo.
ÂŋCÃģmo encajan los hallazgos de los autores con la evidencia proveniente de animales? Con un poco recalibraciÃģn conceptual podrÃan encajar bastante bien. Los roedores nacen con sistemas nerviosos relativamente inmaduros, asà que la neurogÃĐnesis de los roedores adultos podrÃa ser un modelo adecuado para este proceso en niÃąos o adolescentes. Dado que la depresiÃģn, esquizofrenia y la enfermedad de Alzheimer estÃĄn enraizadas en defectos tempranos del hipocampo, incluso neuronas generadas en la infancia podrÃan tener un papel clave en la etiologÃa en humanos. AdemÃĄs, datos provenientes de primates (DOI: 10.1073/pnas.1017099108) sugieren que las nuevas neuronas en los humanos podrÃa pasar por una larga fase de maduraciÃģn (aÃąos o incluso dÃĐcadas) en relaciÃģn con lo que ocurre en los roedores, en los que este tiempo mejoran su plasticidad y obtienen importantes propiedades funcionales. Mientras que la continua adiciÃģn de nuevas neuronas puede proporcionar plasticidad en roedores adultos, el desarrollo prolongado de neuronas podrÃa proporcionar una plasticidad similar en humanos adultos.
En el otro extremo del proceso de desarrollo incluso en roedores, la neurogÃĐnesis es muy baja a mediana edad. AsÃ, los datos de Sorrells y colegas no son del todo inconsistentes con la literatura de animales. Si el foco de atenciÃģn de los estudios sobre roedores se desplazara a identificar los mecanismos por los cuales la neurogÃĐnesis disminuye con el tiempo, y a cÃģmo la neurogÃĐnesis puede ser mejorada para compensar patologÃas debidas a la edad, se podrÃan de traducir estos hallazgos en descubrimientos que mejoren la salud humana.
Fuente bibliográfica
Questioning human neurogenesis
Jason S. Snyder
Department of Psychology, Djavad Mowafaghian Centre for Brain Health, University of British Columbia, Vancouver, British Columbia V6T 1Z3, Canada.
doi: 10.1038/d41586-018-02629-3