
23
Contenido disponible en
www.neumologia-pediatrica.clBiopsia pulmonar
Los avances en procedimientos por imágenes y estudios
genéticos han reducido su indicación. Se debe obtener 3
muestras de las zonas más afectadas según la tomografía de
alta resolución. Actualmente se realiza mediante videoto-
racoscopía (VATS), pues tiene un rendimiento similar a la
realizada a cielo abierto (50%), pero con menos complica-
ciones
(9)
.
EPI ESPECÍFICAS DEL LACTANTE
Alteraciones difusas del desarrollo
Ocurre en etapas tempranas del desarrollo pulmonar. Se
asocia a microdeleción en el gen FOX en locus 16q24.1 y
mutación de FOXF1. El diagnóstico lo determina la biopsia
pulmonar
(10)
. Todas presentan historia familiar. Pertenecen a
este grupo la displasia acinar, displasia alveolar congénita y la
displasia alveolocapilar con malrotación de las venas pulmona-
res. En la displasia acinar la detención del desarrollo pulmonar
ocurre en la etapa seudoglandular o canalicular temprana. En
la displasia alveolar congénita, la detención ocurre en la fase
canalicular tardía o en la sacular temprana. Se presentan en
RN de término, con falla respiratoria progresiva, HTP severa,
falleciendo dentro de los primeros 2 meses de vida. El único
tratamiento es el trasplante pulmonar
(10,11)
.
Anormalidades del crecimiento
Presentan defectos de la alveolarización, resultando en
simplificación alveolar. Se asocian a condiciones prenatales
como restricción toráxica, oligoamnios, anomalías esqueléti-
cas, alteraciones neuromusculares, cardiopatías con hipoflujo
y cromosomopatías.
También se relacionan con injurias a partir del naci-
miento, como ocurre en la enfermedad pulmonar crónica
del prematuro (“nueva displasia broncopulmonar”). Las
anomalías del crecimiento además incluyen a la hipoplasia
pulmonar, trisomía 21 (con agrandamiento alveolar, mayor
a nivel subpleural) y malformaciones cardíacas congénitas sin
cromosomopatías
(11)
.
Manifiestan HTP y mortalidad significativa, relacionadas
con la severidad de la alteración del desarrollo alveolar (a
mayor tamaño alveolar peor pronóstico). En algunos casos la
biopsia pulmonar muestra áreas focales de glicogenosis inters-
ticial pulmonar, lo cual favorecería la respuesta a corticoides .
Hiperplasia de células neuroendocrinas
de la infancia
Recientemente fue descrita en cuatro familias, sugiriendo
un factor genético o ambiental como posible causa. Puede
iniciarse desde el período neonatal hasta los primeros años de
vida
(12)
. Los pacientes presentan taquipnea, retracciones, cre-
pitaciones, hipoxemia, por más de 3 meses, la sintomatología
aumenta con infecciones virales, sin embargo, no presentan
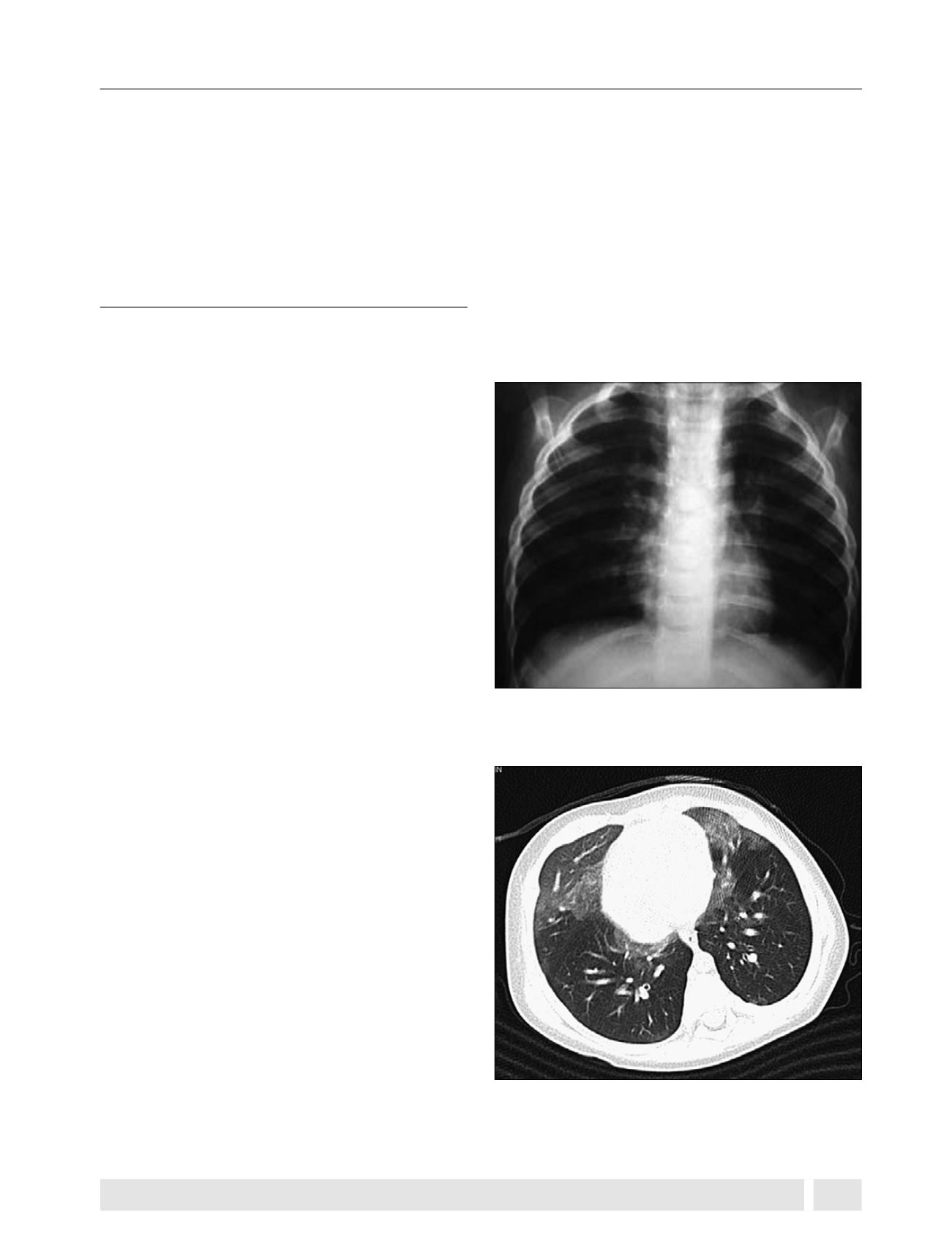
insuficiencia respiratoria. La radiografía de tórax muestra
hiperinsuflación moderada a severa y escasos infiltrados
intersticiales. La tomografía de alta resolución muestra opaci-
dades en vidrio esmerilado especialmente en língula y lóbulo
medio (“deformidad en alas de murciélago”) y atrapamiento
aéreo en los lóbulos inferiores, con una sensibilidad de 78%
y especificidad de 100% (Figuras 1A y 1B).
La única alteración histológica es la hiperplasia de células
neuroendocrinas en los bronquiolos. Esto se demuestra con
tinción inmunohistoquímica para bombesina. El resto del te-
jido puede presentar alteraciones inespecíficas (Figura 2). No
siempre es necesaria la biopsia debido al alto rendimiento del
estudio por imágenes
(13)
.
El tratamiento es de mantención, mediante oxígeno-
terapia en casos de hipoxemia. No se recomiendan los
corticoides.
Presenta buen pronóstico mostrando mejoría gradual en
meses o años, no se ha descrito mortalidad.
Enfermedad pulmonar intersticial del lactante - L. Rubilar et al
Neumol Pediatr 2014; 9 (1): 21-26.
Figura 1A.
Hiperplasia de células neuroendocrinas. Radiografía de
tórax: insuflación severa, atrapamiento aéreo, infiltrados intersticiales
bilaterales en regular cantidad.
Figura 1B.
Hiperplasia de células neuroendocrinas. Tomografía com-
putada de tórax (corte supracarinal): imágenes vidrio esmerilado en
lóbulo medio y língula, zonas de atrapamiento aéreo en ambos lóbulos
inferiores.


















