Un nicho para la regeneración alveolar
La regeneración tisular es necesaria para la restauración de la homeostasis después de una lesión grave. Algunos órganos, como el intestino, albergan células madre activas mientras que los pulmones, a menudo contienen células progenitoras facultativas que son reclutadas después de la lesión para participar en la regeneración. Recientemente se demostró que un linaje de progenitores epiteliales alveolares (PEA) que responden a la proteína WNT dentro de la población de células alveolares tipo 2 (AT2) actúa como una importante fuente de progenitores facultativos en el pulmón distal. Los PEA son un linaje estable durante la homeostasis, pero se expanden rápidamente para regenerar una gran proporción del epitelio alveolar después de una lesión pulmonar aguda. Los PEA exhiben un transcriptoma, epigenoma y fenotipo funcional distintos y responden específicamente a la señalización vía Wnt. A diferencia de otros progenitores pulmonares, las células PEA humanas se aíslan directamente mediante la expresión del marcador de superficie TM4SF, y pueden actuar como progenitoras epiteliales funcionales en organoides tridimensionales. En suma, los resultados identifican al linaje PEA como un progenitor alveolar evolutivamente conservado entre especies, que representa un nuevo blanco para la regeneración pulmonar.
Señalización vía WNT
Una fácil respiración depende de los millones de alvéolos -delicados sacos llenos de aire que son el sitio de intercambio gaseoso en los pulmones. Cada alvéolo se compone de dos tipos distintos de células epiteliales: las células epiteliales cuboides de tipo 2 (AT2), especializadas en la producción de proteínas surfactantes, y las células muy delgadas con una gran superficie, conocidas como células de tipo 1 (AT1). Estas células, junto con capilares y células del estroma, están incrustadas dentro una matriz extracelular fina y elástica (figura 1). La integridad y eficiente reparación de los alvéolos después de de las lesiones dependen en gran medida de la salud de las células AT2. Esto se debe a que constituyen -como población- las células madre epiteliales de los alvéolos: pueden auto-renovarse y diferenciarse en células AT1. El equilibrio entre estos dos comportamientos parece depender del tipo de lesión sufrido. Los primeros estudios acerca del tema, demostraron que si las células AT1 son dañadas por dióxido de nitrógeno, las AT2 proliferan y se diferencian robustamente en AT1. Por el contrario, si solo las AT2 se agotan, las sobrevivientes proliferan y se dispersan entre los alvéolos para efectuar la reparación, pero generan pocos ejemplares AT1.
Dada la importancia de las células AT2, se requiere saber más sobre qué controla su comportamiento y si existe una subpoblación especial de AT2 "de élite" que sean intrínsecamente eficientes en el mantenimiento y reparación de alvéolos. Alternativamente, tal vez la mayoría de las AT2 tienen esta capacidad, pero son mantenidas en un estado de reposo por su microambiente o nicho. En cualquier caso, identificar y aislar subpoblaciones "de elite" de AT2 o activar las AT2 "durmientes" alterando su nicho podría facilitar las terapias celulares y la reparación endógena del pulmón después de lesiones agudas. La heterogeneidad de células madre ha sido explorada y establecida en otros tejidos, incluida la piel, médula ósea, e intestino, usando una combinación de herramientas genéticas, moleculares, matemáticas y de imagen.
La comprensión del comportamiento de las células madre AT2 ha sido adelantado por estudios recientemente reportados por dos grupos - Morrisey y colegas (DOI: 10.1038/nature25786) y Desai y colaboradores (DOI: 10.1126/science.aam6603)- que alcanzaron conclusiones similares, pero con algunas diferencias. Ambos grupos usaron modelos genéticos de ratón y se centraron en la señalización evolutivamente conservada del factor de crecimiento WNT, un importante regulador de la troncalidad de muchos tejidos. Para identificar las células que responden a WNT, los dos grupos utilizaron ratones en los que la actividad de Axin2, un gen de respuesta río abajo, puede ser visualizada en los tejidos. Además, las células Axin2-positivas fueron etiquetadas indeleblemente para que su proliferación y destino pudiera ser rastreado en el tiempo.
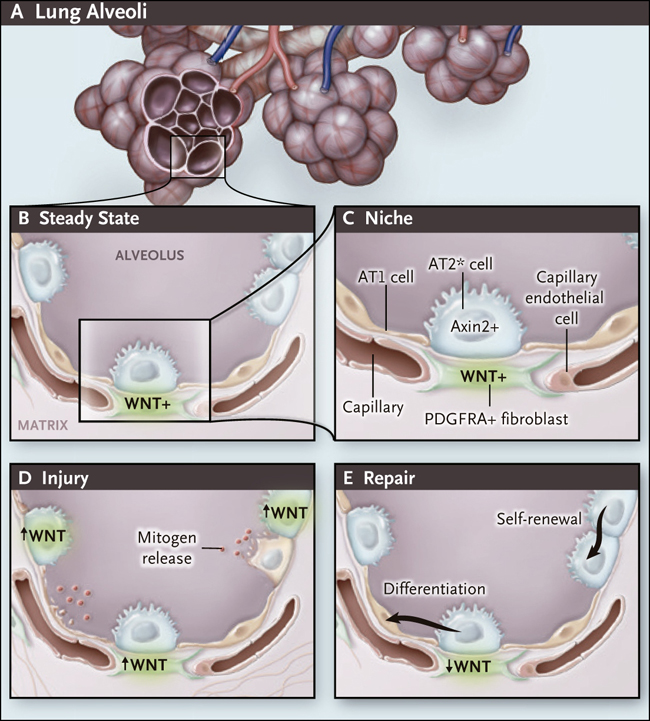
Figura 1. Señalización WNT en el nicho de células madre alveolares.
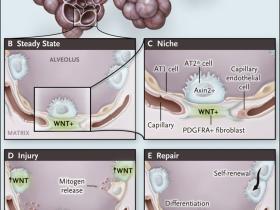
La región distal de intercambio gaseoso del pulmón está compuesta por millones de alvéolos vascularizados (panel A). Cada alvéolo contiene células epiteliales AT2 y AT1 (panel B). Se propone que una subpoblación de células AT2 (etiquetados como AT2* en el panel C) están preparados para responder a las señales proliferativas. Estas células expresan altos niveles de Axin2, lo que indica actividad de la señalización WNT. Nabhan y sus colegas sugieren que una fuente muy local del ligando de WNT es un fibroblasto PDGFRA-positivo, similar a los conocidos por estar en estrecha asociación con las células AT2. Estas células, así como las del endotelio capilar, las células AT1 y la matriz forman el micro entorno o nicho de las células AT2. Los autores indujeron experimentalmente la muerte aleatoria de células AT2 y AT1, lo que dio lugar a la producción local de mitógenos (panel D). Muchas de las células AT2 supervivientes se convierten transitoriamente en Axin2-positivas. Aumentan la expresión de sus propios WNT, que funcionan en un sistema autocrino para promover la troncalidad. A medida que la reparación continúa (panel E), la señalización WNT disminuye, y las células AT2 que han proliferado permanecen como células AT2 (autorrenovación) o se diferencian en AT1, dependiendo de la necesidad local.
El grupo de Morrisey encontró que aproximadamente el 20% de las células AT2 en el pulmón normal expresan Axin2, y la proporción no cambia mucho con el tiempo. Luego infectaron los pulmones con virus influenza H1N1. La infección mató a muchas células AT2, pero en las zonas menos dañadas que sobreviven, las AT2 proliferaron y se diferenciaron en AT1. Parecía haber proliferación preferencial y diferenciación de células AT2 Axin2-positivas, lo que sugiere que representan una subpoblación especial, llamada "progenitora epitelial alveolar" por los autores. Esta conclusión se vio corroborada por el hallazgo de que muchos genes relacionados con la proliferación y diferenciación celular están "dispuestos" a nivel genómico en los progenitores epiteliales alveolares. El grupo luego recurrió al cultivo de organoides para probar la capacidad de las subpoblaciones celulares de autorrenovarse y diferenciarse.
Encontraron que los progenitores epiteliales alveolares aparentemente dieron lugar a más y más grandes alvéolosferas que la mayoría de las células AT2. La adición de proteína WNT a los cultivos promovió la autorrenovación de las células AT2, mientras que la adición de inhibidores de WNT promovió la diferenciación a células AT1. Este resultado destaca la utilidad de los ensayos en organoides para la explorar medicamentos que potencialmente pudiesen expandir a estos progenitores y regular la diferenciación. Sin embargo, se desconoce si esto funcionará del mismo modo para los pulmones humanos.
Entre los genes que estaban presentes en mayor cantidad en las células progenitoras del epitelio alveolar, se encontró a TM4SF1, que codifica una proteína de superficie previamente identificada en el epitelio de células tumorales, por lo que los anticuerpos contra TM4SF1 fueron usados para purificar una población de células progenitoras epiteliales alveolares humanas putativas. Aunque los organoides humanos formados por células AT1 y AT2 son menos robustos que los del ratón, los resultados obtenidos por el grupo de Morrisey sugieren que las células humanas responden a WNT y a inhibidores de WNT de la misma manera.
El grupo de Desai usó una cepa de ratón diferente para visualizar la actividad de la vía WNT en el alvéolo y una nueva hibridación in situ muy sensible para respaldar sus resultados. Sorprendentemente, encontraron que sólo el 1% de las células AT2 en el pulmón normal expresaba Axin2. Entonces, indujeron la muerte de aproximadamente la mitad del epitelio alveolar. Posteriormente, muchos de las células AT2 supervivientes expresaron Axin2, proliferaron y se diferenciaron en células AT1, lo que sugirió que en tiempos de necesidad aguda, las células "durmientes" pueden convertirse en "élites".
El grupo entonces exploró cuáles células en el nicho AT2 estaban haciendo y respondiendo a WNT, centrándose en células tipo fibroblastos como que se asocian muy estrechamente con las células AT2. Usando varias herramientas para inhibir la producción y recepción de WNT, mostraron que bajo circunstancias normales, los fibroblastos cerca de las células AT2 Axin2-positivas producen y secretan WNT. Sin embargo, después de la lesión, las células "durmientes" sintetizan sus propias WNT y mantienen autónomamente su troncalidad hasta que se logra la reparación.
Actualmente, no está claro por qué los dos grupos encontraron diferencias en la proporción de células AT2 Axin2-positivas en pulmones lesionados y en estado estacionario. Tales diferencias se han observado en la investigación con células madre que involucra a otros tejidos. Sin embargo, ambos estudios concluyeron que la señalización WNT regula la robustez de las células AT2, un importante resultado que permitirá un manejo más poderoso de grupos de células progenitoras in vivo e in vitro.
Fuente bibliográfica
Stemming Lung Disease?
Brigid Hogan, Ph.D.
Department of Cell Biology, Duke University Medical Center, Durham, NC.
DOI: 10.1056/NEJMcibr1803540