Induciendo la pluripotencia
En 2007, el científico japonés Shinya Yamanaka reprogramó células adultas de la piel en un estado parecido al de las células madre por medio de un conjunto de genes. Este trabajo sobre células madre pluripotentes inducidas (iPSC) ganaron el Premio Nobel en 2012, iniciando una oleada de investigaciones, y prometiendo el desarrollo de una forma de hacer crecer tejidos a medida.
Pero las técnicas de reprogramación son todavía notoriamente ineficientes. A lo sumo, se puede convertir en torno al 10 por ciento de las células adultas en células iPS, a menudo, sólo se manejan el 0,1 por ciento. Peor aún, el proceso parecía ser demasiado azaroso, y era imposible predecir qué unidades se reprogramarían con éxito. Ahora, con los últimos avaneces, este obstáculo puede ser una cosa del pasado.
El bloqueo de la pluripotencia
Muchas actividades de traslación, incluyendo el estudio de los mecanismos de enfermedades y la medicina de trasplantes, se ven limitadas por la escasez o falta de disponibilidad de células humanas clínicamente relevantes. La derivación de células madre embrionarias humanas pluripotentes y la proliferación de métodos para dirigir su diferenciación en diversos tipos celulares representan un enfoque para superar esta escasez de tejido. El posterior descubrimiento de métodos para la reprogramación celular, incluyendo la sangre y los fibroblastos de la piel, en células madre pluripotentes (iPS) inducidas, que comparten las propiedades de las células madre embrionarias humanas, ha aumentado considerablemente la utilidad de las células madre pluripotentes, permitiéndoles, en principio, que se produzcan a partir de cualquier tejido.
Por lo tanto, la combinación de las tecnologías de biología de células madre y de reprogramación ha comenzado a entregar células a medida del paciente. Estas preparaciones incluyen, por ejemplo, cultivos de neuronas dopaminérgicas del cerebro medio que albergaban el genoma de un paciente. Tales preparaciones celulares ya han mostrado utilidad sustancial en el estudio de variantes genéticas que causan una enfermedad y probablemente serán terapias de reemplazo celular en una variedad de contextos.
El entusiasmo por la aplicación de estas tecnologías se ha extendido a muchas áreas de la medicina. Sin embargo, la ineficiencia es la principal limitación de la reprogramación de células somáticas a células iPS. Incluso los métodos más eficientes producen una sola célula iPS por cada 1.000 a 10.000 unidades somáticas sometidas reprogramación. Como resultado, la producción de células madre de un paciente dado requiere mucho tiempo, es laboriosa y costosa.
Tal vez lo más preocupante, es que ha aumentado ineficiencia extrema ya que las presiones selectivas se ejercen durante la reprogramación. Estas presiones han surgido como un obstáculo potencial a la traducción, contribuyendo posiblemente a la acumulación de anomalías genéticas o epigenéticas en las células madre resultantes. Aunque los cambios epigenéticos podrían limitar la utilidad de una línea de células madre dada, la mayor cantidad mutaciones implicadas en el control de la proliferación celular podría constituir una preocupación de seguridad.
Un reciente estudio de Yoach Rais y colegas (Nature 2013; 502:65-70) promete aliviar tales preocupaciones. Los investigadores identificaron la proteína reguladora de cromatina MBD3 (metil-CpG vinculante de dominio de la proteína 2) como una barrera principal para la reprogramación. Cuando los niveles de MBD3 se redujeron por medio de la ablación genética o caída mediada por ARN, la eficiencia de reprogramación mejoró significativamente, en algunos contextos a una tasa del 100%. También observaron una importante aceleración en la formación de células iPS humanas: un proceso que normalmente lleva 1 mes se redujo a tan sólo 7 días.
Estos estudios sugieren que MBD3 constituye un bloqueo central y conservado a la reprogramación de las células iPS. Al reducir los niveles MBD3, los autores descubrieron la cerradura de la pluripotencia, lo que permite el paso fácil a un estado de células madre. Otra buena analogía sería considerar la reprogramación de células iPS como una reacción química. Las células somáticas y los factores de reprogramación sirven como reactivos, y las células iPS son el producto. En este contexto, la eliminación de MBD3 podría ser pensado como la reducción de la energía libre necesaria para la reacción de reprogramación a producir (figura 1).
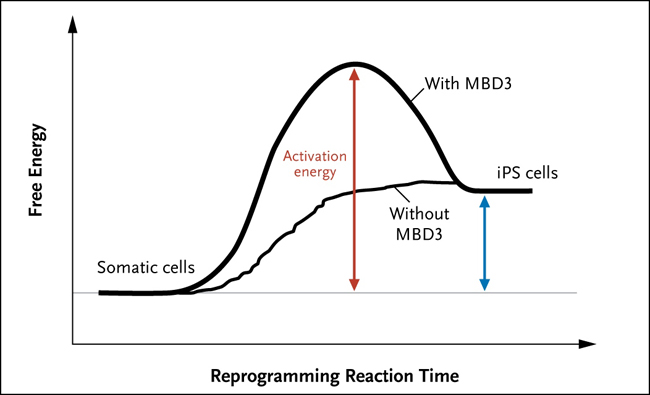
Figura 1: inducción de células madre pluripotentes
La reprogramación de células somáticas a células madre pluripotentes (iPS) es ineficiente y lenta. Un estudio reciente demuestra un enfoque oportuno y eficiente para su generación. Si las células somáticas y factores de reprogramación fuesen consideradas reactivos en una reacción química y las células iPS el producto, a continuación, la eliminación de la proteína MBD3 durante la reprogramación disminuiría la energía de activación requerida para la conversión. La flecha roja indica que la energía de activación necesaria para la reprogramación de las iPS, y la flecha azul la energía mínima para la reprogramación cuando se elimina la expresión de MBD3.
Ya que el desbloqueo de MBD3 mediado por ARN puede ser fácilmente incorporado en muchas estrategias ejecutadas rutinariamente para la reprogramación de las células iPS, el descubrimiento de estos investigadores probablemente tenga varios efectos importantes en la ciencia de la traducción. En primer lugar, la eficiencia y la velocidad de generación de células iPS limitadas por MBD3 aliviarían las preocupaciones respecto a eventos no deseados que están asociados con las presiones selectivas impuestas anteriormente por la reprogramación. Aunque se necesitan más estudios, puede ser que las células iPS producidas con este método alberguen menos mutaciones y son por lo tanto potencialmente más seguras y útiles en aplicaciones como la medicina de trasplantes.
En segundo lugar, la reprogramación eficiente y rápida con esta estrategia debe permitir la producción de líneas de células iPS a partir de un número creciente de pacientes. En lo inmediato, esta forma de reprogramación puede permitir el estudio de condiciones genéticamente complejas, tales como la esquizofrenia, o en poblaciones de pacientes con enfermedades raras. En el futuro, las mejoras adicionales inclinarán la balanza hacia la producción de líneas de células iPS de cualquier paciente, un desarrollo con implicaciones de largo alcance para diagnósticos y terapias personalizadas.
Fuente bibliográfica
Picking the Lock on Pluripotency
Kevin Eggan, Ph.D.
Howard Hughes Medical Institute, Chevy Chase, MD; and the Harvard Stem Cell Institute, the Stanley Center for Psychiatric Research, Broad Institute, and the Department of Stem Cell and Regenerative Biology, Harvard University, Cambridge, MA.
N Engl J Med 2013; 369:2150-2151