HER2 y cáncer de mama: una relación exitosa
Durante las últimas tres décadas, el riesgo de morir de cáncer de mama ha disminuido gracias a una combinación de pruebas de detección y terapia temprana, así como a más tratamientos que son efectivos y con menos efectos secundarios, especialmente con el enfoque adyuvante. Particularmente, el estudio del receptor 2 del factor de crecimiento epidérmico humano (HER2) dio inicio a una nueva era en la investigación clínica y la práctica de la oncología. Distintos agentes biológicos terapéuticos actúan a nivel de este receptor: inhiben las rutas de señalización intracelular de HER2 que son responsables de la posterior proliferación celular, migración, invasión y supervivencia, todos sellos distintivos del cáncer de mama metastásico HER2-positivo. Estos avances ofrecen un abanico de posibilidades para el progreso médico en supervivencia y curación de pacientes que sufren esta patología.
Contra el receptor epidérmico humano
En 1980, existían dos clases de terapias sistémicas disponibles para el cáncer de mama: la quimioterapia y, para las pacientes con cánceres ricos en receptores de estrógeno, la terapia antiestrógeno (más apropiadamente llamada terapia "endocrina"). A finales de los años setenta y ochenta, la explosión de las nuevas tecnologías de biología molecular condujo a la clonación genética y a la comprensión biológica de una variedad de factores de crecimiento y de sus receptores, alimentando las esperanzas de su explotación terapéutica. Entre estos descubrimientos se encuentra la identificación del factor de crecimiento epidérmico (EGF) y su receptor (EGFR) (Natl Cancer Inst Monogr. 1978 May;(48):149-56) que ahora se sabe pertenece a una familia que contiene otros tres receptores, conocidos como los receptores epidérmicos humanos, o HER.
Tres miembros de esta familia, EGFR (también conocido como HER1), HER3, y HER4, se unen a por lo menos 11 ligandos peptídicos conocidos, lo que resulta en la homo y heterodimerización entre estos receptores y subsecuentes cascadas de señalización de mediadas por tirosina quinasa río abajo del receptor. Estas cascadas de señalización estimulan la posterior proliferación celular, migración, invasión y supervivencia, todos sellos distintivos del cáncer (figura 1A). HER2 no tiene ligando conocido, pero es el socio preferido para la dimerización de los otros tres receptores (Figura 1A). El gen que codifica para HER2 (ERBB2, anteriormente conocido como neu) se amplifica y sobreexpresa en aproximadamente el 20% de los cánceres de mama recién diagnosticados. Esta observación, seguida de una investigación inspirada y tenaz tanto en la academia como en el área de la industria farmacéutica, ha cambiado la cara del cáncer de mama. Estas investigaciones han sido dirigidas en particular por los tres galardonados con el premio Lasker-DeBakey.
Poco después de la observación de que la sobreexpresión de ERBB2 ocurre frecuentemente en el cáncer de mama, estudios preclínicos de varios investigadores mostraron que los tumores que tienen esta aberración son más agresivos que los que no la tienen. Trabajando con el difunto William McGuire y otros colaboradores, los doctores Ullrich y Slamon fueron los primeros en reportar que la amplificación y sobreexpresión de ERBB2 está asociada con un peor pronóstico para las mujeres con cáncer de mama (Science. 1987 Jan 9;235(4785):177-82). Al mismo tiempo, los investigadores de Genentech habían generado un conjunto de anticuerpos monoclonales de ratón contra la proteína. Uno de ellos, denominado "MoAb 4D5", era particularmente potente en la reducción de la proliferación y supervivencia de las líneas celulares de cáncer de mama HER2-positivo (Mol Cell Biol 1989;9:1165-1172). Sin embargo, aún quedaba por superar un obstáculo importante: el desarrollo de un anticuerpo monoclonal murino "humanizado" que pudiese ser administrado de forma segura y repetida a pacientes con cáncer de mama HER2-positivo. El Dr. Shephard dirigió un equipo de colegas que injertaron con éxito el dominio de unión al antígeno murino en el esqueleto de inmunoglobulina humana, abriendo la puerta para posteriores ensayos clínicos (Proc Natl Acad Sci U S A 1992;89:4285-4289).
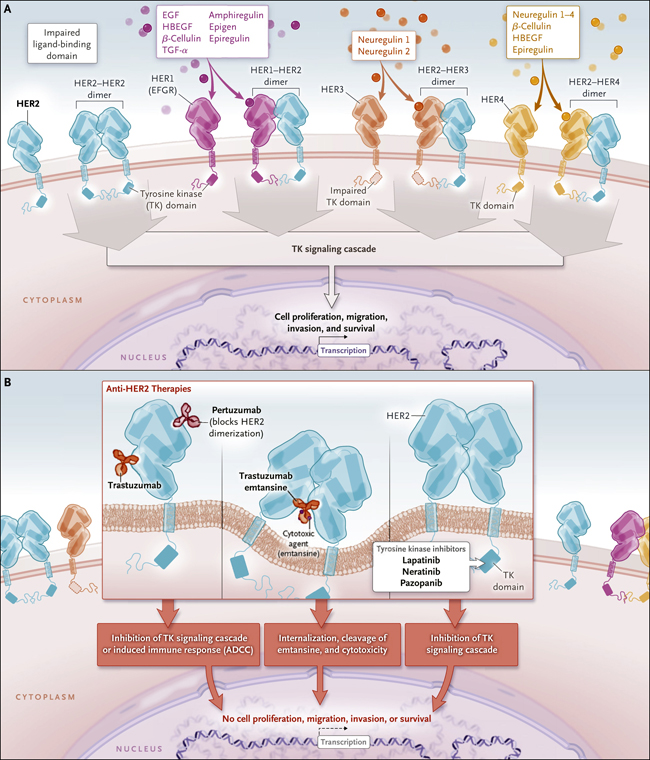
Figura 1. El Sistema del Receptor Epidérmico Humano (HER) y las formas de dirigirse a él.
Como se muestra en el Panel A, el sistema HER consta de cuatro miembros de la familia, denominados HER1 (también conocido como receptor del factor de crecimiento epidérmico[EGFR]), HER2 (codificado por ERBB2, anteriormente conocido como neu), HER3, y HER4. Al menos 11 factores de crecimiento peptídico conocidos se unen a HER1 (factor de crecimiento epidérmico [EGF], factor de crecimiento similar a la heparina [HBEGF], β-celulina, factor de crecimiento transformante α [TGF-α], anfiregulina, epigen, y epiregulina), HER3 (neuregulinas 1 y 2), y HER4 (neuregulinas 1, 2, 3, y 4; β-celulina, HBEGF; y epiregulina). HER2 no tiene dominio de ligando, pero parece actuar como un guardián para el mecanismo de acción de la familia. La unión de HER1, HER3 o HER4 induce la dimerización consigo mismo o con uno de los otros tres receptores. EGFR, HER2, y HER3 cada uno tiene un dominio tirosina cinasa que se activa con la dimerización y transmite una señal en cascada a un gen receptivo, que induce la proliferación celular, invasión, migración, o la supervivencia, todas características del cáncer. HER3 tiene un dominio de tirosina cinasa dañado. El panel B muestra las regiones de unión celular de las terapias anti-HER2. El trastuzumab y el pertuzumab, y el conjugado trastuzumab emtansine, se unen al dominio extracelular de HER2. Tanto trastuzumab como pertuzumab alteran la señalización normal de la tirosina quinasa o inducen la citotoxicidad mediada por el complemento dependiente de anticuerpos (ADCC). Por su parte, trastuzumab emtansina se interioriza y el agente quimioterapéutico se separa enzimáticamente, lo que provoca citotoxicidad. Los inhibidores de la tirosina cinasa lapatinib, neratinib y pazopanib atraviesan la membrana celular e inhiben las actividades intracelulares del dominio de la tirosina cinasa.
El dogma oncológico sostiene que las mujeres que tienen cáncer de mama metastásico no se curarán. Sin embargo, algunos de estos pacientes que han estado libres de la enfermedad por períodos prolongados de tiempo, desafían ese dogma. A pesar de todo, incluso para las muchas pacientes que tienen cáncer de mama metastásico HER2-positivo que no se curan, la terapia anti-HER2 da como resultado una mejora considerable y duradera en la calidad de vida y la supervivencia general. En este sentido, se están probando nuevos avances en el campo de la terapia anti-HER2. Los nuevos conjugados de anticuerpos y los inhibidores de la tirosina cinasa están en ensayos clínicos, al igual que las combinaciones innovadoras de terapias anti-HER2 con otros enfoques estratégicos, como los inhibidores del punto de control inmunológico. Además, se ha demostrado que trastuzumab es activo en otros cánceres no mamarios positivos para HER2, en particular en los gástricos.
Sin embargo, estos tratamientos son caros y requieren cierta experiencia en su administración, factores que limitan su disponibilidad para los pacientes que no tienen un seguro de salud adecuado y para los que viven en países de bajos ingresos. Las investigaciones en curso están dando lugar a una mayor disponibilidad de terapias anti-HER2, incluido el uso de anticuerpos biosimilares y la administración subcutánea, en lugar de intravenosa, de trastuzumab.
La comunidad médica oncológica y los pacientes deben a los doctores Ullrich, Shepard y Slamon y a los numerosos investigadores de laboratorio, traslacionales y clínicos que han desempeñado un papel en esta extraordinaria historia un gran reconocimiento. También se debe reconocer a las mujeres que han participado, y continúan haciéndolo, en los ensayos clínicos que nos han llevado a donde estamos en el tratamiento de los cánceres HER2-positivos. Las áreas de investigación en curso y planificadas en este campo continuarán guiándonos a un futuro en que aún más mujeres con cáncer de mama positivo para HER2 vivirán más tiempo o incluso se curarán.
Fuente bibliográfica
HER2 and Breast Cancer — A Phenomenal Success Story
Daniel F. Hayes, M.D.
University of Michigan Rogel Cancer Center, Ann Arbor.
DOI: 10.1056/NEJMcibr1909386