El rol de los macrófagos cardíacos
La función de los cardiomiocitos depende del ATP, cuya generación tiene lugar en la mitocondria, en donde, además, el buen rendimiento de los orgánulos probablemente sea fundamental para la función cardíaca. Se acaba de delinear un mecanismo a través del cual se eliminan las mitocondrias que han envejecido.
El corazón es como un motor de alto octanaje. Los cardiomiocitos, alimentados por ácidos grasos, son ricos en mitocondrias, ya que se necesita generar mucho ATP a través de la fosforilación oxidativa para mantener la estructura funcionando. Sin embargo, los cardiomiocitos no se queman limpiamente. Un estudio reciente de José Nicolás-Ávila y colaboradores observa que, para mantener el orden, los macrófagos dentro del corazón eliminan las mitocondrias gastadas y en descomposición. Este enfoque apunta a nuevas vías para el mantenimiento normal del miocardio y la participación de un “equipo” de limpieza, lo que es especialmente crítico después de una lesión en el miocardio.
Los macrófagos en el embrión pueblan los tejidos durante el desarrollo y se auto renuevan o se reponen de la médula ósea. Una vez en el tejido, ocupan nichos para apoyar la homeostasis y la inmunovigilancia del tejido sano. En términos de masa, los cardiomiocitos dominan la composición del corazón, pero este también incluye fibroblastos y macrófagos cardíacos (denominados aquí como macrófagos residentes en el corazón o cMacs); los cMacs se movilizan y adaptan en condiciones de lesiones. Utilizando marcadores para distinguir macrófagos cardíacos de cardiomiocitos, los investigadores mostraron que cada cardiomiocito abarca, en promedio, a cinco macrófagos (figura 1).
Se analizó entonces, la relevancia de los macrófagos para la función cardíaca al eliminar genéticamente los cMacs de los corazones de ratones adultos. Días después de la eliminación, los niveles de proteína mitocondrial se reducían en los cardiomiocitos, acumulándose anormalmente un mayor número de mitocondrias. Estas, funcionalmente dañadas, ya no producían las cantidades normales de ATP. Además, los ecocardiogramas obtenidos mostraban un menor volumen ventricular izquierdo y un llenado deficiente, características compatibles con insuficiencia cardíaca con fracción de eyección preservada.
Al utilizar marcadores para diferenciar los cardiomiocitos de sus mitocondrias y de los macrófagos, también se concluyó que las mitocondrias en realidad son emitidas por los cardiomiocitos y engullidas por los macrófagos cardíacos más cercanos. Además, los paquetes de mitocondrias expulsadas están encapsulados en estructuras llamadas exóferos. Estos exóferos cardíacos están altamente enriquecidos con proteínas mitocondriales en relación con otras proteínas de cardiomiocitos, como las motoras sarcoméricas. Apenas unos días después de "devorar" los exóferos llenos de mitocondrias de cardiomiocitos, los macrófagos ya no expresaban proteínas mitocondriales, sugiriendo que habían digerido completamente las mitocondrias gastadas.
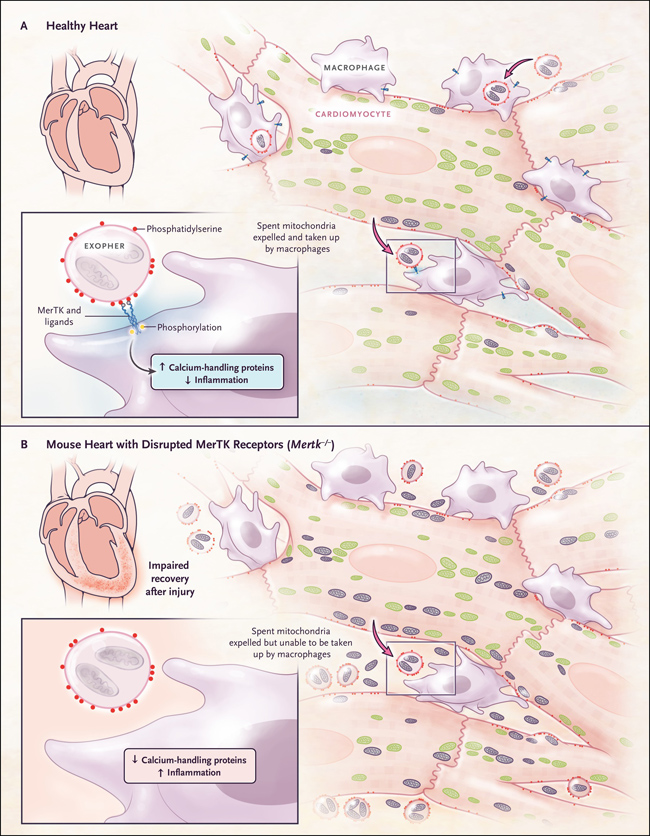
Figura 1: la salud de los cardiomiocitos mantenida por los macrófagos cardíacos
En este estudio se utilizaron modelos de ratón para mostrar que cada cardiomiocito está rodeado, en promedio, por cinco macrófagos cardíacos (panel A). Los autores se refirieron a estos como macrófagos residentes en el corazón (o cMacs) y describen cómo eliminan las mitocondrias gastadas al expulsarlas del cardiomiocito mediante estructuras conocidas como exóferos. El agotamiento de los macrófagos cardíacos produce características compatibles con la insuficiencia cardíaca con fracción de eyección conservada. También demostraron que, en ratones, la interrupción MerTK afecta directamente la capacidad de los macrófagos cardíacos para absorber mitocondrias (panel B).
El proceso de transferencia mitocondrial del cardiomiocito al macrófago requiere un sistema de autofagia que funcione normalmente, es decir, el proceso que utilizan las células para digerir los orgánulos. Bajo estrés adrenérgico, los cardiomiocitos aumentan la producción de exóferos; esto refuerza el concepto de que se necesitan macrófagos cardíacos para limpiar las mitocondrias gastadas. Los exóforos están marcados con fosfatidilserina, que sirve como una señal de "cómeme" para los macrófagos cercanos. La fosfatidilserina suele estar presente en la cara interna de las membranas; cuando se produce una lesión celular, este resto se desplaza hacia la superficie exterior de las membranas, donde puede desencadenar la activación de las células vecinas. El receptor de tirosina mieloide-epitelial-reproductivo (MerTK), un receptor en la superficie del macrófago cardíaco es clave para la activación desencadenada por fosfatidilserina. Anteriormente se había demostrado que era necesario para la recuperación cardíaca después de una lesión, en ratones que carecen de MerTK, los macrófagos cardíacos están intactos, pero no pueden absorber las mitocondrias, un hallazgo que implica a MerTK en la eliminación de las mitocondrias.
La porción extracelular de MerTK se escinde y se libera en el suero, donde se puede medir como biomarcador en pacientes después de un infarto de miocardio. Un modelo generado con una forma no escindible de MerTK mostró un mejor rendimiento cardíaco después de una lesión por isquemia-reperfusión en comparación con ratones normales, lo que indica que MerTK intacto es esencial para la función cardioprotectora de los macrófagos. Otros han demostrado que la señalización por MerTK implica la fosforilación del dominio citoplasmático de MerTK, lo que da como resultado una mayor expresión de genes que codifican proteínas manipuladoras de calcio y en la activación de vías de señalización para promover la síntesis de lípidos bioactivos que ayudan a resolver la inflamación.
La transferencia de material mitocondrial de los cardiomiocitos a los macrófagos parece ser una característica del corazón. Otros tejidos, como el bazo y el hígado, aparentemente no descargan de manera apreciable las mitocondrias gastadas hacia los macrófagos residentes. Curiosamente, el músculo esquelético muestra cierta transferencia mitocondrial a los macrófagos residentes, aunque en menor medida que en el corazón. En el músculo esquelético, las mitocondrias se acumulan en los sitios de ruptura de la membrana plasmática después de una lesión y ayudan a reparar los miocitos. El resellado o la reparación ineficaz de las células dañadas se relacionarían naturalmente con una mayor liberación de mitocondrias. Se desconoce la dependencia energética cuando se produce la liberación de exóferos, pero la célula puede equilibrar el requerimiento de energía de la reparación celular con el necesario para la liberación de mitocondrias.
Los conos y bastones de la retina también tienen muchas mitocondrias y altas tasas de fosforilación oxidativa. En seres humanos, las mutaciones en MERTK provocan ceguera; esto sugiere que las células epiteliales del pigmento de la retina, que son fagocíticas y expresan MerTK, podrían tomar exóferos de manera similar. Al igual que los cardiomiocitos, los conos y bastones de la retina poseen una prolongada vida útil, por lo que es posible que esta función de depuración sea una característica del enriquecimiento mitocondrial, de la longevidad celular y de alta energía. Los macrófagos cardíacos y la vía MerTK presentan nuevas oportunidades para mejorar la homeostasis cardíaca y así mantener el motor funcionando limpiamente.
Fuente bibliográfica
Cardiac Macrophages — Keeping the Engine Running Clean
Elizabeth M. McNally, M.D., Ph.D.
Center for Genetic Medicine, Northwestern University Feinberg School of Medicine, Chicago.
N Engl J Med 2020; 383:2474-2476