Vacunas candidatas para el virus Zika
El virus Zika (ZIKV) ha surgido recientemente como una pandemia asociada con neuropatología grave en recién nacidos y adultos. Actualmente no existen tratamientos preventivos específicos contra este patógeno. Por lo tanto, el desarrollo de una vacuna segura y efectiva es de gran prioridad. El ARN mensajero (ARNm) ha surgido como una plataforma versátil y altamente eficaz para suministrar antígenos y proteínas terapéuticas en forma de vacunas. Recientes estudios demuestran que una dosis única de una formulación sintetizada utilizando ARNm con nucleósidos modificados y encapsulados en nanopartículas lipídicas, codificantes para proteínas de envoltura virales, confiere una potente y duradera respuesta humoral neutralizante en ratones y en primates no humanos. Estos hallazgos representan un gran ejemplo acerca de cómo nuevas tecnologías basadas en biología molecular podrían dar una solución a uno de los más grandes problemas en salud pública de los últimos años.
Vacunas de ARN
La epidemia del virus Zika (ZIKV), que se inició en el año 2015, está teniendo un efecto considerable sobre la salud pública a nivel mundial, pero también en la seguridad de productos sanguíneos y sobre la seguridad de los viajes internacionales. Todos estos antecedentes alimentan aún más el debate sobre la interrupción voluntaria del embarazo. La infección por ZIKV es la última enfermedad infecciosa en revelar nuestras limitaciones en la preparación y respuesta frente a amenazas biológicas. La consecuencia más profunda de la epidemia es la gran cantidad de malformaciones congénitas que son conocidas por estar asociados o causadas por la infección viral. Además, a medida que los niños que estuvieron expuestos al ZIKV en el útero van creciendo, se están identificando nuevas anomalías del desarrollo, ampliando los efectos de la epidemia. De acuerdo con un reporte reciente de la OMS, 61 áreas han informado transmisión por ZIKV en curso desde 2015, con 31 países que reportan malformaciones congénitas que son potencialmente asociados con la infección. Sin embargo, no está claro si la transmisión se convertirá en endémica con peaks estacionales, como el dengue, o si será más episódica en la naturaleza.
Actualmente, no hay medicamentos antivirales autorizados para prevenir o tratar la infección o enfermedad causada por ZIKV, aunque grupos de investigación están explorando la posibilidad de reposicionar fármacos existentes y desarrollar nuevos compuestos. No existe ninguna vacuna con licencia para prevenir la infección. Una vez se ha producido la infección, el monitoreo clínico diligente y la atención de apoyo son los pilares del tratamiento. El cuidado de los pacientes con manifestaciones graves de la enfermedad, especialmente pacientes que sufrieron exposición intrauterina, es un desafío para todos los involucrados, y requiere una asignación sustancial de recursos, que muchas veces son limitados. Debido a estos desafíos, la OMS ha llamado al desarrollo de una vacuna contra ZIKV, con un enfoque inicial basado en la protección de las mujeres en edad fértil.
Dos estudios recientes describen pruebas experimentales exitosas de vacunas contra ZIKV en animales modelos. Uno de ellos, llevado a cabo por Pardi y colaboradores (Nature. 2017 Mar 9;543(7644):248-251) y el otro por Richner y colegas (Cell. 2017 Mar 9;168(6):1114-1125). Ambos grupos diseñaron un ARN mensajero (ARNm) con secuencias codificantes para glucoproteínas precursoras de membrana y envoltura (pRM y E, respectivamente). La proteína E es crítica para la unión del virus, para su entrada y replicación en el hospedero infectado (figura 1A), lo que la hace un objetivo racional para las vacunas. Anticuerpos neutralizantes dirigidos a la proteína E se han identificado y correlacionado con protección en vacunas dirigidas contra otros flavivirus, como el virus de la encefalitis japonesa, fiebre amarilla, y los virus de la encefalitis transmitida por garrapatas.
Pardi y sus colaboradores desarrollaron una vacuna de ARNm con un nucleósido modificado, que se basó en la secuencia de prM y de E de la cepa Polinesia Francesa 2013 del ZIKV, formulando la vacuna con nanopartículas lipídicas. El nucleósido modificado fue utilizado para reducir las respuestas inmunitarias innatas indiscriminadas después de la vacunación, y para aumentar la traducción de proteínas. Por su parte las nanopartículas lipídicas fueron diseñadas para asegurar la expresión prolongada de las proteínas (las moléculas de nucleósidos son el bloque fundamental de los ácidos nucleicos como el ARNm). Los autores vacunaron dos cepas diferentes de ratones (C57BL/6 y BALB/c), sin observar efectos secundarios agudos, y subsecuentemente detectaron la unión específica de la proteína E con anticuerpos de IgG y anticuerpos neutralizantes (figura 1B).
En los ratones C57BL / 6 también se encontró células T CD4 + específicas de antígeno después de la vacunación. Los ratones vacunados fueron desafiados con la cepa Puerto Rico 2015 de ZIKV, 2 o 20 semanas después de la vacunación. Todos los ratones vacunados fueron protegidos de la viremia (su sangre tuvo resultados negativos contra el ARN viral). Los primates no humanos (monos macacos) fueron vacunados con una de las tres dosis (50 μg a 600 μg), sin observarse efectos adversos agudos de seguridad y con producción de IgG específica para la proteína E y de anticuerpos neutralizantes. Sin embargo, no se apreció efecto dependiente de la dosis. Cuando cinco monos inmunizados y seis controles fueron desafiados con la cepa Puerto Rico de ZIKV, 5 semanas tras la vacunación, todos los últimos ejemplares se infectaron, mientras que cuatro de los cinco monos vacunados fueron protegidos de la viremia. Un solo animal vacunado tuvo una viremia de bajo nivel transiente durante 3 días tras el desafío.
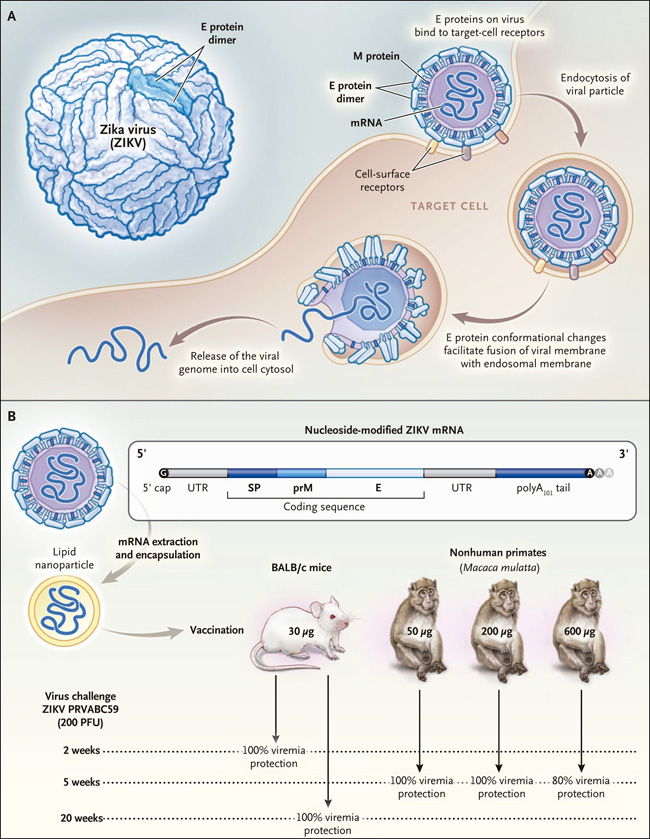
Figura 1: la proteína E del ZIKV y un candidato a vacuna de ARNm con nucleósidos modificados.
La proteína de envoltura (E) del virus Zika (ZIKV) interactúa con los receptores de superficie de las células diana (panel A), promoviendo la entrada viral, el procesamiento, y en última instancia la replicación. La presencia de una cantidad suficiente anticuerpos de alta calidad dirigidos contra la proteína E podría neutralizar el virus y reducir o prevenir la replicación viral. La neutralización del virus y la disminución de su replicación pueden impedir la infección o aminorar sustancialmente la enfermedad. Una vacuna capaz de inducir anticuerpos neutralizantes robustos puede también reducir la probabilidad de transmisión entre las personas y las poblaciones. Pardi y sus colegas basaron su vacuna candidata ARN mensajeros (ARNm) que codifican para la proteína precursora de membrana (prM) de la cepa Polinesia Francesa 2013 del ZIKV y para la proteína E (panel B). La modificación de nucleósidos y la adición de nanopartículas lipídicas formaron una vacuna de ARNm que se evaluó en ratones y en primates no humanos. En diferentes puntos después de la vacunación los roedores BALB / c y los primates no humanos fueron desafiados con la cepa Puerto Rico 2015 del ZIKV. Se encontraron altos niveles de anticuerpos neutralizantes producidos tras la vacunación y una elevada protección frente al desafío. PFU denota unidades formadoras de placas, SP péptido señal y UTR región no traducida.
Richner y sus colegas utilizaron la secuencia de prM-E de una cepa de Micronesia 2007 de ZIKV, la secuencia señal de la IgE (IgE) humana, un nucleósido modificado, un ARNm enzimáticamente sintetizado empacado en nanopartículas lipídicas en su vacuna experimental. Los autores generaron constructos de ARNm adicionales mediante la introducción de mutaciones en o cerca del ADN viral que codifica el bucle de fusión de la proteína E o mediante la sustitución de la secuencia señal de IgE con una correspondiente al virus de la encefalitis japonesa (JEVsig). Se hicieron estas modificaciones para aumentar la eficiencia de la producción de proteínas y para minimizar la generación de reacción cruzada de anticuerpos. En las pruebas de la vacuna IgEsig-prM-E en ratones (de la cepa GA129) como dosis única o doble, Richner y sus colegas encontraron anticuerpos neutralizantes específicos contra la proteína E. Seis semanas después de la vacunación, los ratonesfueron desafiados con ZIKV cepa Malasia 1966 y todos los ejemplares que recibieron la mayor dosis en forma única (10 μg) o dos dosis de 2 μg, sobrevivieron, y el 60% de los ratones que recibieron una sola dosis de 2 μg, también logró sobrevivir. Del mismo modo, en dos dosis, el régimen de 10 μg proteió totalmente a ratones C57BL / 6 ratones contra el desafío utilizando la cepa Dakar 1984 de ZIKV (ninguno de estos ratones tenían viremia 5 días después de la exposición, y ninguno murió). Contrariamente, solo el 30% de los controles sobrevivieron.
Los ratones BALB / c que se inmunizaron y se reforzaron con IgEsig–prM–E o JEVsig–prM–E, mutantes o silvestres tuvieron títulos similares de anticuerpos neutralizantes. La vacuna JEVsig-prM-E proporcionó una protección completa contra la viremia cuando los animales vacunados fueron desafiados con la cepa Dakar 1984 13 semanas después de la vacunación. Se obseró una caída de la viremia en el grupo de ratones que eran vacunados con IgEsig–prM–E. En experimentos in vitro se reveló que las mutaciones en el "loop de fusión" de redujeron el potenciamiento dependiente de anticuerpos, y estudios con un modelo de ratón para el estudio de este fenómeno mostraron una menor morbilidad y mortalidad en asociación con IgEsig–prM–E y JEVsig–prM–E.
Los datos de estudios en animales han sido descritos para numerosos en candidatos vacunales contra ZIKV, los que se han desarrollado con el uso de enfoques moleculares consistentes en la expresión de subunidades proteicas, vectores de adenovirus, viriones completos inactivados, y ahora ARNm. Los candidatos vacunales no generan ninguna señal de efectos adversos agudos, inducen una respuesta humoral o celular específica contra el virus, y confiere potección contra un desafío realizado con el patógeno. Las construcciones de vacunas de ARNm revisadas en este estudio ofrecen numerosas ventajas que incluyen el costo de su fabricación, su aplicabilidad para diversos patógenos y el favorable perfil de seguridad. Sin embargo, la inmunología constantemente advierte contra la extrapolación de conclusiones de experimentos en animales hacia humanos. En el caso de las vacunas ZIKV, la mayor parte de los datos disponibles han sido generados con el uso de animales sin exposición previa a flavivirus. Estos animales no son representativos de la mayoría de las poblaciones humanas, por lo que los resultados deben ser analizados con precaución.
Fuente bibliográfica
Zika Virus Vaccines — A Full Field and Looking for the Closers
Stephen J. Thomas, M.D.
Division of Infectious Diseases, State University of New York Upstate Medical University, Syracuse.
DOI: 10.1056/NEJMcibr1701402