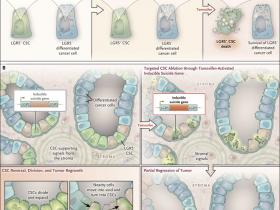
¿Eliminar células madre cancerosas para salvar el colon?
Las células madre cancerosas (CSC, del inglés cancer stem cells) se han propuesto hipotéticamente como impulsoras de la progresión tumoral y metástasis, convirtiéndolas en atractivas dianas terapéuticas. Sin embargo, todavía faltan pruebas experimentales concluyentes sobre su relevancia funcional para la mayoría de las neoplasias malignas. Recientemente estudios han mostrado que el receptor Lgr5 identifica a CSC intestinales de modelos de tumor en ratones que sirven para el estudio de la progresión clínica del cáncer colorectal humano. Particularmente se observó que la eliminación selectiva de la población celular que presenta el receptor Lgr5, restringe el crecimiento tumoral primario, pero no produce regresión tumoral. En su lugar, los tumores son mantenidos por células proliferativas Lgr5+ que intentan continuamente reponer la reserva de las CSC Lgr5+, lo que conduce a una rápida reiniciación del crecimiento tumoral al cesar el tratamiento. En particular, las CSC son críticas para la formación y mantenimiento de metástasis hepáticas derivadas de cánceres colorrectales. Por lo que estos hallazgos resaltan las distintas dependencias de las CSC para el crecimiento tumoral primario versus el metastásico, y sugieren que los enfoques que apunten a las CSC pueden representar una oportunidad terapéutica para el control de la enfermedad metastásica.
Desdiferenciación de células
Se cree que la muerte de las células madre cancerosas (CMC) son un componente crítico de las terapias antitumorales eficaces. Las CMC están en el ápice de una jerarquía que está presente en múltiples tipos de cáncer. Particularmente, en el cáncer colorrectal, es bien aceptado que las CMC, que pueden ser aisladas de tumores humanos y de ratones con el uso de marcadores específicos, pueden iniciar rápidamente el crecimiento tumoral en la transferencia a ratones. Sin embargo, a menudo la progenie diferenciada de estas células no puede iniciar tal crecimiento, lo que sugiere que las CMC alimentan el crecimiento del cáncer de una manera similar a la que las células madre normales conducen a la renovación de los tejidos y a la homeostasis.
Dos grupos de investigadores - liderados por de Sousa e Melo (Nature 2017; 543: 676-80) y Shimokawa (Nature 2017; 545: 187-92) se han enfocado las células madre del cáncer de colon, usando un modelo de ratón de cáncer colorrectal o xenoinjertos. Ambos grupos usaron la misma táctica para matar células madre cancerosas bajo condiciones in vivo: el knock in genético de un constructo que induce la muerte celular activable por pérdida del gen LGR5 (figura 1). Debido a que LGR5 se expresa específicamente en células madre del cáncer de colon de humanos y ratones, el sistema de "suicidio" inducible proporcionó a los investigadores un medio para eliminar selectivamente células madre cancerosas en crecimiento.
Inicialmente, ambos grupos observaron regresión tumoral, como se esperaría ver si la fuente de crecimiento del cáncer fuese eliminado (figura 1). Sin embargo, también notaron que la regresión fue limitada y temporal. Después de que el "interruptor" fue removido - es decir, después de que la ablación específica de células madre tumorales se detiene, aparecen rápidamente nuevos ejemplares celulares positivos para portadores de LGR5 y los tumores regresan.
Shimokawa y sus colegas mostraron que la desdiferenciación de células tumorales maduras era la fuente de estos nuevos ejemplares de células de cáncer de colon (figura 1) y propusieron que el microambiente es crítico para este restablecimiento. Este concepto está fuertemente respaldado por hallazgos anteriores en los que se observó que las células madre cancerosas residen en un nicho del estroma que refuerza el estado de tumoral y que también puede inducir características cancerosas y de troncalidad en las células tumorales ya diferenciadas. Además, estas observaciones son congruentes con la plasticidad observada de las células intestinales, en las cuales se evidencia una desdiferenciación celular o un vuelco hacia un estado de troncalidad cuando las células están bajo estrés. Los autores también propusieron que eliminar las células madre cancerosas liberaría el nicho y permitiría que las células tumorales diferenciadas llenen el espacio para convertirse en células madre cancerosas. Queda por determinar qué factores impulsan esta desdiferenciación y si todas las células tienen la capacidad de sufrir este proceso inverso. Sin embargo, la prueba de que la "troncalidad" es un rasgo dinámico hace que orientar los esfuerzos terapéuticos a las células madre colorrectales sea más desalentador de lo que se pensaba.
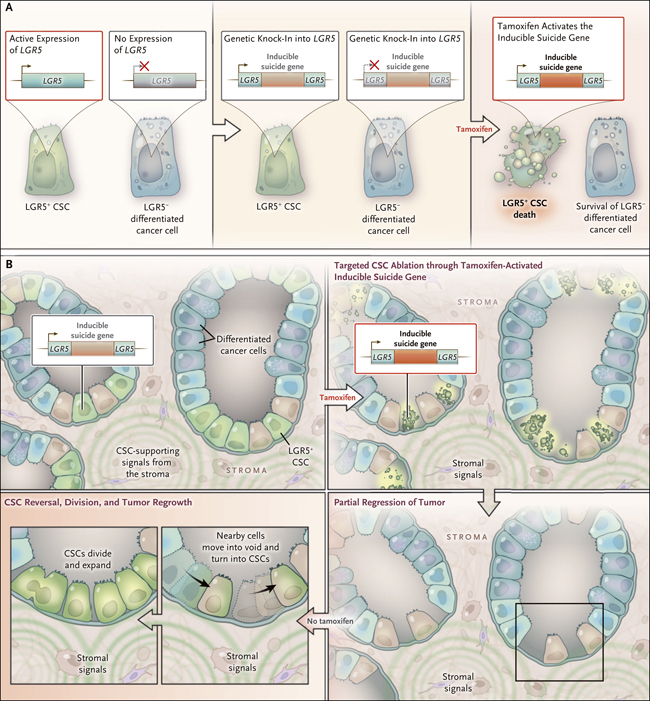
Figura 1. La sabia célula madre del cáncer de colon.
Dos estudios recientes proporcionan información sobre la procedencia de las células madre del cáncer de colon (CSC, del inglés cancer stem cells). El panel A muestra la expresión específica de LGR5 específica de las CSC (verde indica la expresión, y el azul indica ausencia de expresión) combinada con la manipulación genética que permite la introducción de un gen "suicida" inducible desencadenado por la expresión de LGR5 y activado por la inyección de tamoxifeno, resultando en la muerte de CSC de colon solo cuando se inyecta tamoxifeno. Las células tumorales ya diferenciadas no expresan LGR5 y por lo tanto no producen el gen LGR5, y así sobreviven. El panel B muestra la activación del mecanismo suicida en el crecimiento de tumores que resulta en una ablación completa de las CSC positivas para LGR5. Mientras el mecanismo de suicidio se mantenga activo, se produce una regresión tumoral, pero después de que su suicidio ya no es inducido las células tumorales diferenciadas se mueven hacia el espacio disponible y readquiren las cualidades de una CSC. Por lo tanto, se produce un rápido crecimiento del tumor.
Pese a lo anterior, no todo son malas noticias. de Sousa e Melo y sus colegas descubrieron que incluso aunque el crecimiento del tumor primario solo se detiene temporalmente por la eliminación de células madre cancerosas, la "siembra" metastásica y el crecimiento de las metástasis preestablecidas sufre una detención. Esto implica que, a diferencia de lo que ocurre con el cáncer en el sitio primario, las metástasis dependen de células madre preexistentes del cáncer LGR5-positivo y éstas no tienen la capacidad de inducir el cáncer de novo de las células madre. El motivo por el que la desdiferenciación no ocurre en sitios metastásicos no ha sido clarificado. Una explicación podría ser que en el establecimiento rápido de metástasis inherentes a este modelo de ratón, los factores de nicho necesarios están ausentes, y la desdiferenciación de células epiteliales del colon hacia células madre cancerosas no se favorece.
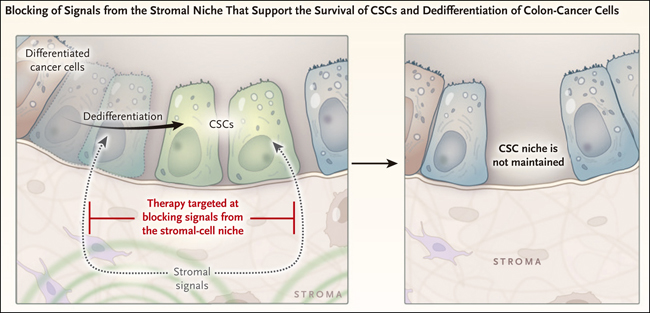
Figura 2. Abordando las células madre cancerosas del colon.
El aspecto dinámico de las CSC del colon puede proporcionar oportunidades para una nueva terapia experimental. Las señales que conducen la desdiferenciación pueden ser identificadas y potencialmente abordadas para prevenir la reinstauración de las CSC. De forma similar, agentes que apuntan a la interacción entre el nicho estromal y las CSC podrían ser una opción terapéutica interesante. Aún queda por determinarse si las señales que inducen la desdiferenciación y las señales de mantenimiento de las CSC son distintas o idénticas.
Shimokawa y colegas buscaron una combinación de terapias para atacar las células madre del cáncer de colon. Mostraron que el bloqueo con cetuximab (que se une al factor de crecimiento epidérmico) potencia la expresión de LGR5 in vivo y por lo tanto, parece expandir el grupo de células medre cancerosas. Cuando este bloqueo se combinó con la posterior ablación de las células madre cancerosas, el efecto sobre la regresión tumoral en ratones fue mucho más más fuerte que con cualquiera de los tratamientos individuales. A pesar de que tal terapia combinada requerirá un análisis más profundo antes de su aplicación en humanos, los datos ilustran que el modelo desarrollado por los autores representa una herramienta que permite identificar nuevas terapias de combinación para eliminar células madre de cáncer colorrectal y prevenir su "resiembra" tras la desdiferenciación.
Que las células madre cancerosas y la desdiferenciación de las células del colon estén favorecidas por el microambiente también abre nuevas posibilidades. De hecho, la localización de células LGR5 positivas hasta el borde del crecimiento tumoral sugiere que la información posicional es transmitidas para "instruir" a las células madre cancerosas. Si tales señales también instruyen a las células para sufrir desdiferenciación, representaría un blanco terapéutico experimental que al ser inhibido eliminaría la mantención de células madre cancerosas y el proceso de desdiferenciación (figura 2). En resumen, el trabajo de ambos grupos de investigadores apunta a nuevas estrategias para combatir a las células madre del cáncer colorrectal.
Fuente bibliográfica
Targeting the Colorectal Cancer Stem Cell
Jan Paul Medema, Ph.D
Laboratory of Experimental Oncology and Radiobiology, Cancer Center Amsterdam, Academic Medical Center, Amsterdam.
DOI: 10.1056/NEJMcibr1706541