Un paso más hacia una vacuna contra el VIH
A pesar de su éxito comprobado en la supresión de la replicación del virus de la inmunodeficiencia humana (VIH), la terapia antirretroviral (TAR) no elimina el reservorio viral y se asocia con una restauración incompleta del sistema inmunológico. Los tratamientos dirigidos al reservorio del VIH son un posible enfoque adicional para lograr una remisión sin tratamiento (o una cura funcional). El inicio de la TAR durante la infección aguda por VIH da lugar a un menor tamaño del reservorio y podría limitar el daño inmunológico, aumentando la capacidad de la inmunidad del hospedero para controlar la replicación viral. Sin embargo, aún no se ha resuelto si estas respuestas inmunológicas son suficientes para mediar un estado de remisión del VIH sin necesidad de la TAR. Recientemente se ha determinado que un régimen de vacunas heterólogas basada en dos vectores virales diferentes codificantes de antígenos mosaico del VIH es seguro e inmunogénico en primates no humanos y en estudios clínicos. Estos potentes vectores son capaces de provocar una amplia gama de respuestas humorales y celulares, además de retrasar el rebote del VIH tras la interrupción de la TAR. Por lo tanto, este régimen de inmunización puede ser una intervención que logre la anhelada remisión en pacientes seropositivos.
Rebote viral
En las personas con infección establecida por el virus de la inmunodeficiencia humana (VIH), la inmunidad del huésped al patógeno se ha vinculado con un control parcial de la replicación viral. Sin embargo, aún no se ha resuelto si esas respuestas inmunológicas son suficientes para mediar un estado de remisión del VIH sin tratamiento antirretroviral (TAR) después de la interrupción de esta terapia o cómo inducir esas respuestas mediante cualquier intervención en personas infectadas. En un estudio publicado en Nature Medicine, Donn Colby y colaboradores informan los resultados preliminares de una vacuna terapéutica en personas infectadas por VIH que habían iniciado TAR poco después de la infección (Nat Med. 2020 Apr;26(4):498-501).
En la gran mayoría de las personas infectadas con VIH que están en TAR, después de la interrupción de la terapia, los provirus competentes para replicación en el reservorio viral impulsan un rápido rebote viral en un plazo de 2 a 4 semanas. Curiosamente, en varios estudios, los niveles más bajos del reservorio viral se han asociado con un retraso en el tiempo de rebote viral. Aunque tal vez no se logre la erradicación completa, muchas de las estrategias de curación actuales tienen por objeto movilizar y reducir el reservorio a niveles que permitan un control eficaz y sostenido del virus.
Es bien sabido que las personas que pueden iniciar la TAR en las primeras semanas después de la adquisición del VIH suelen presentar niveles más bajos de reservorios, menor agotamiento del sistema inmunitario y menos variantes virales adaptadas al sistema inmunitario que las personas que inician TAR en etapas posteriores de la infección. Así, se ha formulado la hipótesis de que las personas que reciben TAR en las primeras fases pueden inducir una respuesta inmunológica protectora capaz de controlar su reservorio viral después de la vacunación terapéutica, ya que el reservorio es más pequeño y menos adaptado. Esto también se apoya en la noción de que hasta el 10-15% de las personas tratadas en forma temprana pueden ser capaces de mantener la viremia en niveles indetectables o bajos después del cese de la terapia (controladores postratamiento) sin necesidad de ninguna intervención inmunológica. Si bien los mecanismos precisos que conducen al control posterior al tratamiento siguen siendo difíciles de elucidar y pueden diferir de los mecanismos que intervienen en el control espontáneo del VIH, parece plausible que la respuesta inmunológica inducida del huésped durante la infección primaria y preservada por la TAR temprana pueda desempeñar un papel fundamental en la capacidad de esas personas para contener el rebote viral.
Colby y sus colegas llevaron a cabo un estudio de una vacuna terapéutica en 26 personas infectadas por VIH y suprimidas por el TAR en Tailandia, que fueron tratadas en las primeras etapas de su infección por (etapas I a IV de Fiebig). La vacunación en este estudio incluyó un régimen de cuatro inyecciones utilizando formulaciones con dos vectores virales diferentes, Ad26 (adenovirus) y MVA (vacuna modificada de Ankara), que expresan dos inmunógenos mosaicos multivalentes de las proteínas del VIH Gag, Pol y Env. Las vacunas se administraron dos veces cada una en un período de 12 meses. Estos novedosos inmunógenos en mosaico se diseñaron in sílico para aumentar la cobertura de la inmunización de los posibles epítopos de células T en los virus en circulación y tenían por objeto hacer frente a la diversidad del VIH de tipo 1 y limitar la capacidad del virus para escapar a la inmunovigilancia. En experimentos anteriores en un modelo de primate no humano del virus de la inmunodeficiencia de los simios, las vacunas de mosaico, administradas solas o en combinación con un agonista del modulador inmunitario TLR7, mostraron tanto un retraso en el rebote viral como una reducción significativa del punto de referencia viral después de la interrupción de la TAR, en los animales tratados tempranamente. Cabe destacar que en el estudio con primates no humanos, el tiempo transcurrido hasta el rebote viral y el punto de ajuste viral se correlacionaron con los niveles de células T inducidas por la vacuna, lo que respalda las pruebas clínicas de esta estrategia.
Colby y colaboradores encontraron que en humanos la intervención era segura, inmunogénica e indujo altos niveles de células T CD4+ polifuncionales y linfocitos T CD8+, además de anticuerpos específicos de la envoltura. Durante una fase exploratoria de interrupción de la TAR, los 17 participantes del brazo activo mostraron un retraso no significativo en el tiempo de rebote viral de 21 días, en comparación con los 15 días de rebote viral de los controles con placebo (figura 1). Todas las personas, excepto un receptor de placebo, tuvieron que reanudar el tratamiento según el protocolo, ya que cumplían los criterios para dos determinaciones consecutivas de viremia > 1.000 copias por ml, con una semana de diferencia. Como concluyeron los autores, la tendencia al rebote retardado fue demasiado corta para afectar positivamente al tratamiento clínico de la infección, pero reprodujo parcialmente el rebote retardado observado en el modelo de primate no humano.
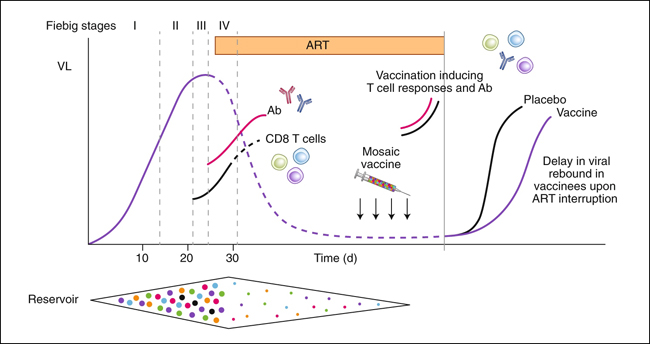
Fig. 1: Representación esquemática de la cinética de la carga viral (VL) del VIH durante la infección aguda y reciente, y tras la interrupción del tratamiento antirretroviral.
La siembra del reservorio viral se produce después de los primeros días de la adquisición del VIH, y se inducen respuestas celulares y humorales durante la infección aguda y temprana del VIH mientras el reservorio aumenta progresivamente en diversidad viral. Las vacunas de mosaico están diseñadas para hacer frente a la diversidad del VIH e inducir tanto anticuerpos como células T específicas contra el VIH. En el estudio de Colby y sus colegas, las vacunas de mosaico fueron inmunogénicas y pudieron retrasar el rebote del VIH después de la interrupción del tratamiento antirretroviral. Los estudios en curso aclararán cómo las respuestas inducidas por las vacunas coinciden con las secuencias de los virus preexistentes y de rebote.
No obstante, a pesar del modesto efecto clínico, se pueden extraer varias lecciones del estudio de Colby y colaboradores, especialmente con respecto al diseño de futuros ensayos y las posibles lecturas en el campo terapéutico. En primer lugar, la interrogante de si un grupo placebo es realmente necesario para la validez científica en estudios piloto en los que participan grupos de VIH tan singulares y escasos que también presentan un rebote viral casi universal y para los que las comparaciones de eficacia entre grupos no pueden tener suficiente potencia. En segundo lugar, la estratificación por genotipo de HLA tras la asignación aleatoria entre los brazos podría ser necesaria para limitar los posibles efectos de la genética del huésped en los resultados, como se destaca en el presente estudio. Como han mencionado los autores, los criterios conservadores de reanudación de la terapia antirretroviral utilizados en el estudio pueden haber reducido la posibilidad de detectar cualquier posible control del virus después de una fase inicial de viremia transitoria. Ese control posterior al rebote solo puede producirse después de que las respuestas de las células T de memoria inducidas por la vacuna sean estimuladas por primera vez por el virus de rebote para recuperar las funciones efectoras plenas o la residencia del tejido pertinente para eliminar las células infectadas.
Alternativamente, también pueden requerirse mecanismos inmunológicos innatos conocidos como "efectos vacunales" desencadenados por una viremia transitoria antes de que el virus pueda ser controlado eficazmente. Dado que más del 30% de los casos de control posterior al tratamiento pueden ocurrir después de una viremia transitoria superior a 10.000 copias por mL, puede ser necesario emplear criterios de reanudación de la TAR más relajados para ofrecer a los que entran en una interrupción analítica del tratamiento (ITA) la posibilidad de lograr un control eficaz posterior al rebote. Sin embargo, los niveles elevados de viremia durante un período prolongado también aumentan considerablemente el riesgo de transmisión viral durante la ITA, y cualquier enfoque de ese tipo requeriría una mitigación efectiva del riesgo para evitar esa transmisión.
Como se muestra en el estudio de Colby y colaboradores, la vacunación terapéutica fue capaz de inducir respuestas inmunológicas robustas y amplias. Sin embargo, queda por determinar si la falta de control del virus puede haberse debido a una estimulación aún insuficiente de las respuestas inmunitarias, a perfiles de respuesta inadecuados, a la falta de movilización de los reservorios, a una cobertura limitada de los virus autólogos o a la expansión de las respuestas de las células T y B a objetivos irrelevantes del virus. Se espera que los análisis de comparación de secuencias de virus preexistentes y de rebote, conocidos como análisis de "efecto de tamiz", así como la caracterización detallada de la inmunidad del huésped antes del inicio de la TAR y durante la ITA, ayuden a dilucidar los mecanismos que determinan la cinética de rebote.
Por último, los resultados de este estudio no pueden ocultar el hecho de que el campo de la cura del VIH está todavía muy lejos de reproducir los recientes avances realizados en el modelo de primate no humano. En particular, existe una necesidad urgente de comprender mejor los mecanismos asociados con la infección primaria y el rebote viral durante la interrupción analítica del tratamiento, no solo para facilitar el diseño de nuevas intervenciones destinadas a reproducir los fenotipos controladores posteriores al tratamiento, sino también para ayudar a optimizar los diseños de los ensayos de curación. Sin embargo, las indicaciones positivas de la labor de Colby y sus colegas justifican claramente que se sigan ensayando vacunas mejoradas y estrategias combinadas.
Fuente bibliográfica
Small steps forward for HIV vaccine development
Beatriz Mothe & Christian Brander
IrsiCaixa AIDS Research Institute, Badalona, Spain
Nat Med. 2020 Apr;26(4):466-467
Temas Relacionados