Terapia oral selectiva para la enfermedad de Crohn
Nuevas publicaciones informan los resultados de ensayos con upadacitinib (fármaco de molécula pequeña que inhibe la proteína Janus quinasa [JAK] 1 [JAK1]) para el tratamiento de la enfermedad de Crohn de moderada a grave.
La enfermedad inflamatoria intestinal (EII) incluye la colitis ulcerosa y la enfermedad de Crohn. Estos son trastornos intestinales idiopáticos inmunomediados se caracterizan por inflamación en la evaluación endoscópica, histológica y radiográfica. Mientras que la colitis ulcerosa se limita a la mucosa del colon, la enfermedad de Crohn puede afectar a cualquier parte del tracto gastrointestinal, aunque suele abarcar al íleon, colon o a ambos.
La EII es una afección del mundo desarrollado. Su incidencia se ha mantenido en América del Norte y Europa, aunque está aumentando en Asia y América Latina y entre los inmigrantes en Estados Unidos. Las personas negras e hispanas tienen peores resultados que las blancas no hispanas, posiblemente debido a un diagnóstico más tardío y al menor uso de medicamentos biológicos.
La mayoría de los pacientes presentan dolor abdominal, diarrea y fatiga. Los niños con Crohn son susceptibles de retraso en el crecimiento. La anemia por deficiencia de hierro es frecuente. Las fístulas perianales, una complicación mórbida, se desarrollan en aproximadamente el 20% de los afectados. Otras manifestaciones extraintestinales incluyen artritis y pioderma gangrenoso o eritema nodoso.
Las causas de Crohn son heterogéneas y complejas. Hay más de 240 loci implicados en su patogénesis; la mayoría de los estudios genéticos se han limitado a poblaciones europeas. Sin embargo, se sabe que los cambios en el microbioma y la activación de la respuesta inmune de la mucosa son requisitos para la expresión de la patología. Los estudios de activación de vías inmunitarias implican inflamación mediada por células T helper 17 (Th17) y el factor de necrosis tumoral (TNF), la interleucina-23, interleucina-17 e interferón-γ. Sin embargo, la causa raíz aún se desconoce.
El advenimiento de la terapia anti-TNF fue fundamental para el tratamiento de la enfermedad de Crohn. Infliximab y, posteriormente, adalimumab, que inhiben al TNF, dieron lugar a una mayor probabilidad de remisión clínica a corto plazo y, entre los pacientes que inicialmente responden, también a largo plazo. Se ha utilizado la endoscopia para establecer la eficacia en los primeros ensayos de infliximab y adalimumab. En estos, la actividad endoscópica (úlceras e inflamación) disminuye o se resuelve con el tratamiento; estos resultados han marcado el comienzo de la era actual en la que la cicatrización de la "mucosa", determinada por la actividad endoscópica, es el punto final terapéutico predominante. El talón de Aquiles de la terapia anti-TNF, especialmente con infliximab, incluye la inmunogenicidad y la pérdida de respuesta. Desafortunadamente, los individuos que no responden tienen una respuesta deficiente a los subsiguientes agentes.
Por otra parte, se cree que la producción de interleucina-23, principalmente por macrófagos intestinales CD14 positivos (pero también por células dendríticas y células epiteliales) en la mucosa del intestino, activa las células Th17, lo que hace que produzcan TNF, interleucina-6, interleucina-17A, e interleucina-22, que perpetúan la inflamación (figura 1). La interleucina-23 comprende dos subunidades: p19 y p40. Los agentes biológicos aprobados para el tratamiento de la enfermedad de Crohn incluyen inhibidores de la interleucina-23, como ustekinumab (que se dirige a la subunidad p40 y, por lo tanto, inhibe la interleucina-12, una citocina compuesta por p40 y otra subunidad proteica), risankizumab (que se dirige a la subunidad p19) y guselkumab (que también se dirige a p19 y aún está bajo investigación). Ustekinumab tiene una eficacia modesta en pacientes que han estado expuestos a agentes anti-TNF; hay alguna indicación de que los inhibidores más nuevos, que se dirigen a p19, pueden tener una mayor eficacia.
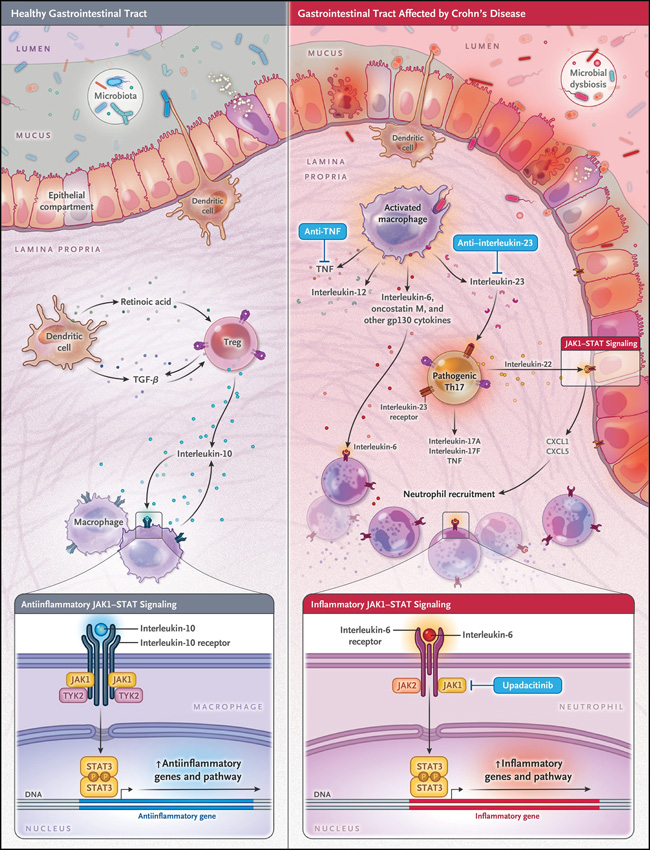
Figura 1: blancos de la mucosa en la enfermedad de Crohn.
Respecto a vedolizumab, que inhibe el tráfico de linfocitos de localización intestinal hacia el intestino (inhibe la integrina α4β7 en la superficie de los linfocitos), es eficaz en quienes no han recibido tratamiento previo, pero menos en los que ya han sido tratados con anti-TNF.
¿Por qué las JAK son dianas en la enfermedad de Crohn? Upadacitinib es un inhibidor de molécula pequeña de JAK1 (figura 1 y figura 2). Los transductores de señales y activadores de la transcripción (STAT) son factores de transcripción que, al ser fosforilados por una JAK, se translocan al núcleo, se unen a secuencias de ADN afines y activan la transcripción de ciertos genes. En la estrategia "Lego" utilizada por el sistema inmunitario, diferentes receptores de citoquinas se unen a parejas de JAK y STAT para orquestar una respuesta inmunitaria apropiada o, en el caso de la EII, inapropiada. En pocas palabras, debido a que las citoquinas en sí mismas son dianas de fármacos eficaces, los componentes de las vías a través de las cuales emiten señales también son candidatos objetivos. En un estudio que examinó células inmunitarias innatas aisladas de muestras de biopsia intestinal obtenidas de pacientes con EII, múltiples genes JAK-STAT y la vía STAT3 se regularon al alza en el tejido inflamado. Curiosamente, tofacitinib, que inhibe a JAK1, JAK2 y JAK3, fue ineficaz en la enfermedad de Crohn, incluso a dosis más altas, pero competente en el tratamiento de la colitis ulcerosa.
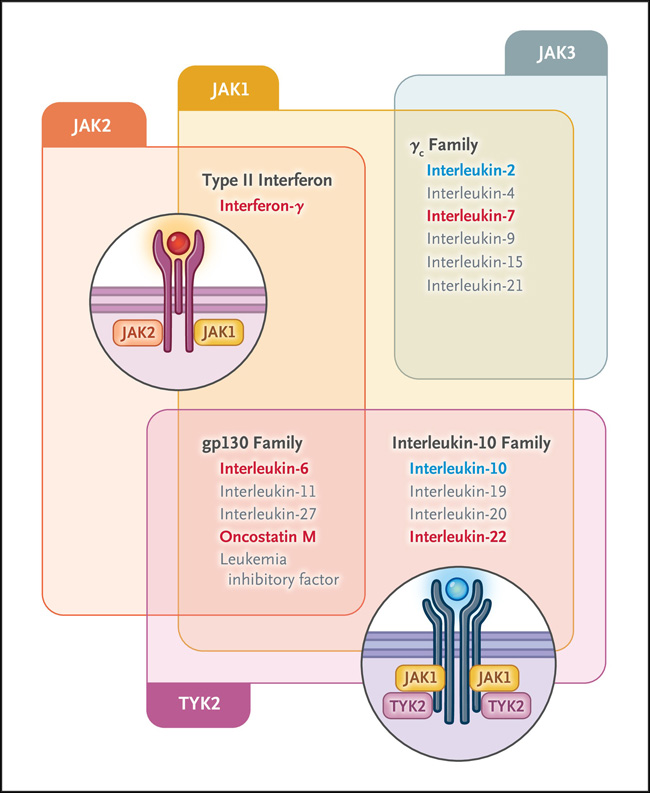
Figura 2: vías de citoquinas dependientes de JAK1 en la enfermedad de Crohn.
¿Es upadacitinib efectivo? Sí. A pesar de los decepcionantes resultados con tofacitnib, fue eficiente en el tratamiento de la enfermedad de Crohn de moderada a grave. Un factor importante para evaluar la eficacia es la proporción de pacientes que fueron tratados previamente con productos biológicos. Aproximadamente el 75% de ellos había estado expuesto a al menos un fármaco biológico. En los ensayos de inducción, el porcentaje que tuvo remisión clínica fue casi el doble con upadacitinib que, con placebo, y el porcentaje con respuesta endoscópica fue al menos tres veces mayor.
Es difícil comparar los hallazgos entre los estudios debido a las diferencias en las características de los pacientes y los criterios de valoración. Dicho esto, las incidencias de remisión clínica observadas son mayores que en la mayoría de los estudios con fármacos biológicos para tratar la enfermedad de Crohn. Además, upadacitinib tiene más probabilidades que placebo de resolver las manifestaciones extraintestinales. La falta de eficacia de tofacitinib puede deberse a problemas de los ensayos clínicos (p. ej., alta respuesta al placebo o falta de endoscopia). También puede haber disparidades no apreciadas en los efectos funcionales de los diferentes inhibidores de JAK.
Upadacitinib se administra por vía oral. Los pacientes y médicos generalmente están preocupados por los productos biológicos inyectables y tienden a sentirse menos intimidados por los medicamentos orales, que pueden suspenderse e iniciarse sin consecuencias potenciales de inmunogenicidad. También hay menos pérdida de un fármaco de molécula pequeña que de uno a base de proteínas en pacientes con enteropatía con pérdida de proteínas derivada de una inflamación intestinal grave.
¿Qué hay de los efectos secundarios? Se ha informado un impacto de dosis sobre el riesgo de infección por herpes zoster, hallazgo consistente con los de clase conocidos de los inhibidores de JAK. No hay evidencia de complicaciones cardiovasculares o tromboembólicas, que se observaron previamente en pacientes con artritis reumatoide tratados con tofacitinib y que dieron lugar a una advertencia. Sin embargo, se requerirá de un mayor número de personas durante más tiempo para determinar si upadacitinib está asociado con un peligro de tales complicaciones.
Entre los eventos adversos específicos de upadacitinib más comunes se encuentran la anemia y el acné. El aumento de la primera puede deberse a los efectos no deseados sobre la señalización de eritropoyetina a través de JAK2. Además, se han registrado perforaciones intestinales, registros que recuerda a los estudios de enfermedad de Crohn realizados con anti-interleucina-6, que también se vincula a estos problemas.
Finalmente, es importante comprender la amplitud de la eficacia de upadacitinib en el espectro completo de la enfermedad de Crohn. Las fístulas perianales son una complicación angustiante, a menudo dolorosa, y los polimorfismos en JAK1 se han relacionado con la condición fistulizante perianal. Se requieren más estudios sobre su uso en pacientes con enfermedad perianal, así como análisis de medicamentos en individuos negros e hispanos, que han estado subrepresentados. También se justifica una evaluación oportuna de seguridad en el embarazo y los efectos sobre la fertilidad; las personas con EII suelen ser jóvenes y no se les debe negar innecesariamente el acceso a los inhibidores de JAK.
Fuente bibliográfica
JAK1 Inhibition to Treat Crohn’s Disease
Maria T. Abreu, M.D.
Department of Medicine, Division of Digestive Health and Liver Diseases, and the UHealth Crohn’s and Colitis Center, University of Miami Miller School of Medicine, Miami.
N Engl J Med 2023; 388:2005-2009