Suministrar insulina evadiendo la inmunidad
La inhibición inmunitaria mediada por el receptor PD-1 y su ligando, PD-L1, es el objetivo de supresión de los fármacos para tratar el cáncer. ¿Podría el aumento de este eje inhibidor evitar que el sistema inmunitario rechace las células tipo islote trasplantadas? Un estudio reciente ofrece una respuesta cualificada.
Hay pocas experiencias más angustiosas para una familia que descubrir que un niño tiene diabetes tipo 1 y que necesitará inyecciones de insulina de por vida. En las personas sanas, las células beta pancráticas suministran insulina directamente a la circulación minuto a minuto para regular las concentraciones de glucosa en sangre. A pesar de los avances en las bombas de insulina y sensores de glucosa, la administración de insulina en tejido subcutáneo con acceso retardado a los tejidos diana puede restablecer solo parcialmente el control glucémico, y con una atención constante.
Las personas con diabetes tipo 1 se enfrentan a una incesante lucha, día y noche, por mantener el rumbo entre la hipoglucemia que pone en peligro la vida y las consecuencias a largo plazo de la hiperglucemia, como falla renal y ceguera. La sustitución de células beta mediante el trasplante de páncreas o islotes revierte la diabetes, lo que supone una prueba de la superioridad del reemplazo de células beta para restablecer el control glucémico y la independencia de las inyecciones de insulina. Sin embargo, la limitada oferta de órganos de donantes y la sustitución de los riesgos a largo plazo de la inmunosupresión por los de la diabetes limitan este enfoque. Después de que se establecieran protocolos para generar células tipo beta funcionales a partir de células madre, se preveía que la cura de la diabetes tipo 1 era inminente, pero siguen existiendo otros obstáculos para lograr este objetivo. Yoshihara y colaboradores describieron recientemente una estrategia para abordar uno de ellos.
Para que una terapia de células beta derivadas de células madre llegue a la clínica, el protocolo de diferenciación debe ser escalable para generar de forma reproducible células funcionales tipo beta, con un número mínimo de células indefinidas o pluripotenciales para reducir el riesgo de teratomas y crecimiento excesivo de tipos celulares no deseados. Las células tipo beta deben estar bien diferenciadas para que la secreción de insulina se acople a las concentraciones de glucosa con una respuesta a la dosis similar a la obtenida con las células beta primarias. Una vez alcanzados estos objetivos, un requisito clave será un medio para trasplantar las células que las proteja del rechazo del aloinjerto y de la reaparición de la eliminación mediada por autoinmunidad.
Para evitar los riesgos de la inmunosupresión a largo plazo, esto puede abordarse de dos maneras: mediante la encapsulación de los islotes injertados dentro de un dispositivo protector que permita el intercambio de nutrientes e insulina, pero no de células inmunitarias, o mediante la manipulación genética de las células de los islotes derivadas de células madre que las haga resistentes a la destrucción inmunitaria. Existe una larga historia de fracasos en la encapsulación de islotes debido a una reacción progresiva al cuerpo extraño, en la que el injerto se encapsula y las células encapsuladas mueren. El éxito de Yoshihara y sus colegas consistió en mejorar la diabetes en un modelo de ratón con un trasplante "desnudo" de islotes humanos derivados de células madre que resisten el rechazo del xenoinjerto y aloinjerto. Lo consiguieron induciendo genéticamente la expresión de la proteína de punto de control inmunitario ligando 1 de muerte programada (PD-L1) en las células madre que diferenciaron en células tipo beta (figura 1).
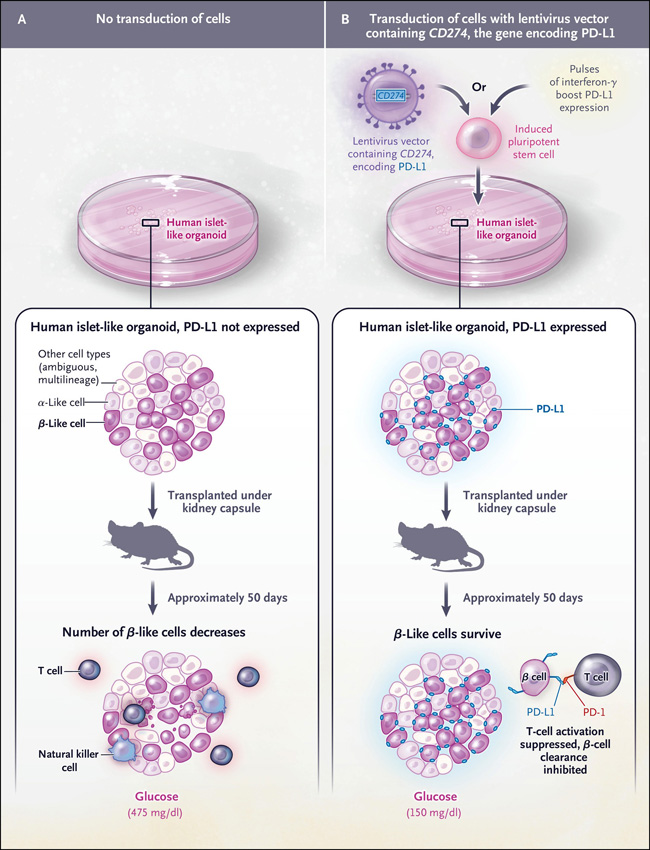
Figura 1: reversión de la diabetes mediante islotes derivados de células madre inmunotolerantes.
Yoshihara y sus colegas describieron un método para proteger los islotes pancreáticos derivados de células madre del rechazo alogénico mediado por el sistema inmunológico y de la pérdida recurrente mediada por el sistema autoinmune si se trasplantan en un paciente con diabetes de tipo 1. Después de la diferenciación a partir de una línea de células madre pluripotenciales humanas inducidas, los organoides similares a islotes humanos se expusieron a pulsos intermitentes de interferón-γ que indujeron epigenéticamente una alta expresión de la proteína de punto de control inmunitario ligando 1 de muerte programada (PD-L1), que a su vez suprimió la eliminación inmunomediada por el xenoinjerto y el aloinjerto de las células de los islotes después del trasplante en ratones.
PD-L1 se expresa en respuesta a la inflamación y se localiza en las membranas celulares, donde se une a la molécula de muerte celular programada 1(PD-1) en las células T y suprime su activación, inhibiendo la eliminación de las células viables del huésped. Las células cancerosas también expresan PD-L1 y evaden la vigilancia inmunitaria, una adaptación que aprovecha con éxito la inmunoterapia con anticuerpos PD-L1. La diabetes tipo 1 se desarrolla en un subconjunto de receptores de la terapia con anticuerpos PD-L1, un hallazgo consistente con el papel de PD-L1 en la protección contra la autoinmunidad de las células beta. Además, la inmunoterapia anti PD-1 puede provocar el rechazo de trasplantes renales alogénicos al restaurar la función citotóxica de las células T, apoyando el papel de PD-L1 en la preservación de la supervivencia y función del aloinjerto. Yoshihara y colaboradores aumentaron la expresión de PD-L1 en las células madre utilizadas para generar células tipo beta mediante el uso de un lentivirus. Tras demostrar la protección relativa de las células islote derivadas de células madre trasplantadas contra el xenografo, repitieron estos estudios luego de aumentar la expresión de PD-L1 mediante la exposición repetitiva de los islotes a pulsos de interferón-γ in vitro, una estrategia que evita el potencial oncogénico que puede implicar la mutagénesis insercional. Aunque la introducción de PD-L1 para proteger a las células de la eliminación inmunitaria es un enfoque razonable, debido a que las células beta del páncreas de los pacientes con diabetes tipo 1 tienen altos niveles de expresión de PD-L1, esta estrategia por sí sola puede ser insuficiente para evitar la reaparición de la eliminación autoinmune de células beta en humanos.
La diferenciación de la línea de células madre pluripotenciales utilizada por Yoshihara y sus colegas no alcanzó los niveles de función de las células beta (secreción de insulina inducida por la glucosa) reportados por otros grupos que utilizan líneas celulares diferentes, quienes lo abordaron mediante un paso adicional de diferenciación y la incorporación de células endoteliales de vena umbilical humana y células madre derivadas de tejido adiposo humano en un cultivo tridimensional, estrategias que mejoraron la función de las células beta. La comparación directa entre los islotes humanos y los derivados de células madre mostró menos células beta y un número relativamente alto de células ambiguas multilinaje en los islotes derivados de células madre. Esto explica probablemente la imposibilidad de alcanzar niveles típicos de glucosa en sangre humana de aproximadamente 100 mg por decilitro en ratones implantados con islotes derivados de células madre humanas, aunque se obtuvieron 200 mg por decilitro, un nivel de "control de diabetes" que sería inferior al nivel que puede obtenerse con las bombas de insulina actuales. Además, la regulación al alza de PD-L1 en esta población mixta de células mal caracterizadas plantea la posibilidad de que se formen teratomas con expresión de PD-L1, una preocupación que deberá abordarse en estudios toxicológicos a más largo plazo de los trasplantes.
Sin embargo, la combinación de la diferenciación más robusta obtenida por otros grupos para reducir la proporción de células indiferenciadas y lograr niveles aceptables de glucosa en sangre con este nuevo enfoque de tolerancia inmunológica tiene un potencial apasionante.
Yoshihara y colegas han dado un paso hacia el desarrollo de islotes derivados de células madre con privilegios inmunes como una posible terapia celular para la diabetes. Si este enfoque logrará una protección sostenida contra la autoinmunidad o sin riesgo de formación de teratomas está por verse. Por lo tanto, es importante que, junto a este enfoque, se sigan investigando estrategias alternativas, como la mejora de la protección inmunitaria en células más caracterizadas y nuevas estrategias de encapsulación. Se están investigando enfoques alternativos para inducir una tolerancia inmunitaria específica a las células beta alogénicas. Es a través de un esfuerzo múltiple que encontraremos una estrategia que haga realidad el sueño de los de los pacientes con diabetes tipo 1: lograr la independencia a la insulina.
Fuente bibliográfica
Supplying Insulin while Evading Immunity
Peter C. Butler, M.D.
From the Larry L. Hillblom Islet Research Center, David Geffen School of Medicine, University of California, Los Angeles, Los Angeles.
N Engl J Med 2021; 384:967-969







