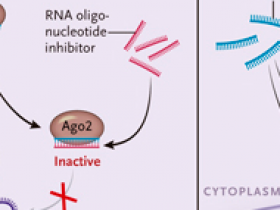
Potenciando la seguridad de la edición genética
La técnica de edición génica CRISPR-Cas se está convirtiendo en una prometedora terapia para combatir enfermedades. Sin embargo, los mecanismos enzimáticos de CRISPR-Cas pueden producir modificaciones genéticas no deseadas o efectos secundarios peligrosos. Moléculas similares a fármacos que pueden inactivar las enzimas CRISPR-Cas podrían ayudar a facilitar un desarrollo terapéutico más seguro. Basándose en la necesidad de guiar el ARN y la interacción del ADN diana por las enzimas Cas, recientemente se diseñaron pequeños inhibidores de Cas9 como oligonucleótidos capaces de unirese a la secuencia guía del ARN CRISPR o bien a los oligonucleótidos de ADN con el que el complejo interacciona. El acoplamiento resulta en una alta afinidad de unión e inhibición eficiente de la actividad de clivaje del ADN por parte de Cas9. Estos hallazgos proporcionan una plataforma para el diseño racional de inhibidores de la enzima CRISPR-Cas, lo que debería traducirse en otras enzimas efectoras y permitir un mejor control de las aplicaciones basadas en la edición génica.
Antioligonucleótidos
Las medicinas genéticas basadas en el ARN, tanto en desarrollo como en uso clínico, son terapias altamente selectivas que reconocen su blanco de secuencias de ADN o ARN mediante el apareamiento de bases. Estos medicamentos incluyen CRISPR-Cas9 (repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas- endonucleasa Cas9), una técnica experimental que utiliza oligonucleótidos de ARN para guiar a la enzima Cas9 hacia la secuencia de ADN diana, y oligonucleótidos antisentido, que son oligonucleótidos de una sola cadena y que suprimen los niveles de ARN mensajero (ARNm) o alteran su empalme. Otra clase de medicinas de ARN consiste en moléculas de doble cadena conocidas como ARN interferentes cortos (siRNAs, por sus siglas en inglés). Después de que los siRNAs son incrustados en un complejo citosólico y una de las hebras (la hebra de "sentido") es abierta, dejando expuesta la hebra de antisentido (o guía), se dirigen a sus mRNAs cognados para su degradación por la enzima Argonauta 2 (Ago2, también un componente del complejo).
Debido a que los siRNAs pueden inhibir de forma duradera sus objetivos, una preocupación importante acerca de los medicamentos dirigidos a los genes es la posibilidad de efectos fuera de objetivo. Por ejemplo, el siRNA unido a la enzima Ago2 puede dividir los mRNAs objetivo durante más de 6 meses después de una dosis subcutánea de oligonucleótido. Tal durabilidad destaca la preocupación acerca de los efectos fuera del objetivo: ¿qué pasa si se desarrolla un evento adverso grave, como resultado de un efecto fuera del objetivo, meses después de la dosis inicial? Para abordar este problema, investigadores han desarrollado un antioligonucleótido "Reversir" de una sola cadena que se dirige específica y eficazmente a una cadena de guía de siRNA (antisentido) cargada con Ago2, desactivando la respuesta de interferencia del ARN y restaurando la expresión del mRNA TTR diana (que codifica la transtiretina) pocos días después de la inyección subcutánea en ratones (figura 1). De manera similar, se han utilizado oligonucleótidos anti-antisentido para revertir los efectos de un oligonucleótido antisentido que afecta al gen SMN2 en un modelo de atrofia muscular espinal en ratones. En conjunto, estos enfoques sientan las bases para contrarrestar o revertir específicamente la actividad de las terapias de ARN.
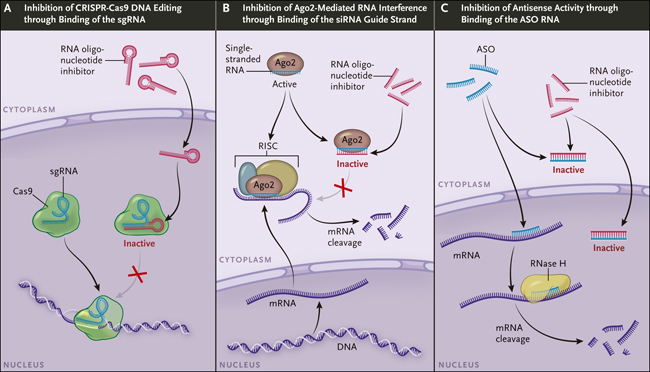
Figura 1. Regulación de la Terapéutica del ARN.
Los antioligonucleótidos reducen o inactivan edición del ADN por CRISPR-Cas9 mediante el apareamiento de bases con el ARN mono-guía (sgRNA) (panel A). Asimismo, los antioligonucleótidos pueden inhibir a los complejos silenciadores interferentes cortos (siRNA)-Ago2 RNA-inducidos (RISCs) y por lo tanto restaurar los niveles de ARN mensajero (mRNA) del gen objetivo (panel B). Los antioligonucleótidos también pueden inhibir la degradación mediada por oligonucleótidos antisentido (ASO) del ARNm por la RNasa H (panel C).
La edición genética mediada por CRISPR-Cas9 tiene el potencial de revertir permanentemente las mutaciones patológicas del ADN. Sin embargo, con la permanencia de la edición de genes viene el problema general de terminar la actividad enzimática de Cas9 después de haber completado la modificación terapéutica del ADN, con el fin de evitar la edición potencial fuera del objetivo, así como la edición dentro del objetivo en tejidos no deseados. En este sentido, Barkau y colaboradores dieron un paso al usar un enfoque antioligonucleótido para regular la edición del gen CRISPR-Cas9 en un cultivo de células humanas (DOI: 10.1089/nat.2018.0758).
CRISPR-Cas9 es una nucleasa de ribonucleoproteína (es decir, un complejo de proteína-ARN). El componente de ARN es un ARN de ingeniería genética de una sola guía (sgRNA).5 El sgRNA contiene la región guía que se empareja tanto con la secuencia de ADN diana a ser dividida como con el motivo adyacente al protoespaciador (PAM) que contiene el sitio de clivaje; también contiene cuatro bucles de vástago estructurales que están unidos por la proteína Cas9, necesarios para el correcto plegado de la proteína Cas9. Barkau y sus colegas aprovecharon estos requisitos estructurales del ARN y los trataron individualmente en combinación con oligonucleótidos complementarios, de una sola hebra, transfiriendo células renales embrionarias humanas (de la línea celular HEK293) por electroporación. Sorprendentemente, la selección de la región guía obvia del sgRNA tuvo poco efecto en la actividad general de Cas9. De la misma manera, la selección individual de varias de las estructuras de bucles de vástagos del sgRNA también fue ineficaz. Sin embargo, la vinculación de un oligonucleótido anti-PAM con un oligonucleótido que apuntaba a un loop estructural del sgRNA resultó en una reducción significativa de la actividad de Cas9 cuando se realiza el ensayo 5 días después de la electroporación. Debido a que excluye la secuencia variable de la región guía, se trata de un antioligonucleótido universal de Cas9 que, en teoría, puede inactivar todas las ribonucleoproteínas de CRISPR-Cas9.
Este enfoque simple tiene el potencial de abrir la puerta a la mejora de la seguridad de las aplicaciones clínicas de edición genética CRISPR-Cas-9. Se puede imaginar que después de optimizar la cinética de la máxima edición de genes en el objetivo en un tejido dado o en una población de células ex vivo, el antioligonucleótido sería entonces administrado para detener la actividad de Cas9 y así reducir o prevenir la edición de ADN fuera del objetivo. Del mismo modo, si el gen diana sólo necesita ser editado en un tejido, entonces la administración previa del antioligonucleótido en los tejidos no deseados evitaría la edición del ADN fuera de lugar. Esto, por supuesto, depende de que se resuelva el problema del suministro de oligonucleótidos.
En suma, Barkau y sus colegas han abierto un camino para mejorar la seguridad de la edición de genes mediante la inactivación de ribonucleoproteínas de Cas9 a través de los enfoques sencillos: los antioligonucleótidos que se unen al sgRNA CRISPR-Cas9 y lo bloquean.
Fuente bibliográfica
Controlling CRISPR-Cas9 Gene Editing
Steven F. Dowdy, Ph.D
Department of Cellular and Molecular Medicine, University of California, San Diego, School of Medicine, La Jolla.
DOI: 10.1056/NEJMcibr1906886