La química, la biología y la medicina
El Premio Nobel de Química 2022 fue otorgado a Bertozzi, Meldal y Sharpless por el desarrollo de las químicas bioortogonal y de clic. En este artículo se explica cómo estas técnicas están generando mecanismos de aplicación clínica.
El impulso para comprender mejor los sistemas vivos y la búsqueda de herramientas clínicas más efectivas han impulsado un incremento de investigación en la intersección de la química, la biología y la medicina. Un tema común ha sido la modificación de moléculas biológicamente activas para crear sondas de sistemas biológicos y producir diagnósticos y terapias. Sin embargo, la manipulación química de biomoléculas, ya sean pequeñas, ácidos nucleicos, carbohidratos, lípidos, proteínas o anticuerpos, se complica por tres aspectos. Primero, la naturaleza usa solo un puñado de grupos funcionales (por ejemplo, aminas y ácidos carboxílicos), cada uno con sus propias demandas en lo que respecta a la reactividad. En segundo lugar, una biomolécula a menudo puede contener múltiples copias de un determinado grupo funcional y, para empeorar las cosas, algunas de ellas pueden estar situadas en el área responsable de su actividad biológica. Como resultado, modificar una biomolécula en un solo sitio sin alterar su función es una tarea abrumadora. En tercer lugar, muchas biomoléculas son muy sensibles a la temperatura, disolventes y pH y, por lo tanto, solo se manipulan en condiciones biocompatibles. Históricamente, estos obstáculos intrínsecos se han combinado para hacer que la síntesis de herramientas biomoleculares efectivas sea difícil en el mejor de los casos e imposible en el peor.
El Premio Nobel de Química 2022 fue otorgado a los doctores Carolyn Bertozzi, Morten Meldal y K. Barry Sharpless por su creación de un conjunto de nuevas transformaciones químicas, "química de clic", que ha revolucionado la investigación en la interfaz de la química y la biología. Estas reacciones son rápidas, eficientes, modulares, limpias, selectivas y compatibles con condiciones acuosas. El nombre, acuñado por Sharpless, recuerda piezas de rompecabezas moleculares que se conectan entre sí (y solo entre sí) de manera simple y fácil. Meldal y Sharpless desarrollaron de forma independiente y concomitante lo que hoy se conoce como la reacción del clic canónico. En esta transformación, una azida y un alquino se someten a una reacción de cicloadición con la ayuda de un catalizador de cobre para formar un anillo de triazol, uniendo cualquier carga adherida a los miembros de este dúo molecular (figura 1A). Se puede imaginar cómo esta cicloadición de azida-alquino catalizada por cobre (CuAAC) podría usarse para sortear los desafíos antes mencionados: una biomolécula que contiene azida podría "hacer clic" fácilmente con un compañero que contenga alquino en condiciones acuosas suaves sin la formación de subproductos no deseados. Más allá de la biología química, la ligadura CuAAC ha demostrado ser indispensable en campos que van desde el desarrollo de fármacos y la química de materiales hasta la ingeniería biomédica y la nanociencia.
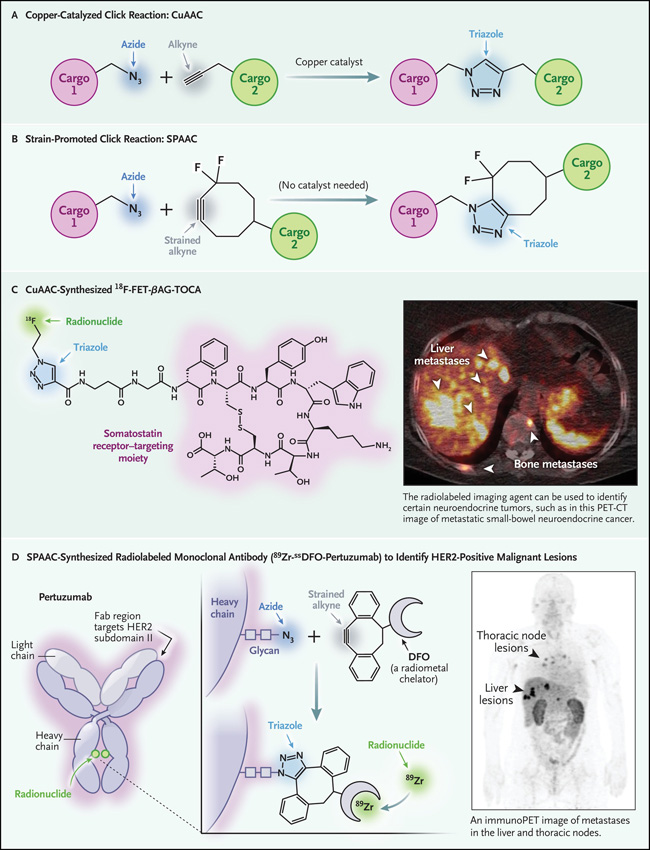
Figura 1: Cuando la química hace clic.
Tras su descubrimiento, la reacción de CuAAC fue un éxito instantáneo, pero algunas condiciones resultaron inadecuadas para la ligadura. En sistemas biológicos complejos, como los organismos vivos, es demasiado difícil reunir la azida, el alquino y el catalizador en un solo lugar. Se necesitaba una versión más simple de dos componentes de la reacción desarrollada por Sharpless y Meldal. Aquí es donde entra en juego el trabajo de Bertozzi. Su variación de la cicloadición todavía usa una azida, pero la empareja con un alquino cíclico que está cargado con un efecto resorte que los químicos llaman "tensión anular" (figura 1B). Su liberación le da a la cicloadición el impulso que necesita para continuar sin un catalizador de cobre. Esta transformación se denominó cicloadición de azida-alquino promovida por tensión (SPAAC). Como reacción del clic bioortogonal, una transformación que puede ocurrir en los sistemas biológicos sin perturbarlos, la reacción SPAAC ha permitido el uso de la química del clic en entornos biológicos previamente inaccesibles. Esto fue elegantemente demostrado por Bertozzi y sus colegas cuando trataron embriones de pez cebra vivos con azúcares modificados con azida. A medida que se desarrollaban los embriones, estos azúcares que contenían azida se incorporaban metabólicamente a los glicanos de la superficie celular en los tejidos, donde luego podían someterse a reacciones SPAAC con alquinos tensos marcados con fluoróforos para iluminar el glucoma emergente del pez cebra.
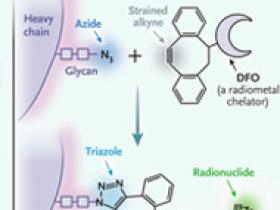
El advenimiento de la química del clic ha tenido un gran efecto en casi todas las áreas de la química. La radiofarmacéutica no es una excepción. La química del clic es una herramienta notablemente poderosa para la radioquímica: la descomposición de los radionúclidos hace que la velocidad sintética sea una prioridad, y tanto la selectividad como la compatibilidad con el agua son fundamentales porque las biomoléculas se utilizan a menudo como plataformas para radiotrazadores y radioterapéuticos. Durante los últimos 15 años, las reacciones CuAAC y SPAAC se han utilizado para crear radiofármacos etiquetados, desde nucleidos de vida corta (por ejemplo, carbono-11 y flúor-18 [18F]) para tomografía por emisión de positrones (PET) hasta isótopos vivos (lutecio-177 y actinio-225) para la terapia dirigida con radionúclidos. Algunos de estos agentes han comenzado a impactar en la clínica. En 2016, el fluoroetiltriazol-Tyr3-octreotato marcado con 18F, un agente de imagen dirigido al receptor de somatostatina que se sintetiza con la reacción CuAAC, se considera para la imagen PET de tumores neuroendocrinos (figura 1C). Más recientemente, la reacción SPAAC se utiliza para crear una variante de pertuzumab que está radiomarcada con zirconio-89 en los glicanos de cadena pesada (figura 1D). Actualmente se está realizando una prueba de esta sonda para la obtención de imágenes PET basada en anticuerpos (inmunoPET) de lesiones malignas positivas para el receptor 2 del factor de crecimiento epidérmico humano.
Este Premio Nobel marca un momento emocionante y trascendental para la química del clic. En el laboratorio, los laureados han inspirado el desarrollo de una serie de nuevas reacciones de clic bioortogonales, cada una con sus propias aplicaciones en química, biología y medicina. Es importante destacar que las herramientas basadas en química de clics han entrado cada vez más en la clínica. El camino desde el descubrimiento químico hasta la aplicación médica puede ser largo, pero la tecnología que surgió de los descubrimientos de Bertozzi, Meldal y Sharpless está claramente encaminada.
Fuente bibliográfica
Click Here for Better Chemistry
Brian M. Zeglis, Ph.D., and Jason S. Lewis, Ph.D.
Department of Chemistry, Hunter College, City University of New York (B.M.Z.), the Department of Radiology (B.M.Z., J.S.L.) and the Program in Molecular Pharmacology (J.S.L.), Memorial Sloan Kettering Cancer Center, and the Department of Radiology, Weill Cornell Medicine (B.M.Z., J.S.L.) — all in New York.
DOI: 10.1056/NEJMcibr2213596