La promesa de las vacunas de ARNm
Aunque el tiempo de producción (11 meses) de las vacunas de ARN mensajero contra la infección por SARS-CoV-2 estableció un récord, la investigación preclínica que las sustenta abarcó décadas y se vio desafiada por la falta de financiación.
La elaboración de vacunas a menudo es una tarea ingrata. En palabras del Dr. Bill Foege, uno de los mejores médicos de salud pública del mundo, "Nadie te agradece por salvarlos de la enfermedad que no sabían que iban a contraer". Sin embargo, los profesionales de esta área consideran que representan un excelente retorno de la inversión porque previenen muertes y discapacidad, especialmente cuando se administran en la infancia. Entonces, ¿por qué no tenemos vacunas para más enfermedades prevenibles? La razón es que deben ser capaces de mostrar una alta eficacia y seguridad para garantizar su uso en personas sanas, lo que hace que su desarrollo sea un proceso largo y difícil. Antes de 2020, el tiempo promedio desde la concepción de una vacuna hasta la licencia pasaban de 10 a 15 años; el tiempo más corto (para la vacuna contra las paperas) fue de 4 años. El desarrollo de una vacuna para la enfermedad por coronavirus 2019 (Covid-19) en 11 meses fue, por lo tanto, una hazaña extraordinaria y fue posible gracias a años de investigación básica en nuevas plataformas, sobre todo ARN mensajero (ARNm). Las contribuciones de Drew Weissman y Katalin Karikó, ganadores del Premio de Investigación Médica Clínica Lasker-DeBakey 2021, son particularmente notables.
Los principios detrás de las vacunas de ácido nucleico tienen sus raíces en el dogma central de Watson y Crick: que el ADN se transcribe en ARNm, que a su vez se traduce en proteínas. Hace casi tres décadas se demostró que la introducción de ADN o ARNm en una célula o en cualquier organismo vivo da como resultado la expresión de una proteína definida por la secuencia de ácido nucleico. Poco después, el concepto de vacunas de ácido nucleico se validó cuando se demostró que las proteínas expresadas a partir de ADN exógeno inducían una respuesta inmunitaria protectora. Sin embargo, la aplicación de la vacunación con ADN en el mundo real ha sido limitada, debido principalmente a preocupaciones de seguridad con respecto a la integración del ADN y luego por la escasa escalabilidad de la entrega eficiente del ADN al núcleo. Por el contrario, a pesar de ser propenso a la hidrólisis, el ARNm parecía ser más manejable porque no era necesario administrar el ácido nucleico al núcleo; es funcional en el citosol. Sin embargo, se necesitaron décadas de investigación básica realizada por Weissman y Karikó, inicialmente en sus propios laboratorios y luego tras la concesión de licencias a dos empresas de biotecnología (Moderna y BioNTech), para la realización de vacunas de ARNm. ¿Cuáles fueron las claves del éxito?
Tuvieron que superar varios obstáculos. El ARNm es reconocido por los receptores de reconocimiento de patrones del sistema inmune innato (figura 1), incluidos los miembros de la familia de receptores tipo toll (TLR3 y TLR7/8, que detectan el ARN bicatenario y el ARN monocatenario, respectivamente) y el ácido retinoico – mediante la vía de la proteína del gen I inducible (RIG-I), para inducir una respuesta inflamatoria y muerte celular (RIG-I es un receptor de reconocimiento de patrones citosólico que reconoce el ARN bicatenario corto y activa el interferón tipo I y, por lo tanto, el sistema inmunológico adaptativo). En consecuencia, la inyección de ARNm en animales provocó un shock, sugiriendo que podría haber un límite en la dosis a usarse en humanos sin generar efectos secundarios inaceptables. Para explorar formas de mitigar la inflamación, los investigadores se propusieron comprender la manera en que los receptores de reconocimiento de patrones discriminaban el ARN derivado de patógenos del auto ARN. Observaron que muchos ARN intracelulares, como los abundantes ARN ribosomales, están muy modificados y especularon que estas modificaciones podrían permitir que los auto ARN eludan el reconocimiento inmunológico. Se produjo un avance crítico cuando demostraron que la modificación del ARNm al reemplazar la uridina con pseudouridina atenuaba la activación inmune al tiempo que conservaba la capacidad de codificar proteínas. Esta modificación dio como resultado un aumento en la producción de proteínas hasta 1000 veces mayor que la del ARNm no modificado porque el ARNm modificado evade el reconocimiento de la proteína quinasa R, un sensor que reconoce el ARN y luego detiene la traducción de proteínas a través de la fosforilación y activación del factor de inicio de la traducción eIF-2α. Este ARNm modificado con pseudouridina es lo que forma la columna vertebral de las vacunas de ARNm autorizadas.
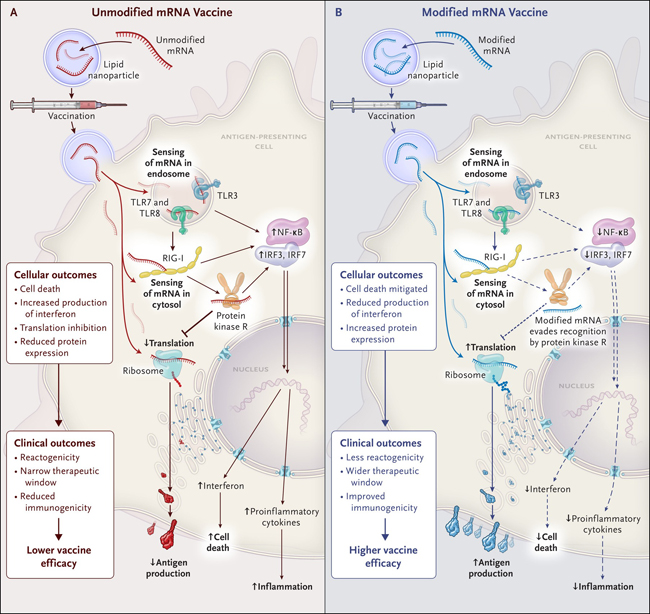
Figura 1: reconocimiento celular y consecuencias clínicas del uso de ARNm modificado y no modificado en vacunas.
Como se muestra en el Panel A, el ARN mensajero (ARNm) no modificado introducido en la célula se acopla a los receptores de reconocimiento de patrones endosómicos y citosólicos para inducir la muerte celular o una respuesta inflamatoria. Además, el reconocimiento del ARNm no modificado por la proteína quinasa R detiene la síntesis de proteínas y reduce la expresión de antígenos. Las vacunas que contienen ARNm sin modificar muestran una mayor reactogenicidad, una ventana terapéutica estrecha y una inmunogenicidad reducida. Como se muestra en el Panel B, el ARNm que se ha modificado mediante la adición de pseudouridina no se acopla a los receptores de reconocimiento de patrones intracelulares y citosólicos, y muestra una menor inflamación y muerte celular. El fracaso del ARNm modificado para activar la proteína quinasa R da como resultado una expresión de proteína continua y una fuerte inmunogenicidad. En la clínica, las vacunas que contienen ARNm modificado muestran menos reactogenicidad, una ventana terapéutica más amplia y una inmunogenicidad mejorada, en comparación con las vacunas que contienen ARNm no modificado. IRF representa al factor regulador de interferón, NF al factor nuclear, RIG-I a la proteína del gen I inducible por ácido retinoico y TLR al receptor tipo toll.
El último avance fue determinar la mejor manera de empaquetar el ARNm para protegerlo de la hidrólisis y entregarlo al citosol de la célula. Se han probado varias formulaciones en diferentes vacunas contra otros virus. En 2017, tales pruebas condujeron a una vacuna de ARNm que, cuando se encapsulaba y administraba mediante una nanopartícula lipídica, aumentaba la inmunogenicidad al tiempo que conservaba un perfil de seguridad manejable. Los estudios en animales mostraron que las nanopartículas de lípidos se dirigían a las células presentadoras de antígenos en el ganglio linfático de drenaje y también complementaban la respuesta al inducir la activación de linfocitos T auxiliares CD4 foliculares. Estos aumentan la producción de anticuerpos, el número de células plasmáticas de larga vida y el grado de respuesta de las células B maduras. Las dos vacunas de ARNm Covid-19 actualmente autorizadas utilizan formulaciones de nanopartículas lipídicas.
Se tuvo la suerte de que estos avances se hubieran completado antes de la pandemia y, por lo tanto, las empresas estaban preparadas para el éxito. Las vacunas de ARNm son seguras, eficaces y escalables; se han administrado más de mil millones de dosis, y la capacidad de escalar aún más para suministrar de 2 a 4 mil millones de dosis en 2021 y 2022 será vital en la lucha global contra Covid-19. Desafortunadamente, hasta que se logre la escala máxima, persistirán las grandes desigualdades en el acceso a estas herramientas que salvan vidas, y las vacunas de ARNm se administrarán principalmente a personas que viven en países de ingresos altos.
De manera más general, el ARNm presagia un nuevo amanecer para el campo de la vacunación y ofrece oportunidades para la protección contra otras enfermedades infecciosas, como la mejora de la vacuna contra la influenza y el desarrollo de vacunas para los grandes asesinos (malaria, VIH y tuberculosis) que se han mantenido relativamente refractarios a los enfoques convencionales. Ahora se pueden considerar condiciones como el cáncer que anteriormente eran objetivos difíciles debido a la baja probabilidad de éxito y la necesidad de una vacunación personalizada. Más allá de este proceso, ahora se han administrado miles de millones de dosis y demostrado que es seguro, allanando el camino para otras terapias de ARN, como el reemplazo de proteínas, la interferencia de ARN y edición de genes CRISPR-Cas. La revolución del ARN acaba de comenzar.
El arduo trabajo y los logros de Weissman y Karikó ejemplifican aspectos del proceso científico. Las grandes cosas surgen de los pequeños comienzos, y la tarea es larga, requiriendo tenacidad, sabiduría y visión. Aunque no hay que olvidar que muchas partes del mundo permanecen sin vacunas, los que han tenido la suerte de haberlas recibido deben agradecer su protección. Felicitaciones a estos dos científicos básicos, cuyo notable trabajo hizo posibles estas vacunas.