Estrategia celular contra la fibrosis hepática
La fibrosis es el principal determinante de la morbilidad y mortalidad en pacientes con esteatohepatitis no alcohólica (EHNA), pero no cuenta con una farmacoterapia aprobada, en parte debido a la comprensión incompleta de sus mecanismos. En un reciente estudio, se revela que la actividad de la proteína receptora Notch en los hepatocitos recapitula la gravedad de la enfermedad y la respuesta al tratamiento en pacientes con EHNA. En modelos de ratones con pérdida de función específica de Notch se observa que la fibrosis hepática asociada EHNA se encuentra atenuada, lo que demuestra la causalidad de la patología hepática inducida por obesidad. Por el contrario, la activación forzada de la fibrosis inducida por hepatocitos con actividad Notch en ratones aumenta la expresión y secreción de Osteopontina (Opn) dependiente de Sox9 desde los hepatocitos, que a su vez activan las células estrelladas hepáticas residentes. En un estudio transversal, se encontró que Opn explica la correlación positiva entre la actividad de Notch y el estadio de fibrosis en los pacientes. Además, al inhibir la vía de señalización de Notch se redujo la fibrosis en ratones alimentados con una dieta inductora de EHNA. En resumen, estos estudios demuestran el rol patológico y la accesibilidad terapéutica de la respuesta de los hepatocitos con actividad Notch en la fibrosis hepática asociada a EHNA.
Señalización vía Notch
La enfermedad del hígado graso no alcohólico es una afección compleja que implica la progresión de la esteatosis simple a la inflamación (esteatohepatitis no alcohólica [EHNA]) y luego a la fibrosis grave y al carcinoma hepatocelular, que son los principales factores de predicción de muerte en pacientes con esta enfermedad. Paralelamente al reciente aumento de la obesidad, la incidencia de hígado graso no alcohólico está aumentando. Sin embargo, en la actualidad, no existe ningún tratamiento farmacológico aprobado que se dirija específicamente a la EHNA.
Las proteínas Notch son una familia de receptores implicados en la diferenciación celular durante la embriogénesis. También han sido implicadas en el metabolismo. Por ejemplo, la activación de la proteína Notch en los hepatocitos aumenta la síntesis de triglicéridos intracelulares al estabilizar otra proteína, la diana del complejo 1 de rapamicina (mTORC1; que suele activarse mediante la señalización de insulina), lo que a su vez activa la proteína 1c de unión al elemento regulador del esterol.
Un estudio recientemente reportado por Zhu y colaboradores (DOI: 10.1126/scitranslmed.aat0344) investigó la inhibición de la señalización de Notch como estrategia terapéutica contra la fibrosis causada por la enfermedad del hígado graso no alcohólico. Aunque en circunstancias normales la señalización Notch se suprime en los hepatocitos después de la diferenciación, los autores encontraron una sobrerregulación de esta vía de señalización en los hígados de personas con enfermedad hepática grasa no alcohólica y en ratones alimentados con una dieta que induce EHNA. Es importante destacar que la regulación negativa y la ablación de la señalización de Notch en estos ratones resultaron en una mejoría de la fibrosis hepática (figura 1).
Un estudio de aleatorización mendeliana con el uso de polimorfismos de un solo nucleótido que se han asociado con un aumento de la grasa del hígado mostró que la esteatosis tiene un papel causal en la fibrosis hepática. Los resultados del estudio son consistentes con este hallazgo. Encontraron que, en un modelo de esteatosis hepática y fibrosis en ratones, la ablación de la señalización de Notch resultó en una reducción en la incidencia y gravedad tanto de la esteatosis como de la fibrosis. En particular, los autores no observaron cambios después de la inactivación de Notch en la fibrosis hepática en ratones alimentados con una dieta deficiente en metionina y colina, que causa fibrosis independiente de las calorías y el almacenamiento de lípidos. Estos datos apoyan las observaciones de que el exceso de grasa hepática es perjudicial para el hígado, que la señalización sostenida de Notch induce fibrosis hepática en presencia de acumulación de lípidos, y que la supresión de la señalización de Notch o del contenido de grasa hepática puede mejorar la fibrosis hepática.
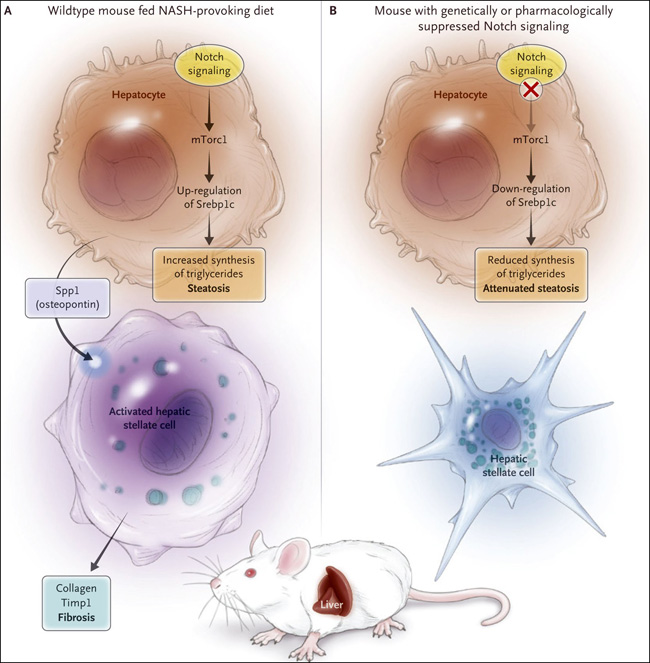
Figura 1. Señalización de Notch, esteatosis y fibrosis.
La señalización por Notch estabiliza la diana mecanicista de la proteína del complejo 1 de rapamicina (mTorc1), lo que resulta en una sobrerregulación de la proteína 1c de unión al elemento regulador de esterol (Srebp1c) y de la síntesis de triglicéridos de los hepatocitos (panel A). Zhu y colaboradores (DOI: 10.1126/scitranslmed.aat0344) evidenciaron que, en ratones, la ablación de la señalización intracelular de Notch en hepatocitos resultó en una reducción de la estabilización de mTorc1 y la consiguiente regulación negativa de Srebp1C, lo que condujo a una reducción de la síntesis de triglicéridos en hepatocitos (panel B). Además, la reducción de la producción de fosfoproteína secretada 1 (Spp1, también conocida como osteopontina) por los hepatocitos dio lugar a la regulación negativa de colágeno y del inhibidor tisular de la metaloproteasa 1 (Timp1), que contribuyen a la fibrosis, en las células estrelladas hepáticas. EHNA denota esteatohepatitis no alcohólica.
Las células madre cancerosas son los progenitores del cáncer. Tienen un papel fundamental en el desarrollo, progresión y recurrencia tumoral. La señalización por Notch promueve una mayor malignidad tumoral al contribuir al desarrollo de células madre cancerosas y a la resistencia a la quimioterapia. Sería interesante ver si la inhibición de Notch podría mejorar el pronóstico de los pacientes con carcinoma hepatocelular asociado a fibrosis o prevenir la recurrencia de la enfermedad.
Las células madre cancerosas son los progenitores del cáncer. Tienen un papel fundamental en el desarrollo, progresión y recurrencia tumoral. La señalización por Notch promueve una mayor malignidad tumoral al contribuir al desarrollo de células madre cancerosas y a la resistencia a la quimioterapia. Sería interesante ver si la inhibición de Notch podría mejorar el pronóstico de los pacientes con carcinoma hepatocelular asociado a fibrosis o prevenir la recurrencia de la enfermedad.
Otra línea de investigación está motivada por la genética de la susceptibilidad a la enfermedad del hígado graso no alcohólico. Las variaciones naturales de la secuencia genética aumentan la grasa y fibrosis hepática por medio de diferentes mecanismos.¿Podría la inactivación de Notch reducir la incidencia y la gravedad de la esteatosis y la fibrosis hepática entre personas con un trasfondo genético específico? Otra consideración es que la regulación negativa a largo plazo de Notch podría afectar el tracto biliar; se sabe que la activación de vía de señalización de Notch induce la diferenciación de colangiocitos. Tal vez un fármaco supresor de Notch que esté dirigido específicamente a los hepatocitos o la administración intermitente de dicho fármaco podría obviar este riesgo.
En conclusión, la regulación a la baja de la señalización de Notch representa una diana terapéutica candidata contra la fibrosis en pacientes con enfermedad hepática grasa no alcohólica. Se necesitan estudios para probar esta hipótesis en humanos y descifrar los mecanismos moleculares que vinculan la señalización de Notch con la fibrosis.
Fuente bibliográfica
Notch and Nonalcoholic Fatty Liver and Fibrosis
Stefano Romeo, M.D., Ph.D.
Department of Molecular and Clinical Medicine, University of Gothenburg, and the Cardiology Department, Sahlgrenska University Hospital, Gothenburg, Sweden.
DOI: 10.1056/NEJMcibr1815636