Complemento y microglía, precursores del olvido
Todos olvidamos cosas, y a veces sería mejor no hacerlo. El olvido normal ocurre con más frecuencia a medida que envejecemos, pero en el alzhéimer y otras demencias, puede ocurrir un olvido progresivo y retrógrado, que puede tener consecuencias graves y amenazantes para la vida. La mayoría asume que la formación de la memoria es un proceso activo y que el olvido refleja una combinación de defectos en la codificación de la memoria inicial, localización de memorias, o recuperación de ellas. Se piensa que la pérdida de memoria es patológica, como en las enfermedades relacionadas con la demencia. Sin embargo, estudios realizados en animales sanos indican que tanto la formación como la pérdida de memoria son procesos activos que implican el fortalecimiento y debilitamiento de las sinapsis mediante acciones dirigidas por las propias neuronas. Se sabe que el fortalecimiento de las sinapsis, dependiente de la actividad, es la base de la formación de la memoria. Y respecto al proceso contrario, un reciente estudio preclínico muestra que es el agotamiento activo de las sinapsis débiles lo que da lugar a la pérdida de memoria, al menos en el cerebro de ratones adultos.
Sinapsis débiles
En el cerebro en desarrollo, las sinapsis débiles son podadas por la microglía (células mieloides fagocíticas residentes) mediante un proceso que implica la expresión neuronal de las proteínas clásicas del complemento como la C1q y la C3, que marcan las sinapsis débiles para ser eliminadas por la microglía que expresa el receptor del complemento. En el hipocampo, donde se forman trazas de memoria, el mismo proceso de eliminación de sinapsis se ha vinculado a las enfermedades de la memoria en los adultos, lo que sugiere que la activación aberrante de esta herramienta de desarrollo en los adultos puede ser patológica. El estudio de Wang y sus colegas sugiere que el mismo proceso también media el olvido normal en animales adultos.
Para determinar si la microglía es necesaria para el olvido normal, los autores evaluaron el comportamiento de congelación inducido por el miedo en ratones condicionados por esta emoción miedo que habían sido sometidos a una ablación genética o farmacológica de la microglía. El condicionamiento de miedo contextual es un método estándar utilizado en la evaluación de la memoria a corto y largo plazo en animales; en el estudio de Wang y sus colegas, la evaluación implicó la medición del grado de comportamiento de congelación en varios puntos de tiempo después de que los roedores recibieran choques leves en los pies con un aparato de entrenamiento.
Los investigadores encontraron que los ratones normales reintroducidos en el aparato después de un intervalo comparativamente largo (35 días) después del entrenamiento se congelaron durante un período más corto que los ratones reintroducidos en el dispositivo después de cinco días. Esta diferencia refleja una cantidad normal de olvido durante el intervalo más largo. Sin embargo, los ratones sin microglía tuvieron una duración de congelación de 35 días similar a la de los ratones sin ablación de microglía probados a los cinco días después del adiestramiento, lo que demuestra una prevención del olvido en los ratones sin microglía. Esos datos indican que es fundamental para el proceso de olvido después del condicionamiento de miedo contextual. Sin embargo, dado que la activación neuronal subyace al aprendizaje y olvido, es importante en este campo de investigación determinar si el olvido mediado por la microglía depende de la actividad neuronal.
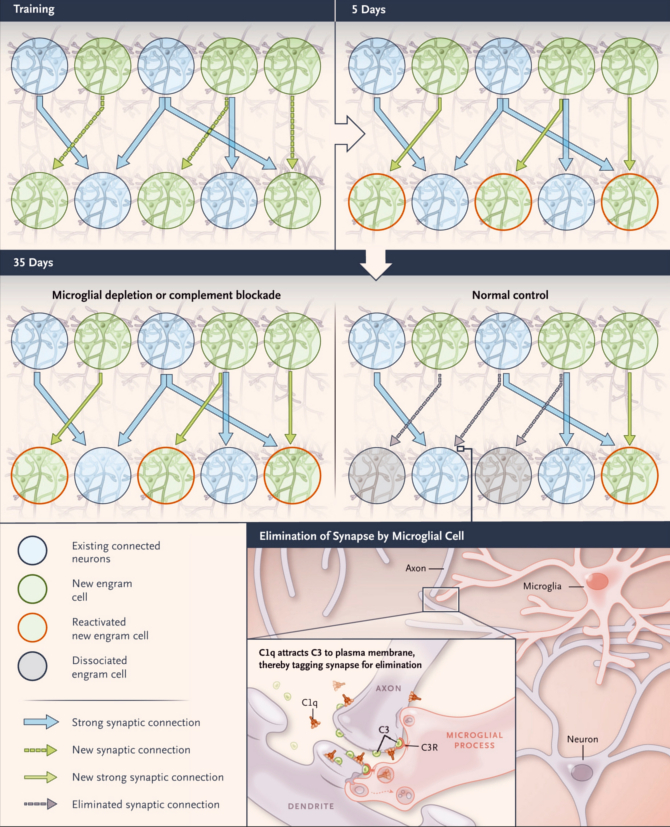
Figura 1. Activación microglial, de complemento y celular en la formación de la memoria, el recuerdo y e olvido.
El agotamiento microglial o la inhibición de la activación del complemento afecta a la conectividad sináptica y a la reactivación de las células engramas durante la formación de la memoria y el olvido en el hipocampo. Las neuronas conectadas existentes (círculos azules) están presentes en redes consolidadas (flechas azules). Durante el condicionamiento contextual del miedo, un pequeño número de nuevas células engramas (círculos verdes) son reclutadas en nuevas redes (flechas verdes punteadas), que se consolidan (flechas verdes sólidas). La reactivación de estas nuevas células engramas (círculos verdes con bordes naranjas) se produce cuando los animales reencuentran las señales que desencadenaron el miedo. El olvido implica la interrupción de estas nuevas conexiones sinápticas (flechas grises discontinuas) con la desconexión de sus células engramas (círculos grises), un proceso que puede invertirse con la ablación de la microglía o la inhibición del complemento. C3R denota receptor C3.
Las células de engramas -inicialmente controvertidas como entidad y por ser importantes para el establecimiento de la memoria- son una población de neuronas que se activan durante el aprendizaje y requieren reactivación para el recuerdo de la memoria. De hecho, son las conexiones sinápticas entre las células engramas, y no las células mismas, las que constituyen los sitios físicos donde se almacenan los recuerdos (Nature. 2009 Dec 17;462(7275):920-4). Los marcadores de la actividad neuronal, incluyendo los c-fos, son herramientas poderosas para etiquetar las células de engramas en base a su historial de actividad neuronal. Usando ratones transgénicos en los que el engrama neuronal reactivado está permanentemente marcado por la inducción de expresión c-fos, Wang y sus colegas mostraron que la tasa de actividad neuronal dentro del hipocampo se correlacionó positivamente con el comportamiento de congelación y que este se incrementa con el agotamiento microglial.
Los niveles de proteínas sinápticas dentro de la microglía también eran mayores a los 35 que a los cinco días después del condicionamiento de miedo contextual en ratones normales, lo que sugiere que la eliminación de la sinapsis subyace al olvido normal. La administración de minociclina, un agente antibiótico que amortigua la activación microglial, redujo la fagocitosis de material sináptico y aminoró el olvido. Los hallazgos de estos experimentos apoyan que la eliminación de sinapsis mediada por microglía normalmente subyace en el acto de olvidar, al menos para ciertos estímulos nocivos.
¿El complemento media este proceso? Parece ser así. Wang y sus colegas mostraron que la proteína del complemento C1q se colocaliza con las proteínas sinápticas dentro de la microglía durante el olvido normal. Luego inyectaron un virus diseñado que expresa CD55, un inhibidor de la activación del complemento, en el cerebro de los ratones. Los animales mostraron un aumento de las conductas de congelación 35 días después del condicionamiento de miedo contextual y tuvieron mayores niveles de activación de células engramas y menores niveles de proteínas sinápticas dentro de la microglía. Experimentos posteriores mostraron que la supresión de la actividad de las células engramas se asociaba con un aumento del olvido, que podía ser abolido por la ablación microglía o la expresión de CD55 (figura 1).
Estos experimentos indican que el acto de olvidar es exactamente eso: un proceso activo en el que las sinapsis más débiles se marcan para ser eliminadas; un proceso que se produce a lo largo de la vida para fortalecer las redes y retener parsimoniosamente los recuerdos. El descubrimiento de que el complemento y la microglía contribuyen al olvido normal sugiere que el olvido patológico, como ocurre en los pacientes con demencias, o el recuerdo patológico, como puede ocurrir en los pacientes con trastorno de estrés postraumático, puede deberse a defectos en el mantenimiento de las redes apropiadas. Los nuevos tratamientos que puedan regular la eliminación de sinapsis mediada por la microglía y el complemento podrían algún día prevenir o promover la pérdida de memoria, dependiendo de la necesidad clínica.
Fuente bibliográfica
On Complement, Memory, and Microglia
Robyn S. Klein, M.D., Ph.D.
Departments of Medicine, Pathology and Immunology, and Neurosciences, Washington University School of Medicine, St. Louis.
DOI: 10.1056/NEJMcibr2002480