Atención oncológica de precisión
El análisis genómico del ADN y tejido tumoral es un componente cada vez más importante en el cáncer; dichas pruebas se pueden usar para evaluar su riesgo, informar el pronóstico y detectar la recurrencia de la enfermedad después de completar el tratamiento. La aplicación más importante ha sido guiar la selección de la terapia mediante pruebas de diagnóstico validadas, en particular las que son complementarias.
La Administración de Alimentos y Medicamentos (FDA) define una prueba de diagnóstico complementario como un dispositivo in vitro esencial para el uso seguro y eficaz de un producto terapéutico. Este enfoque se utilizó por primera vez en 1998, cuando trastuzumab se combinó con una prueba inmunohistoquímica que medía la expresión del receptor 2 del factor de crecimiento epidérmico humano (HER2, también conocido como ERBB2) en tejido de cáncer de mama para determinar la probabilidad de que un tumor respondiera al tratamiento. Desde entonces, las terapias dirigidas molecularmente y pruebas diagnósticas complementarias se han expandido rápidamente.
Hasta junio de 2022, la FDA autorizó o aprobó pruebas complementarias de diagnóstico para unos 27 biomarcadores moleculares para más de 40 medicamentos aprobados en el tratamiento de 16 tipos de tumores. Cinco alteraciones moleculares (alta inestabilidad de microsatélites, alta carga de mutaciones tumorales, fusiones NTRK, mutaciones BRAF V600E y fusiones RET) se han relacionado con tratamientos cuyo uso está aprobado independientemente del tipo histológico del tumor o el sitio de origen.
La secuenciación de próxima generación (NGS), que revela el estado mutacional de cientos de genes en una sola prueba, son particularmente útiles para identificar diversas alteraciones genómicas en tumores que tienen el mismo diagnóstico histológico. Por ejemplo, las modificaciones en hasta una docena de genes en tumores de cáncer de pulmón de células no pequeñas (NSCLC, por sus siglas en inglés) se han relacionado con tratamientos aprobados por la FDA. La NGS está ampliamente disponibles en laboratorios comerciales y hospitalarios, y la FDA ha aprobado tres para el perfil molecular del tumor. En 2018, los Centros de Servicios de Medicare y Medicaid finalizaron una determinación de cobertura nacional para el perfil de tumores NGS, concluyendo que esta es razonable y necesaria en el cáncer avanzado cuando ha sido aprobada como diagnóstico complementario y se realiza en un laboratorio certificado bajo los estándares establecidos.
Las sociedades profesionales médicas han jugado un papel importante en la orientación del uso apropiado de las pruebas genómicas de tumores. Recientemente, la Sociedad Europea de Oncología Médica publicó recomendaciones sobre su uso clínico en pacientes con tumores metastásicos, y la Sociedad Estadounidense de Oncología Clínica (ASCO) recomendó que se realicen pruebas de panel multigénico en pacientes con tumores sólidos avanzados siempre que haya más de un biomarcador genómico relacionado con una terapia aprobada. Las organizaciones de pacientes han informado a sus integrantes sobre las pruebas genómicas basadas en la evidencia y las han defendido, y la información está fácilmente disponible en el Instituto Nacional del Cáncer (NCI), la Sociedad Estadounidense del Cáncer, la ASCO y en muchos grupos centrados en enfermedades.
Sin embargo, encuestas médicas y datos de registros de salud electrónicos (EHR, por sus siglas en inglés) indican una subutilización de las pruebas genómicas de tumores. Por ejemplo, un reciente informe con casi 38.000 pacientes con NSCLC en etapa IV diagnosticados entre 2010 y 2018 reveló que solo el 22% tenía resultados de enálisis moleculares en su historial médico y solo el 3% recibió tratamiento con terapia dirigida, aunque las pautas durante este período recomendaban que todos ellos se sometieran a ensayos para detectar alteraciones tumorales de EGFR, ALK y ROS1. Estos hallazgos coincidieron con otros estudios realizados en los Estados Unidos e internacionalmente que documentaban tasas de pruebas moleculares para NSCLC tan bajas como 20%, según la región geográfica, el entorno de práctica, el período en el que se realizó el estudio y las recomendaciones predominantes para las pruebas moleculares en ese momento.
Una encuesta de 2017 realizada por el NCI identificó varios factores a nivel de proveedor y organización que pueden contribuir a la subestimación. Los oncólogos mencionaron la dificultad para obtener suficiente tejido para el análisis, tiempo insuficiente para ordenar o revisar las pruebas y la falta de personal experto como razones para no ordenar las pruebas de NGS (con menos frecuencia). Estos factores fueron citados con mayor frecuencia por los oncólogos de comunidades rurales o en práctica. Cuando se sí indicaron las pruebas, se usaron con mayor frecuencia para seleccionar una terapia aprobada por la FDA o determinar la elegibilidad para ensayos clínicos. También se encontró que oncólogos con capacitación en genómica o acceso a una junta de tumores moleculares tenían más probabilidades que otros de usar pruebas de NGS.
¿Qué explica la aparente brecha entre la disponibilidad de pruebas genómicas de tumores y su utilización? Se han identificado muchos factores que, considerados en conjunto, sugieren esfuerzos poco coordinados para implementar la atención oncológica de precisión. Los elementos necesarios del flujo de trabajo de la medicina de precisión del cáncer incluyen el análisis genómico integral de los tumores, la interpretación de los resultados de las pruebas genómicas por parte de personal experto, la toma de decisiones compartida con los pacientes sobre la probabilidad de que los resultados de las pruebas identifiquen tratamientos efectivos y el empleo de servicios administrativos para ayudar a los pacientes a obtener acceso a terapias que se identifican como posibles opciones de tratamiento (ver tabla). Cada uno de estos procesos involucra múltiples componentes que deben completarse de manera eficiente para que la atención se brinde dentro de un marco de tiempo aceptable. Dichos componentes pueden incluir la identificación o adquisición de especímenes tumorales adecuados para el análisis genómico y el manejo de las incertidumbres que rodean la elegibilidad para ensayos clínicos o el reembolso de tratamientos no aprobados, cuestiones que pueden ser particularmente desafiantes para los pacientes que carecen de los recursos para viajar a los sitios de ensayos clínicos o no tienen seguro o tienen uno inadecuado para cubrir los costos del tratamiento.
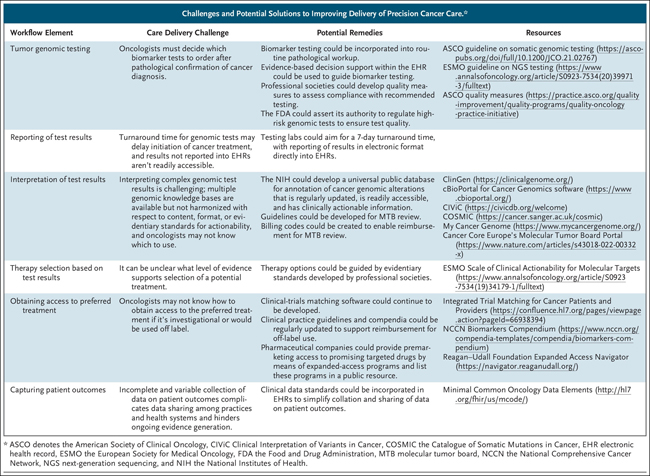
La evidencia de las prácticas comunitarias sugiere que la implementación de flujos de trabajo que activen automáticamente la NGS para pacientes con tumores sólidos avanzados, hagan uso de esquemas de tumores moleculares para interpretar los resultados y brinden asistencia administrativa para la comparación de ensayos clínicos y la obtención de autorización previa son clave para el éxito de la medicina de precisión. La creación de herramientas en EHR que evalúen el desempeño de una práctica en comparación con las pautas establecidas para las pruebas genómicas de tumores también es esencial a la hora de identificar brechas en la atención práctica. Capturar los resultados de los pacientes utilizando elementos de datos comunes y estructurados permitirá el intercambio de datos para avanzar en el conocimiento sobre la mejor manera de usar medicamentos de precisión contra el cáncer.
Los ensayos aleatorios prospectivos, los metanálisis y datos de registros respaldan el uso de pruebas genómicas tumorales integrales para identificar terapias recomendadas y aprobadas por la FDA. Pero se necesita más evidencia que respalde su aplicación fuera de los ensayos clínicos para identificar posibles tratamientos en pacientes que han agotado sus terapias, ya que pocos obtienen beneficios clínicos significativos de estos tratamientos, y con perjuicio financiero. Sin embargo, las pruebas genómicas tumorales son apropiadas para establecer opciones de ensayos clínicos para pacientes con cáncer avanzado. Estudios como el Molecular Analysis for Therapy Choice del NCI y el Targeted Agent and Profiling Utilization Registry (TAPUR) de la ASCO muestran que se pueden establecer esquemas eficaces utilizando perfiles genómicos, incluso en la enfermedad muy avanzada. En el TAPUR, alrededor de dos tercios de los pacientes evaluados fueron asignados a un tratamiento correspondiente a una alteración genómica en su tumor, con mutaciones en BRCA1 o BRCA2, CDKN2A y ERBB2 o ERBB3 cada uno, detectándose en el 10 al 15% de ellos con tumores sólidos avanzados. Entre las 24 cohortes del estudio (definidas según el tipo de tumor, la alteración genómica y el tratamiento), hubo una señal positiva de actividad del fármaco en 16, con tasas de control de la enfermedad entre el 35% y el 70%. Con el tiempo, los nuevos análisis moleculares que puedan proporcionar información sobre el epigenoma tumoral, el transcriptoma, el proteoma circulante y el microbioma intestinal podrían complementar las pruebas genómicas tumorales y refinar aún más la selección de terapias para los pacientes.
Garantizar el despliegue equitativo y eficiente de la medicina de precisión es un desafío global que requiere el acceso de los pacientes a pruebas moleculares validadas, un entorno regulatorio y de reembolso consistente, y de esfuerzos concertados. Poner estas piezas en su lugar no solo cerraría la brecha de las pruebas genómicas en la atención del cáncer, sino que podría transformar los resultados para muchos pacientes con cáncer.
Fuente bibliográfica
Closing the Gap in Cancer Genomic Testing
Richard L. Schilsky, M.D., and Dan L. Longo, M.D.
University of Chicago, Chicago (R.L.S.).
N Engl J Med 2022; 387:2107-2110







