PSA supera a la resonancia magnética en el cribado del cáncer de próstata
La prueba inicial de antígeno prostático específico es más efectiva y rentable que la resonancia magnética biparamétrica, incluso si esta última fuera gratuita.
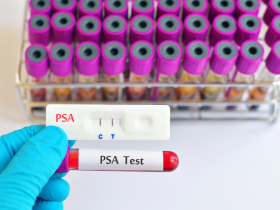
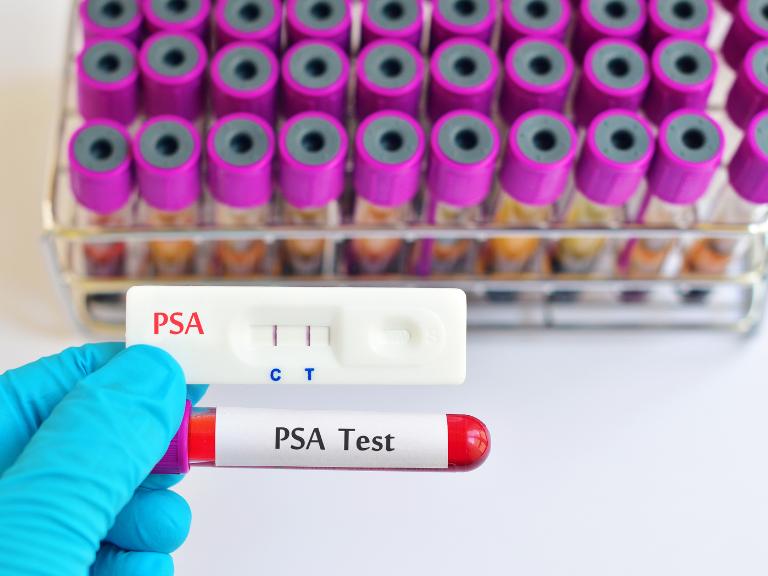
La detección estándar del cáncer de próstata empieza con pruebas de antígeno prostático específico (PSA), seguidas de imágenes por resonancia magnética multiparamétrica (mpMRI) en caso de niveles elevados de PSA. Como alternativa de primera línea, se ha propuesto el cribado mediante resonancia magnética biparamétrica (bpMRI).
El equipo de investigadores liderado por Roman Gulati, del Centro Oncológico Fred Hutchinson en EE. UU., evaluó la efectividad comparativa y la rentabilidad de la bpMRI de primera línea versus la detección basada en PSA.
Se emplearon datos de 1.000 hombres de 55 a 69 años, quienes se sometieron a una detección bienal. El cribado se llevó a cabo utilizando la prueba de PSA de primera línea (umbral de prueba positiva de 4 µg/L) con o sin mpMRI, o bpMRI como primera opción (umbral de prueba positiva PI-RADS: 3 a 5 o 4 a 5), seguida de biopsia guiada por resonancia magnética o por resonancia magnética más ecografía transrectal. El seguimiento se realizó hasta los 100 años.
La efectividad se evaluó considerando los sobrediagnósticos y las vidas salvadas, y la rentabilidad a través de los costos divididos por los años de vida.
Tras el análisis, se determinó que la prueba inicial de PSA sigue siendo más efectiva y rentable, incluso si la bpMRI fuera gratuita, debido a una menor incidencia de falsos positivos y sobrediagnósticos. Los hombres con la patología de bajo riesgo fueron sometidos a seguimiento mediante vigilancia activa o pruebas de detección cada cuatro años.
En conclusión, la prueba de PSA de primera línea seguida de mpMRI es más efectiva y rentable que la bpMRI para el cribado del cáncer de próstata.
Fuente bibliográfica
Lifetime Health and Economic Outcomes of Biparametric Magnetic Resonance Imaging as First-Line Screening for Prostate Cancer: A Decision Model Analysis
Gulati R, et al. Fred Hutchinson Cancer Center, Seattle, Washington
DOI: 10.7326/M23-1504