Semillas amiloides en muestras hormonales
En la angiopatía amiloide cerebral (AAC) y la enfermedad de Alzheimer (EA), los agregados insolubles de un péptido conocido como amiloide-β (Aβ) se acumulan progresivamente en los espacios entre células, formando depósitos amiloides. En la EA, estos agregados se encuentran entre neuronas, mientras que en la AAC, una afección relacionada pero no siempre coexistente, se encuentran en las paredes de los vasos sanguíneos cerebrales. Se cree que los agregados de Aβ son los primeros impulsores de los procesos patológicos de la AAC y la EA que culminan en la neurodegeneración. En 2015, investigadores reportaron pruebas sobre patología temprana en los cerebros de algunas personas con deficiencia de crecimiento que habían sido tratadas con hormona de crecimiento humano (DOI: 10.1038/nature15369). Este hallazgo planteó la posibilidad de que la patología pudiera ser transmisible entre humanos bajo ciertas condiciones a través de derivados contaminados del tejido cerebral. Un reciente estudio provee más apoyo a esta hipótesis.
Viales contaminados
De 1958 a 1985, aproximadamente 30.000 niños con déficit de crecimiento fueron tratados con la hormona de crecimiento derivada de cadáveres (c-hGH, por sus siglas en inglés) en todo el mundo. En 1985, se descubrió que tres receptores habían desarrollado la enfermedad de Creutzfeldt-Jakob (ECJ), que es mortal. Esta patología pertenece a un grupo de enfermedades conocidas como encefalopatías espongiformes transmisibles, que se caracterizan por un daño cerebral progresivo e irreversible resultante de la acumulación de una forma mal plegada de una proteína priónica. Estas proteínas priónicas anormales pueden hacer que las proteínas priónicas normales se plieguen mal y, por lo tanto, propaguen la enfermedad. Dadas las pruebas de que la c-hGH contaminada había causado la ECJ, este tipo de tratamiento se interrumpió rápidamente y la hormona de crecimiento humano recombinante sintética (rhGH) se convirtió en el estándar de atención.
La EA no es una enfermedad priónica clásica, pero comparte características con este tipo de trastorno. Los péptidos Aβ mal plegados y las proteínas tau, que son tóxicas para las neuronas, están presentes en el cerebro como componentes clave de la EA. La inoculación de cantidades diminutas de "semillas" mal plegadas aisladas del cerebro de personas con EA puede inducir la acumulación de depósitos de Aβ (llamadas placas de Aβ) en primates no humanos. Mientras que extractos cerebrales de personas o ratones que desarrollan placas de Aβ también pueden causar la acumulación acelerada de placas cuando se administran a ratones genéticamente modificados.
El hallazgo en 2015 de las placas de Aβ y la AAC en los cerebros de siete de los ocho receptores de la terapia de c-hGH que habían fallecido de la enfermedad de Creutzfeldt-Jakob apoyó además la idea de que la patología por la acumulación de Aβ puede transmitirse a través de un mecanismo tipo prión (figura 1). La patología rara vez se encuentra en adultos jóvenes sin factores de riesgo genéticos para la EA o AAC, por lo que los hallazgos sugieren que la c-hGH utilizada para tratar a los pacientes podría haber sido contaminada con Aβ además de proteínas priónicas mal plegadas.
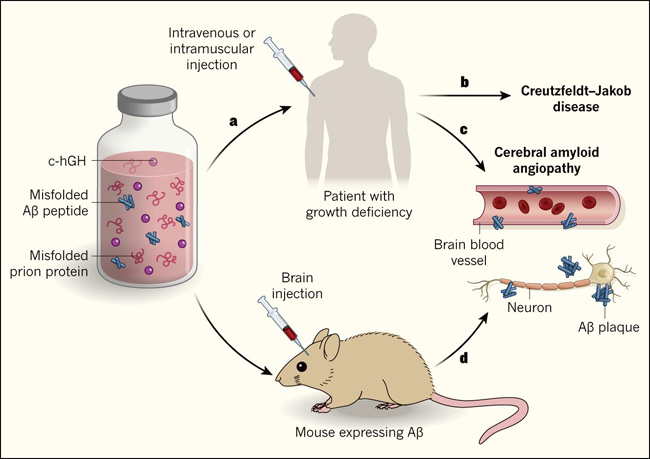
Figura. 1 Transmisión de una patología tipo priónica inducida por tratamiento.
a, De 1958 a 1985, la hormona de crecimiento humana derivada de cadáveres (c-hGH) se utilizó para tratar la deficiencia de crecimiento. b, Algunos lotes fueron contaminados con proteínas priónicas mal plegadas de personas con la enfermedad de Creutzfeldt-Jakob (CJD) y causó que los pacientes tratados desarrollaran CJD. c, Curiosamente, algunos de estos pacientes también presentaban signos tempranos de angiopatía amiloide cerebral (AAC), una afección que frecuentemente coexiste con la enfermedad de Alzheimer, y con la presencia de agregados peptídicos (placas) amiloides-β (Aβ) entre las neuronas. Esto sugirió que los viales de c-hGH también estaban contaminados con péptidos mal plegados de Aβ (semillas Aβ), el principal componente de los depósitos cerebrales patológicos que caracterizan la enfermedad de Alzheimer y la AAC. Purro y cols. (DOI: 10.1038/s41586-018-0790-y) reportaron que algunas de las muestras de c-hGH que aún están almacenadas contienen Aβ d, Los autores muestran que la inyección de materiales de c-hGH que contienen Aβ, en el cerebro de ratones que expresan Aβ, conduce a la acumulación de este mismo péptido especialmente en los vasos sanguíneos del cerebro. Estos resultados demuestran que las semillas de Aβ conservan su capacidad patológica durante mucho tiempo y que pueden ser transmitidas a través de procedimientos médicos.
Para proporcionar evidencia más directa de que los depósitos de Aβ encontrados en estas personas eran el resultado de la contaminación de semillas de Aβ, Purro y cols. (DOI: 10.1038/s41586-018-0790-y) probaron primero si Aβ estaba presente en viales de c-hGH de lotes que habían sido usados para tratar a pacientes y que habían sido almacenados desde la década de 1980. Para obtener c-hGH, las glándulas pituitarias de miles de donantes habían sido agrupadas y mezcladas, y la hormona había sido extraída químicamente usando varios métodos de preparación. Los pacientes recibieron c-hGH de múltiples lotes. Sin embargo, todos los que fueron tratados en el Reino Unido y desarrollaron CJD -38 personas para el año 2000- recibieron inyecciones de lotes preparados mediante el procedimiento Wilhelmi modificado por Hartree (HWP).
Purro y sus colegas detectaron Aβ en todas las muestras de c-hGH preparadas con dicho método, pero no en aquellas preparadas con cualquiera de los otros tres procedimientos. La cromatografía de exclusión por tamaño, una técnica de separación utilizada en todas las preparaciones que no son HWP, podría haber reducido la contaminación por péptidos. Los autores posteriormente demostraron que las preparaciones HWP de c-hGH poseen la capacidad de siembra de Aβ inyectándolas en ratones genéticamente modificados para expresar versiones humanas de Aβ (figura 1). Los ratones inoculados con c-hGH preparado con HWP desarrollaron notablemente más placas y AAC que aquellos inoculados con rhGH sintético.
Por lo tanto, estos resultados proporcionan una fuerte evidencia de que la patología previamente reportada en personas que murieron de CJD después de recibir c-hGH1 fue de hecho causada por su tratamiento. Los datos también corroboran estudios previos en ratones genéticamente modificados que demuestran que el Aβmal plegado puede comportarse de forma similar a un prión. Los estudios futuros deben investigar la cantidad de Aβ que estos pacientes recibieron durante el curso del tratamiento, para tratar de determinar el umbral de concentración de Aβ mal plegado necesario para transmitir la formación de placas o la AAC.
Fuente bibliográfica
Amyloid-β ‘seeds’ in old vials of growth hormone
Tien-Phat V. Huynh & David M. Holtzman
Department of Neurology, Washington University in St. Louis, St Louis, Missouri 63110, USA.
DOI: 10.1038/d41586-018-07604-6