Proteínas creadas con IA para neutralizar venenos de serpientes
El diseño de moléculas mediante deep learning ofrece un enfoque innovador y potencialmente eficaz para combatir toxinas de mordeduras, demostrado en modelos in vitro e in vivo, impulsando avances en el manejo del envenenamiento a nivel mundial.
La mordedura de serpiente con envenenamiento es una enfermedad tropical desatendida que causa mortalidad y morbilidad significativas, especialmente en regiones de África subsahariana, Asia y América Latina. El tratamiento principal consiste en la administración parenteral de antivenenos, que son inmunoglobulinas o fragmentos purificados del plasma sanguíneo de animales inmunizados con venenos de serpiente.
Aunque los antivenenos son eficaces para neutralizar los efectos sistémicos potencialmente mortales, pueden causar efectos adversos, tienen una eficacia limitada contra toxinas poco inmunogénicas y requieren administración en centros de atención médica. Por lo tanto, existe un creciente interés en enfoques innovadores para el tratamiento del envenenamiento por mordedura de serpiente, incluido el uso de anticuerpos recombinantes humanos, inhibidores sintéticos de toxinas o combinaciones de anticuerpos e inhibidores.
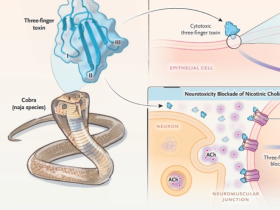
Un estudio reciente liderado por la Dra. Susana Vázquez Torres, de la Universidad de Washington, EE. UU., investigó el uso de un método computacional de deep learning para diseñar nuevas proteínas capaces de neutralizar las toxinas del veneno de serpiente, específicamente las de la familia de "tres dedos" presentes en los venenos de serpientes de la familia Elapidae.
Los investigadores utilizaron el potente método computacional de deep learning RoseTTAFold (RFdiffusion) para diseñar proteínas novedosas con secuencias y estructuras no correspondientes a ninguna molécula conocida. Seleccionaron como diana toxinas potentes de la familia de "tres dedos", que son neurotoxinas que bloquean los receptores colinérgicos nicotínicos en las fibras musculares, causando bloqueo neuromuscular y parálisis, o citotoxinas que inducen daño tisular. Se diseñaron genes sintéticos que codifican estas proteínas inhibidoras y, posteriormente, se optimizaron los inhibidores con mayor afinidad de unión a las toxinas mediante cribado iterativo. Las proteínas inhibidoras se expresaron en un sistema bacteriano y se analizaron mediante cristalografía de rayos X para determinar sus estructuras.
Los análisis cristalográficos revelaron que las estructuras de los inhibidores candidatos principales, cuando se combinaban con las toxinas, eran similares a las de los modelos diseñados mediante el modelado computacional. Las pruebas in vitro mostraron que los inhibidores bloqueaban eficazmente las neurotoxinas en una línea celular de rabdomiosarcoma y neutralizaban los venenos y una citotoxina en una línea celular de queratinocitos.
En modelos de ratón, los inhibidores protegieron a los ratones de los efectos paralizantes y letales de las neurotoxinas cuando se incubaron con estas antes de la inyección o cuando se administraron 15 o 30 minutos después (figura 1).
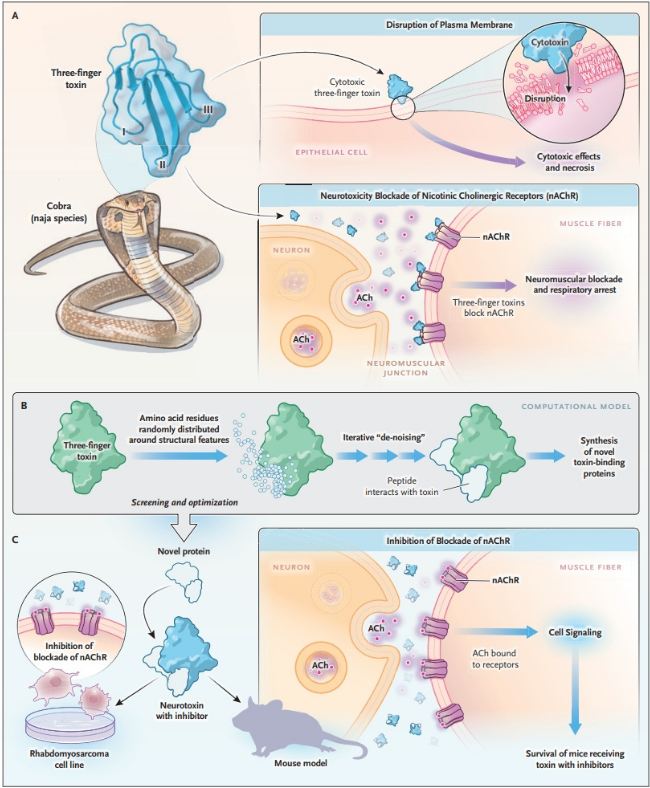
Figura 1: inhibición de las toxinas del veneno de serpiente con nuevas proteínas
Los hallazgos demuestran el potencial de las herramientas de deep learning para el desarrollo de inhibidores del veneno termoestables y sintetizables en grandes cantidades. El método permite diseñar proteínas que actúan como inhibidores contra diferentes tipos de toxinas presentes en el veneno, incluidas las fosfolipasas A₂, las metaloproteinasas y las serina proteasas, además de las toxinas de tres dedos.
El futuro del tratamiento del envenenamiento por mordedura de serpiente probablemente involucrará una combinación de antivenenos derivados de animales, anticuerpos recombinantes e inhibidores de varios tipos, incluidas proteínas novedosas, con variaciones según el tipo de veneno y los contextos regionales.
Los desafíos para la implementación clínica de estos nuevos inhibidores incluyen la evaluación preclínica en profundidad basada en modelos in vitro e in vivo, el desarrollo de marcos regulatorios para la aprobación, el compromiso de los fabricantes con la producción a gran escala y la implementación de políticas de salud pública para garantizar la disponibilidad y la accesibilidad, especialmente en regiones con alta incidencia de envenenamiento.
Fuente bibliográfica
Novel Proteins to Neutralize Venom Toxins
José María Gutiérrez, Ph.D.
Universidad de Costa Rica
N Engl J Med 2025; 392:2065-2068