Nueva ruta hacia la resistencia tumoral
El desarrollo de resistencia a la terapia contra el cáncer es un indicador importante de la mortalidad de los pacientes. Por lo tanto, comprender los mecanismos de resistencia es clave para mejorar los resultados terapéuticos. Recientemente, un estudio reportó el descubrimiento de un mecanismo de resistencia en células de cáncer de ovario que contienen una versión mutante del gen BRCA1. La dilucidación de los procesos moleculares que conducen a la resistencia pone de relieve las diversas maneras en que las células tumorales pueden adaptarse para sobrevivir, y revela las limitaciones de categorizar a los pacientes por sus mutaciones genéticas.
Re-mutaciones en BRCA
Las mutaciones en los genes BRCA1 y BRCA2 pueden causar cáncer de mama y de ovario al inactivar cualquiera de las dos vías biológicas principales que aseguran la estabilidad del genoma. Una de las vías repara el ADN de doble cadena que sufre un quiebre, a través de un proceso llamado recombinación homóloga (RH). El otro proceso denominado protección de horquilla, salvaguarda el ADN recién sintetizado en estructuras llamadas horquillas estancadas que surgen durante la replicación del ADN (DOI: 10.1016/j.ccr.2012.05.015).
En la reparación por RH, un paso esencial y limitante es el procesamiento (resección) de las roturas de la doble hebra por parte de las enzimas nucleasasas para producir ADN de una sola hebra (ss, del inglés single strand). BRCA1 actúa como una proteína reguladora clave que coordina el reclutamiento de las nucleasas, que incluyen el complejo proteico MRE11 - RAD50 - NBS1. BRCA1 también tiene un segundo papel en la reparación por RH: recluta a BRCA2, que a su vez carga la proteína RAD51 en el ADN ss. RAD51 ayuda a unir el ADN ss a una cadena complementaria que sirve como plantilla para una reparación libre de errores.
Las células cancerosas que tienen ciertas mutaciones en BRCA1 o BRCA2 no pueden reparar las roturas de doble cadena causadas por los medicamentos contra el cáncer que se usan actualmente en la clínica, y por lo tanto mueren cuando son tratadas. Entre estos fármacos se incluyen el cisplatino y los inhibidores de PARP (PARPi, fármacos que se dirigen específicamente a los tumores mutantes BRCA aprovechando sus defectos de reparación de roturas). Sin embargo, las células cancerosas pueden adquirir estrategias para eludir las acciones de los medicamentos, causando resistencia y limitando el uso de estos medicamentos inicialmente efectivos.
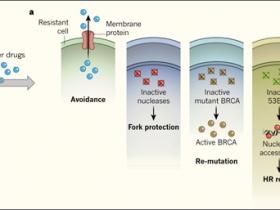
En su riguroso estudio, Yizhou Joseph He et al. utilizaron un método de revisión de edición genética para identificar los mecanismos de resistencia en las células de cáncer de ovario mutantes BRCA1 (DOI: 10.1038/d41586-018-07188-1). Una vía de resistencia conocida tanto en las células mutantes para BRCA1 como en las células con mutaciones en BRCA2 es la restauración de la función BRCA mediante la re-mutación de la mutación BRCA original (figura 1a). Un segundo mecanismo es la elusión medicamentosa, en la que una proteína de la membrana bombea el fármaco fuera de la célula o reduce su absorción. Los investigadores identificaron correctamente una proteína de membrana implicada en la absorción de cisplatino por las células tumorales como un contribuyente a la resistencia, verificando la idoneidad del enfoque de los autores.
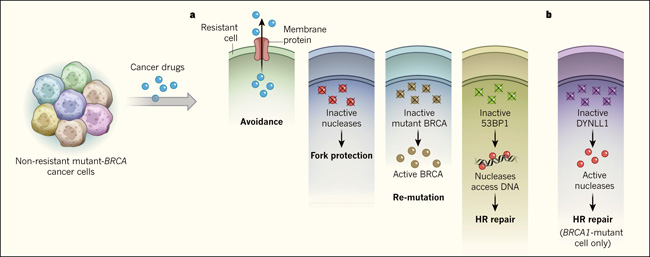
Figura 1: mecanismos de resistencia a los medicamentos en células cancerosas que contienen mutaciones en BRCA.
Numerosas células cancerosas tienen mutaciones en los genes BRCA1 o BRCA2. Estas mutaciones inactivan una vía de reparación del ADN que implica un proceso llamado recombinación homóloga (RH), o un proceso conocido como protección de horquilla que está implicado en la replicación del ADN. a, las células cancerosas BRCA mutantes han desarrollado muchos caminos diferentes para resistir la muerte por medicamentos contra el cáncer, incluyendo: elusión de medicamentos mediante bombeo de fármacos fuera de la célula a través de una proteína de membrana; restauración de la protección de la horquilla mediante la inactivación de enzimas nucleasas; re-mutación de la mutación original del BRCA para restaurar las funciones de las proteínas BRCA; y restauración de la reparación por RH, por ejemplo, mediante la desactivación de la proteína 53BP1 en células BRCA1 mutantes para permitir que las nucleasas tengan acceso al ADN. Aquí, las células resistentes se derivan de otras no resistentes del mismo color. b, Yizhou Joseph He y sus colegas reportan que en las células mutantes de BRCA1, pero no en las mutantes para BRCA2, la inactivación de la proteína DYNLL1 activa las nucleasas y, por lo tanto, restaura la reparación mediante RH.
Es importante destacar que uno de los genes más importantes identificados como causales de resistencia tanto al cisplatino como a PARPi fue DYNLL1. La proteína DYNLL1 actúa en muchos procesos celulares, incluyendo el transporte intracelular y la motilidad, y también inhibe la enzima óxido nítrico sintasa (que produce la molécula de señalización celular óxido nítrico), pero no había sido previamente involucrada en la resistencia al cáncer de próstata. Por lo tanto, descifrar cómo su inactivación conduce a la resistencia parecía una tarea de enormes proporciones.
Los autores establecieron firmemente que DYNLL1 actúa como regulador negativo de las nucleasasas que procesan el ADN - interactúa directamente con MRE11 y por lo tanto mantiene su actividad de nucleasa bajo control. La desactivación de DYNLL1, por lo tanto, desencadena la actividad de la nucleasa del MRE11, incluso cuando BRCA1 no está allí para ayudar a guiarlo a las rupturas, y así restaura la primera de las dos funciones de reparación por RH que normalmente lleva a cabo BRCA1 (figura 1b).
Conceptualmente, la resistencia al fármaco asociada a la inactivación de DYNLL1 es análoga a la causada por la inactivación de 53BP1, otra proteína que inhibe la resección del extremo del ADN, en este caso bloqueando el acceso de las nucleasas al ADN. Se ha reportado que la inactivación del 53BP1 restaura la resección y por lo tanto la resistencia en las células mutantes BRCA1, pero no en las células mutantes BRCA. Además, se sabe que DYNLL112 interactúa con 53BP1. Sin embargo, inesperadamente, los autores muestran que la resistencia asociada con la inactivación de DYNLL1 no ocurre a través de la pérdida de la interacción 53BP1-DYNLL1.
El estudio destaca la complejidad de las distintas funciones genéticas en la resistencia a los medicamentos contra el cáncer, y la importancia de definir mecanismos y actividades biológicas para predecir si las células tumorales serán destruidas. En este caso, la inactivación de DYNLL1 reactiva la resección, que se elimina en las células mutantes en BRCA1, pero no en las células tumorales mutantes de BRCA2. La inactivación de DYNLL1, por lo tanto, resulta en resistencia en las células mutantes BRCA1, pero no en las células mutantes BRCA2.
Finalmente, el estudio sugiere que la función molecular, en lugar de la función del genotipo -en este caso, el papel específico de BRCA1 en la resección, en lugar de su papel general en la reparación por RH o en la protección de la horquilla- dicta los resultados celulares. En términos más generales, estos resultados sugieren que se deben considerar estrategias de medicina personalizada que tengan en cuenta las funciones moleculares de los individuos, en lugar de categorizar a las personas únicamente por genotipo.
Fuente bibliográfica
A new road to cancer-drug resistance
Katharina Schlacher
Department of Cancer Biology, University of Texas MD Anderson Cancer Center, Houston, Texas 77058, USA.
DOI: 10.1038/d41586-018-07188-1