Insulinas inteligentes: el futuro del control de la diabetes
Una formulación sensible a la glucosa inyectada subcutáneamente ha demostrado eficacia en modelos animales y podría ofrecer beneficios significativos para los pacientes con la enfermedad, dado que presenta una mínima hipoglucemia y toxicidad.
Han pasado más de 100 años desde el descubrimiento de la insulina, un avance que transformó la diabetes de una enfermedad con alta morbilidad y mortalidad a una condición crónica manejable. Actualmente, el tratamiento se acerca más al objetivo de imitar los perfiles fisiológicos de la insulina endógena gracias a las formulaciones de acción rápida y prolongada, el monitoreo continuo de glucosa y los sistemas híbridos de circuito cerrado. Sin embargo, muchas personas con diabetes que siguen esta terapia aún enfrentan necesidades insatisfechas y pueden experimentar niveles de glucosa en sangre fuera de los límites recomendados durante períodos prolongados.
Las innovaciones en esta terapia incluyen la ingeniería de insulinas que actúan principalmente en el hígado y las insulinas sensibles a la glucosa (GRIs) o "inteligentes", que se activan cuando los niveles de glucosa en sangre aumentan y se inactivan cuando están en el rango normal. Imitan la función de las células beta al liberar la hormona según las necesidades basadas en los niveles variables de glucosa en sangre. Esto aumenta el tiempo en el rango óptimo durante las excursiones glucémicas diarias y reduce la incidencia de hipoglucemia e hiperglucemia en personas con diabetes.
Un equipo liderado por el investigador Juan Zhang de la Universidad de Zhejiang en China evaluó un nuevo tipo de GRI subcutánea en función de su capacidad de satisfacer tanto las necesidades prandiales como basales, utilizando evaluaciones de laboratorio y modelos preclínicos en ratones y cerdos enanos (figura 1). Primero, probaron la cinética in vitro de la liberación de insulina, encontrando una buena respuesta a la glucosa y un mejor control de sus niveles en sangre (por debajo de 200 mg/dL) en ratones con diabetes inducida, durante una semana, aunque la liberación de la hormona y su eficacia disminuyó a los 12 y 21 días.
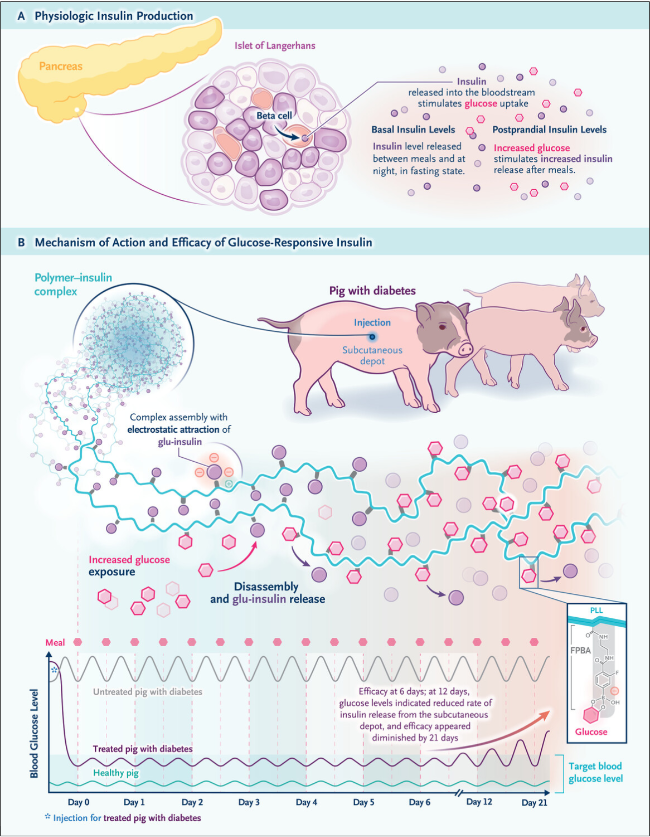
Figura 1: insulina sensible a la glucosa inyectada por vía subcutánea
El rendimiento de la GRI también se evaluó en tres cerdos enanos diabéticos, que imitan más de cerca las características fisiológicas de los humanos. El complejo mostró una eficacia sostenida en el control de los niveles de glucosa en sangre durante una semana y superó la efectividad de las inyecciones diarias de insulina glargina. En conjunto, estas observaciones sugieren que la formulación tiene un potencial clínico como insulina basal. En ambos estudios con ratones y cerdos enanos, se observó una hipoglucemia y toxicidad mínimas, y no se evidenció la formación de cápsulas fibrosas.
Hay varios desafíos clínicos que deben abordarse antes de su uso. Primero, es necesario demostrar que la GRI responde de manera precisa a un rango estrecho de glucosa para mantener adecuadamente los niveles en humanos. Los estudios in vivo no han confirmado este requisito. Segundo, la formulación inyectada presenta una disminución en la liberación de insulina tras múltiples ciclos, complicando el control de la dosis, especialmente problemático para personas con diabetes tipo 1. Los episodios hiperglucémicos tempranos podrían agotar el depósito de insulina, afectando el control glucémico posterior. Tercero, sería tranquilizador demostrar una alta selectividad para la glucosa y la invulnerabilidad a la liberación de la hormona inducida por otros estímulos.
Otro desafío es si la GRI puede realmente imitar la liberación endógena de insulina respondiendo a cambios rápidos en los niveles de glucosa, haciendo viable su uso en terapias de insulina en bolo o prandial en humanos. La posición subcutánea del depósito podría causar un desfase temporal en la difusión de la glucosa desde la sangre al líquido intersticial. Es crucial que una GRI responda adecuadamente a diferentes tipos de comidas. Aunque los datos actuales satisfacen las necesidades basales, sería útil comparar esta GRI con las nuevas formulaciones en cuanto a la carga de atención y el control glucémico. Además, a pesar de que los datos a corto plazo sobre toxicidad son alentadores, es necesario investigar los posibles efectos tóxicos a largo plazo.
Este estudio amplía la creciente investigación sobre las insulinas sensibles a la glucosa, ofreciendo una prueba de concepto de una formulación biodegradable que libera insulina de manera sensible a la glucosa, demuestra eficacia a largo plazo in vivo y parece tener una toxicidad mínima. Sin embargo, se necesitan estudios adicionales antes de que este agente pueda considerarse una opción viable en humanos.
Fuente bibliográfica
Engineering an Insulin Complex to Treat Diabetes
William T. Cefalu, M.D., and Guillermo Arreaza Rubín, M.D.
Division of Diabetes, Endocrinology, and Metabolic Diseases, National Institute of Diabetes and Digestive and Kidney Diseases, National Institutes of Health, Bethesda
N Engl J Med 2024;390:2214-2216






