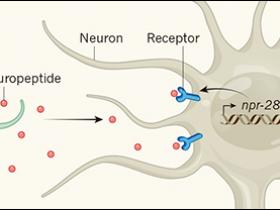
Culpa genética en el envejecimiento
La tasa de deterioro del comportamiento biológico de la población que envejece es notablemente variable entre los individuos. A pesar del considerable interés en estudiar su variación natural para identificar componentes que controlen el envejecimiento normal y saludable, todavía no se han encontrado tales factores. Un estudio reciente provee una base genética para la variación de las tasas de envejecimiento en el organismo modelo Caenorhabditis elegans. Se evidenció que diferentes cepas de este nemátodo muestran diversas reducciones en su comportamiento reproductivo, y funciones como el bombeo faríngeo y la locomoción. Los polimorfismos del ADN en un gen codificante para un neuropéptido (regulatory gen for behavioural ageing-1, rgba-1), y en el gen del receptor de neuropéptidos (npr-28) influyen en la tasa de declive de la conducta de apareamiento asociado con la edad. La proteína codificada por rgba-1 derivada de la glia activa la señalización NPR-28, que actúa en neuronas serotonérgicas y dopaminérgicas para acelerar el deterioro del comportamiento. Esta señalización implica la activación una vía que modula el envejecimiento. En consecuencia, la variación natural en la señalización glia-neurona mediada por neuropéptidos puede regular la tasa de envejecimiento.
Variantes genéticas y deterioro
La secuenciación del genoma humano fue publicada en 2001, pero la secuencia de ADN de cualquier individuo no coincide exactamente con esta referencia. Cada genoma individual contiene millones de polimorfismos - regiones variables que difieren de la referencia. Muchas investigaciones se dedican a entender cómo los polimorfismos influyen en los rasgos biológicos, pero esto sigue siendo un reto formidable, porque la base genética subyacente a tales características es compleja. En un estudio reciente (doi: 10.1038/nature24463) Jiang-An Yin y colaboradores suman nuevos aportes a la comprensión de la base genética del envejecimiento. Los autores informan que, en nemátodos, la lombriz Caenorhabditis elegans (C. elegans) la variación genética natural en dos genes, modifica el declive relacionado a la edad, específicamente en características de apareamiento y alimentación. Los autores demuestran que esta variación actúa para modular una vía de señalización que controla la actividad neuronal.
En la genética clásica, los genes que regulan los rasgos de interés se identifican mediante el análisis de muchos animales que han sido objeto de mutación de tal manera que cada uno alberga un cambio genético diferente. Este enfoque se ha utilizado durante mucho tiempo en organismos modelo para identificar cambios únicos y dañinos que causan la inactivación de un gen, regulando los rasgos biológicos. Sin embargo, las diferencias de rasgos entre individuos son típicamente influenciadas por una multitud de cambios genéticos, que perturban la expresión génica sólo ligeramente. Esto es probablemente atribuible, al menos en parte, a factores evolutivos que purgan mutaciones que tienen un efecto deletéreo o negativo sobre la aptitud evolutiva de la población.
C. elegans se usa a menudo para estudios genéticos del envejecimiento, porque tiene una esperanza de vida de sólo unas dos semanas. Los autores estudiaron las diferencias en la tasa de envejecimiento en estado silvestre de cepas del gusano (una estrategia que es comparable a estudiar las diferencias naturales en individuos de una población). En vez de centrarse sólo en la esperanza de vida, los autores midieron las tasas de deterioro relacionado con la edad en rasgos asociado con el apareamiento, alimentación y locomoción, para examinar cuan sanas permanecían las lombrices más tardíamente.
Algunos autores habían demostrado previamente que los cambios en la expresión de la enzima BAS-1 se correlacionan con el declive relacionado con la edad en dos rasgos: la virilidad de apareamiento y el bombeo de la faringe, que lleva alimento al intestino desde el ambiente. En el estudio actual, los investigadores mapearon las variantes genéticas que modulan la expresión de BAS-1, y encontraron polimorfismos en un solo gen responsable de aproximadamente la mitad de la variación en el declive relacionado con la edad en estos dos rasgos. Los investigadores denominaron al gen, rgba-1 (del inglés, regulatory-gene-for-behavioural-ageing-1) y mostraron que las mutaciones que causan la pérdida de la función rgba-1 previenen el deterioro de este comportamiento biológico.
El gen rgba-1 parece ser único para C. elegans (no está presente en otros nemátodos estrechamente relacionados), sugiriendo que evolucionó en el linaje de C. elegans. Los autores mostraron que el gen codifica cuatro fragmentos proteicos llamados neuropéptidos. Los neuropéptidos pueden actuar como neurotransmisores, que transmiten señales entre neuronas, o como moléculas de señalización de acción lenta llamadas neuromoduladores que modifican la dinámica neuronal y la neurotransmisión. A través de una variedad de experimentos, identificaron el receptor de neuropéptidos 28 (NPR-28) como el receptor para uno de los neuropéptidos rgba-1, RGBA-1-2b. Aunque los neuropéptidos rgba-1 son específicos de C. elegans, el NPR-28 no lo es. Está relacionado con receptores de los neuropéptidos humanos somatostatina y nociceptina. Al igual que el NPR-28, los receptores humanos modulan la función neuronal.
Yin y sus colegas encontraron que el gen npr-28 también alberga polimorfismos que modifican el declive de apareamiento en las cepas silvestres de gusano. Aunque el envejecimiento ha sido ampliamente estudiado en C. elegans, los npr-28 y rgba-1 no han sido identificados como genes asociados a la edad por ningún enfoque genético clásico, lo que sugiere que esta vía neuropeptídica podría ser particularmente relevante para la variación genética que causa cambios sutiles de comportamiento. De hecho, ya se ha demostrado que los sistemas de señalización de neuropéptidos desempeñan un papel en la variación del comportamiento en diversos entornos.
Debido a que los neuromoduladores tienen un papel importante en la regulación de la actividad de la señalización neuronal de largo alcance entre las regiones cerebrales, la expresión de los neuropéptidos y sus receptores es un sustrato genético importante sobre el que las fuerzas evolutivas pueden actuar para optimizar los comportamientos. No se espera que los rasgos de envejecimiento que regulan rgba-1 y npr-28 estén bajo selección evolutiva, ya que regulan los comportamientos en animales adultos mayores, después de que se haya producido la mayor parte de la reproducción. Sin embargo, es probable que este sistema de señalización también regule los rasgos de comportamiento en animales más jóvenes que se encuentran bajo presión evolutiva - el declive relacionado con el envejecimiento asociado con estos genes es simplemente un efecto secundario.
Los autores demostraron que uno o más de los neuropéptidos codificados por rgba-1 eran liberados por las células gliales (figura 1). Estas células fueron identificadas originalmente por su papel en el suministro de apoyo físico y nutricional a las neuronas. Sin embargo, también pueden modificar directamente los circuitos neuronales liberando moléculas de señalización glial.
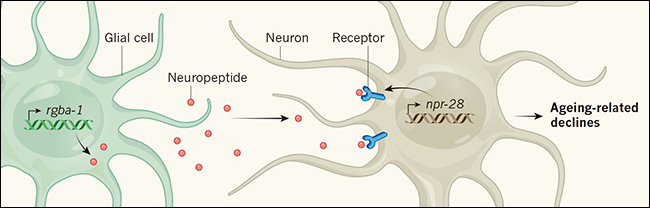
Figura 1. Regulación del declive de la salud asociada con al envejecimiento.
Jiang-An Yin y colaboradores (doi: 10.1038/nature24463) reportaron que en el nemátodo Caenorhabditis elegans, las células gliales que apoyan neuronas expresan el gen rgba-1, que codifica cuatro tipos de neuropéptidos. Uno o más de estos, se liberan de las células gliales en gusanos que envejecen y se unen al receptor del neuropéptido 28 (codificado por el gen npr-28) en ciertas neuronas. Los autores demuestran que la variación genética natural en rgba-1 y npr-28 modula la velocidad a la que las lombrices se vuelven deficientes en dos comportamientos - la capacidad de apareamiento y el bombeo faríngeo, que está involucrado en la alimentación - durante el envejecimiento.
Finalmente, los autores demostraron que el npr-28 se expresa en neuronas que producen los neurotransmisores serotonina y dopamina. Cuando es activado por el RGBA-1-2b, el receptor reprime la actividad de una respuesta al estrés -la respuesta mitocondrial a proteínas desplegadas (mtUPR).
Es tentador especular que la liberación de los neuropéptidos rgba-1 se desencadena cuando la glía percibe cambios inducidos por la edad en la función o salud de las células neuronales que soportan. Tal mecanismo podría vincular el deterioro dependiente de la edad en la función neuronal con cambios regulados en los circuitos neuronales. Por ejemplo, la disminución de la señalización dopaminérgica en ancianos debido a la muerte de las neuronas liberadoras de dopamina. Se piensa que esta disminución contribuye a los síntomas neurológicos del envejecimiento, incluida la pérdida de control cognitivo y de memoria. Tal vez la disminución de los niveles de dopamina están mediados por la señalización de los neuropéptidos - el aumento de la acción de mtUPR podría retrasar este proceso. Sin embargo, los autores no demostraron que mtUPR actúe en las neuronas productoras de dopamina, por lo que también es posible que la actividad de las neuronas productoras de dopamina y serotonina module la vía de mtUPR en las células río abajo.
El trabajo de Yin y sus colegas sirve como un valioso ejemplo mecanístico sobre cómo la variación genética puede modificar el declive dependiente de la edad. Un reto importante que queda por resolver es determinar si los neuropéptidos tienen un papel similar en la regulación de la esperanza vida sana en humanos. Los receptores neuropéptidos son miembros de la familia de receptores acoplados a proteína G, a los que a menudo se unen fármacos para el tratamiento de enfermedades. Centrarse en la señalización de los neuropéptidos en el envejecimiento humano podría conducir al desarrollo de fármacos que reduzcan el deterioro de la salud relacionadas con el envejecimiento. Aunque es probable que los mecanismos que regulan el envejecimiento normal impliquen algo más que una simple señalización por neuropéptidos, estos desarrollos podrían alargar el tiempo que cada individuo pasa en un estado saludable y juvenil.
Fuente bibliográfica
Neurobiology: A genetic cause of age-related decline
Patrick T. McGrath
School of Biological Sciences, Georgia Institute of Technology, Atlanta, Georgia 30332, USA.
doi:10.1038/551179a