Biomarcadores de respuesta en carcinoma urotelial
Los anticuerpos que se dirigen a la PD-1 o a su ligando PD-L1, como el atezolizumab, tienen una gran eficacia en el cáncer urotelial metastásico, lo cual podría potenciarse gracias a biomarcadores para facilitar la identificación de tumores que responden al tratamiento. Recientemente, se han publicado resultados de un estudio de fase 2 de un solo brazo, en el que se investigan dos ciclos de atezolizumab antes de la cistectomía en 95 pacientes con cáncer urotelial muscular invasivo. Como variables de evaluación secundarias de este estudio se incluyeron la seguridad, la supervivencia sin recaídas y el análisis de biomarcadores: la alta expresión de CD8 dentro del tumor y la firma transcripcional de linfocitos T citotóxicos de ocho genes en particular, incluyendo a interferón gamma y citoquinas específicas.
Firmas moleculares
Los inhibidores de puntos de control son medicamentos que se dirigen a los reguladores clave del sistema inmunológico. Dos inhibidores de punto de control, el pembrolizumab (contra la proteína de muerte programada PD-1) y el atezolizumab (contra el ligando de PD-1 o PD-L1) han recibido la aprobación de la Administración de Alimentos y Fármacos de los Estados Unidos (FDA) para el tratamiento del cáncer urotelial metastásico (mUC). Dado que la minoría de los pacientes con mUC que reciben estos fármacos se benefician -las tasas de respuesta global son del 23 al 29%-, se están buscando marcadores biológicos para ayudar a seleccionar a los pacientes con probabilidad de beneficiarse en el escenario de una metástasis. Recientemente, también se está estudiando la inmunoterapia en el entorno prequirúrgico (conocido como entorno neoadyuvante) en el cáncer de vejiga invasivo muscular, donde el estándar de atención es la quimioterapia seguida de la resección de la vejiga. En un reciente estudio Powles y colaboradores (DOI: 10.1038/s41591-019-0628-7) reportan los resultados del ensayo clínico ABACUS (ClinicalTrials.gov identifier: NCT02662309) que evaluó dos ciclos de atezolizumab neoadyuvante en el cáncer urotelial muscular invasivo operable de la vejiga en el que se realizaron estudios tisulares para identificar biomarcadores predictivos de respuesta (figura 1).
Entre los 88 pacientes evaluables del estudio, la respuesta patológica completa (pCR) -el criterio de valoración primario del estudio- fue del 31%. Esto es comparable a la tasa de pCR del ensayo PURE-01 que investiga el tratamiento neoadyuvante del carcinoma urotelial con pembrolizumab y la quimioterapia neoadyuvante con gemcitabina/cisplatino y pembrolizumab. El ensayo ABACUS incluyó pacientes de mayor riesgo que en PURE- 01 (pembrolizumab preoperatorio), ya que no eran elegibles para el tratamiento con cisplatino y tenían enfermedad residual en vejiga antes de recibir atezolizumab. Es notable que en el ensayo ABACUS, la respuesta de los pacientes se logró después de solo dos ciclos de inmunoterapia neoadyuvante, y esto es consistente con el bloqueo neoadyuvante de PD-1 en el melanoma, en el que se observó una rápida respuesta inmunológica y clínica con una revigorización de las células T que alcanzó su punto máximo una semana después del inicio del tratamiento.
Anteriormente, los biomarcadores como PD-L1, la carga de mutación tumoral (TMB), las mutaciones relacionadas con la reparación de daño al ADN (DDR) y ciertos subtipos moleculares y fenotípicos se han asociado con la respuesta a la inmunoterapia en individuos con mUC. En los pacientes que participaron en el ensayo PURE-01, la alta TMB, el alto número de alteraciones DDR y el estado positivo de PD-L1 (P = 0,01) en el preoperatorio se correlacionaron por separado con la pCR después del tratamiento con pembrolizumab neoadyuvante. Estos marcadores fueron analizados como parte del estudio ABACUS, pero ninguno se correlacionó con los resultados clínicos. Sin embargo, es importante notar que los umbrales para DDR y TMB "altos", así como los ensayos para PD-L1 no están estandarizados a través del campo y difieren a través de estos estudios.
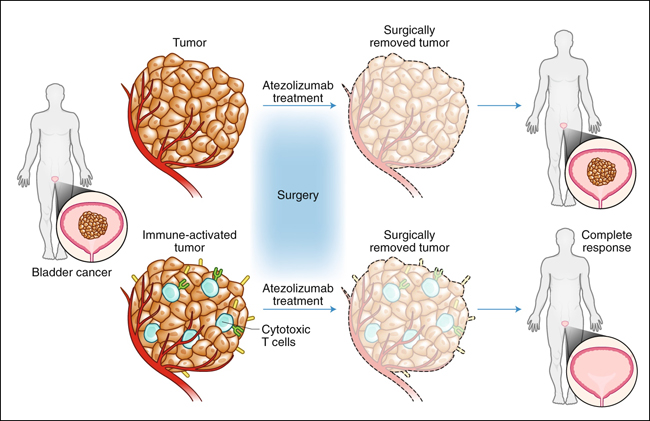
Figura 1: Biomarcadores inmunológicos que sugieren una respuesta a la inmunoterapia neoadyuvante.
Powles y sus colegas encontraron que la presencia de células T CD8+ activadas en el tumor y la firma de células T citotóxicas se correlacionan con la respuesta inmunitaria en los pacientes que reciben inmunoterapia neoadyuvante para el tratamiento del cáncer de vejiga invasivo muscular.
El mUC también puede clasificarse en distintos subtipos moleculares, y el subtipo Lund "genómicamente inestable" se ha asociado con la respuesta a la inmunoterapia. Sin embargo, este subtipo no se asoció con la respuesta en el estudio ABACUS. Anteriormente, se han descrito distintos fenotipos inmunológicos como "inmune inflamado", "inmunoexcluido" y "desierto inmunológico" en el mUC3, y los tumores inflamados -aquellos con mayor infiltración inmunológica- tenían la mayor respuesta al atezolizumab en mUC. Los autores evidenciaron en este ensayo que la presencia del fenotipo inmune inflamado en los pacientes no se correlacionó con la respuesta en el mUC.
Sin embargo, los autores observaron que la alta expresión de CD8 dentro del tumor y la firma transcripcional de células T citotóxicas de 8 genes (IFN, CXCL9, CD8A, GZMA, GZMB, CXCL10, PRF1, TBX21) se correlacionan fuertemente con la pCR. Se reportaron resultados análogos en PURE-01, donde la expresión de la firma inmunológica del interferón gamma fue significativamente mayor en las lesiones pre terapéuticas de los pacientes que lograron pCR en comparación con las lesiones pre terapéuticas de quienes no lograron la pCR. Puede ser que, tal como en el melanoma, las células T CD8+ previamente preparadas se agoten y luego, tras el bloqueo de la PD-1, se revitalicen rápidamente, lo que da lugar a una respuesta inmunitaria. Un mayor entendimiento de los subtipos de células T CD8+ en el cáncer de vejiga aclararía el mecanismo.
Los resultados obtenidos justifican la validación en un conjunto de datos independiente. Los biomarcadores como TMB, alteraciones DDR, PD-L1 y subtipos moleculares, que anteriormente se había reportado que enriquecían la respuesta al atezolizumab en la enfermedad metastásica, no lo hicieron en el entorno neoadyuvante en este estudio. Aunque la asociación entre la firma de células T citotóxicas y la pCR fue significativa, un tamaño de ensayo más amplio confirmaría aún más esto. El desarrollo de métodos consistentes de puntuación para determinar la expresión de CD8 "alta" versus "baja" y las firmas estándar de células T será importante para traducir este hallazgo al uso clínico. Aunque algunos de los biomarcadores inmunológicos entran en conflicto con los datos de PURE-01, donde los tumores PD-L1-positivos y de alta DDR tuvieron una mayor respuesta a la inmunoterapia, los datos de los biomarcadores fueron reportados en solo 50 pacientes en PURE-01, y hasta la fecha ningún conjunto de hallazgos ha sido validado independientemente en una cohorte posterior. Además, el uso de diferentes fármacos de inmunoterapia, las diferencias en las poblaciones de pacientes y tres en vez de dos ciclos de inmunoterapia neoadyuvante pueden contribuir a algunas diferencias entre los dos estudios.
A medida que la inmunoterapia neoadyuvante y los regímenes de quimioinmunoterapia de combinación demuestren resultados alentadores en el cáncer urotelial, la identificación de biomarcadores validados para predecir la respuesta inmunológica informará las mejores decisiones de tratamiento. El trabajo de Powles y sus colaboradores es un paso en esa dirección. En última instancia, el poder determinar a quién ofrecer inmunoterapia neoadyuvante frente a la quimioterapia versus la terapia de combinación permitiría maximizar el beneficio, minimizar el riesgo y mejorar los resultados de los pacientes.
Fuente bibliográfica
Biomarkers for neoadjuvant checkpoint blockade response in urothelial cancer
Pooja Ghatalia & Elizabeth Plimack
Fox Chase Cancer Center, Philadelphia, PA, USA
Nat Med. 2019 Nov;25(11):1650-1651