Beneficios de la grasa en la diabetes tipo 2
Los lípidos permiten restaurar la secreción de insulina a niveles casi normales.
Con casi el 10% de la población mundial afectada, la diabetes de tipo 2 es un problema de salud pública de primer orden. Un estilo de vida excesivamente sedentario y una dieta demasiado calórica favorecen el desarrollo de esta enfermedad metabólica al alterar el funcionamiento de las células pancreáticas y hacer menos eficaz la regulación del azúcar en sangre. La grasa -que se asume culpable de la enfermedad- no la agrava necesariamente e incluso podría desempeñar un papel protector.
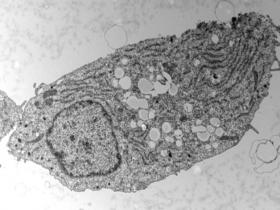
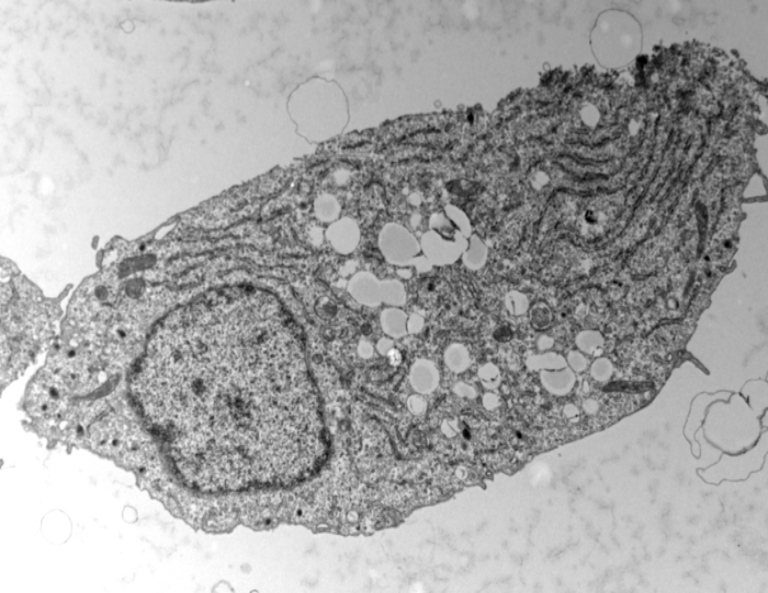
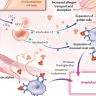
La secreción de insulina es impulsada por la elevación de la glucosa en sangre, que activa el acoplamiento metabolismo-secreción en la célula beta pancreática. La elevación resultante del ATP citosólico cierra los canales de potasio induciendo la despolarización de la membrana y la afluencia de calcio que desencadena exocitosis de la insulina. Se ha propuesto que la exposición crónica de estos organismos celulares a un nivel elevado de glucosa y ácidos grasos induce glucolipotoxicidad.
En este contexto, un grupo de investigadores de Universidad de Ginebra delinearon el patrón de expresión de los genes relacionados con las vías lipídicas junto con el almacenamiento/movilización de grasas durante la secreción de insulina estimulada por la glucosa.
Para este experimento, el grupo cultivó células secretoras de insulina durante tres días, a diferentes concentraciones de glucosa (5.5, 11.1, 25 mmol/l) sin o con palmitato y oleato de 0,4 mmol/l complejados con albúmina de suero bovino. Luego, se realizaron análisis transcriptómicos de las vías de los lípidos en islotes humanos mediante RNA-Seq (Secuenciación del Transcriptoma Entero para Clonación al Azar).
Como resultado, la exposición crónica a palmitato y oleato modificó la expresión de un panel de genes implicados en el manejo de lípidos. La exposición a ácidos grasos C18:1 insaturados favoreció la acumulación de lípidos intracelulares de forma dependiente de la glucosa, efecto que también se observó con ácidos grasos C16:0 saturados cuando se combina con el inhibidor de panlipasa Orlistat. La tasa de movilización de lípidos estuvo determinada principalmente por los niveles de grasa almacenada como consecuencia directa de las condiciones de cultivo más que por las demandas energéticas, excepto en las células cargadas con palmitato.
Para diferenciar el efecto de la grasa del del azúcar, los científicos expusieron las células beta a un exceso ambos factores de manera individual y en conjunto. En primer lugar, se confirmó la toxicidad del azúcar: las células expuestas a altos niveles de esta secretaban mucha menos insulina de lo normal. Gracias a esto, se demostró que la reserva de grasa, en lugar de empeorar la situación, permite restablecer la secreción de insulina a niveles casi normales.
Al analizar más a fondo los cambios celulares en juego, el equipo se dió cuenta de que las gotas de grasa no eran reservas estáticas, sino que eran el lugar de un ciclo dinámico de almacenamiento y movilización. Y gracias a estas moléculas de grasa liberadas, las células beta se adaptan al exceso de azúcar y mantienen la secreción de insulina casi normal.
Ahora, los científicos intentan determinar el mecanismo detrás de este proceso, con la esperanza de descubrir una forma de retrasar la aparición de la diabetes.