Rompiendo los cristales del asma
Aunque la cristalización espontánea de proteínas es un evento poco frecuente in vivo, los cristales de Charcot-Leyden (CLC) que consisten en la proteína galectina-10 (Gal10) se observan con frecuencia en enfermedades eosinofílicas, como el asma. En este estudio se evidencia que los CLC derivados de pacientes muestran un ensamblaje cristalino y estructura de Gal10 idéntica a la de los cristales de esta proteína cultivados in vitro. Cuando se administra a las vías respiratorias, la Gal10 cristalina estimula la inmunidad innata y adaptativa y actúa como adyuvante de tipo 2. Por el contrario, una Gal10 mutante soluble es inerte. Los anticuerpos dirigidos contra los epítopos clave de la interfaz de cristalización disuelven CLC preexistentes en mucosidad de pacientes en cuestión de horas y revierten la inflamación impulsada por cristales, la síntesis de inmunoglobulina E (IgE) y la hiperreactividad bronquial en un modelo humanizado de asma. Por lo tanto, los cristales de proteína pueden promover las características distintivas del asma y son susceptibles de ser tratados con anticuerpos mediante su desintegración.
Galectina-10
Los cristales de Charcot-Leyden se han observado en mucosidad de las vías respiratorias de pacientes con enfermedad alérgica de las vías respiratorias desde el siglo XIX, pero su función en la patogénesis de la alergia no está clara. Los cristales de Charcot-Leyden y la lisofosfolipasa son abundantes en eosinófilos y basófilos, y originalmente, se pensaba que la lisofosfolipasa era la proteína constituyente de estos cristales. La elucidación posterior de la organización, secuencia y estructura genómica de la proteína constituyente reveló el dominio característico de reconocimiento de carbohidratos de las galectinas, un hallazgo que llevó a la designación de la proteína como galectina-10. Las galectinas son proteínas conservadoras de glicano conservadas evolutivamente, o lectinas, con afinidad canónica por los glicoconjugados modificados con beta-galactosa. Regulan las interacciones proteína-proteína tanto dentro de la célula como en la matriz extracelular (figura 1A).3 Entre las aproximadamente 20 proteínas de galectina humana conocidas generadas a través del empalme alternativo de ARNs pre-mensajero a partir de 11 genes, sólo se sabe que la galectina-10 cristaliza rápida y espontáneamente bajo ciertas condiciones, incluso después de la exocitosis del eosinófilo en el medio extracelular.
Persson y sus colegas, con la intención de obtener más información sobre los mecanismos biológicos de la galectina-10 en las vías respiratorias, verificaron recientemente que los cristales de Charcot-Leyden son abundantes en muestras de tejido obtenidas de pacientes con rinosinusitis crónica con pólipos nasales -una enfermedad asociada con la infiltración de eosinófilos- y utilizaron datos estructurales de las radiografías para confirmar la biosimilitud de los cristales de Charcot-Leyden in situ y de la galectina-10 expresada de forma recombinante (DOI: 10.1126/science.aaw4295). Cuando los autores eliminaron un tag de histidina ubicado estratégicamente, de la proteína recombinante, se produjo la cristalización espontánea de los dímeros de galectina-10, y una combinación de análisis estructurales y mutacionales los llevó a diseñar una galectina-10 mutante dimérica, en la que se reemplazó el aminoácido tirosina en la posición 69 por ácido glutámico (Tyr69Glu). La proteína mutante no pudo cristalizarse debido a la interrupción del apilamiento de anillos aromáticos en el punto crítico ("crystal-packing hotspot" Tyr69). La inoculación de cristales nativos de Charcot-Leyden en pulmones de ratones causó la inducción de citoquinas innatas como la interleucina-6 y el factor de necrosis tumoral α y fue acompañada de infiltración tisular por neutrófilos y monocitos. Sin embargo, la inoculación de dímeros mutantes no cristalizables no tuvo un efecto similar.
La exposición de los residuos polares de Tyr69 en las puntas de los dímeros de galectina-10, lejos del dominio de reconocimiento de carbohidratos, creó un sitio inmunogénico en la interfaz de cristal que fue explotado para crear nanoanticuerpos (nanobodies ) en llamas. Los nanoanticuerpos son proteínas terapéuticas que aprovechan el hecho de que los camélidos (por ejemplo, llamas y camellos) poseen anticuerpos totalmente funcionales que sólo contienen cadenas pesadas. Los nanobodies específicos de galectina-10 se colocaron en los andamiajes de IgG humana y de ratón para crear anticuerpos que fueron seleccionados por su capacidad de disolver los cristales de galectina-10. Los autores encontraron que los anticuerpos monoclonales anti-galectina-10 se dirigían con precisión a las puntas polares críticas expuestas del Tyr69 en los cristales de Charcot-Leyden, y en muestras de mucosidad de pacientes con rinosinusitis crónica con pólipos nasales, y que estos anticuerpos disolvían los cristales. Además, en ratones inmunodeficientes que se reconstituyeron con células mononucleares de sangre periférica de pacientes con alergia a los ácaros del polvo doméstico, la hiperplasia de la mucosa de las vías respiratorias y el aumento de la IgE y la resistencia de las vías respiratorias se desarrollaron cuando estuvieron expuestos al alérgeno en presencia de cristales de Charcot-Leyden. Estos cambios fueron abrogados por la coadministración del anticuerpo anti cristal de Charcot-Leyden. De esta forma, los autores revelaron un papel de los cristales de Charcot-Leyden en la patogénesis y una base para un enfoque terapéutico experimental: la disolución de los cristales en tejidos afectados.
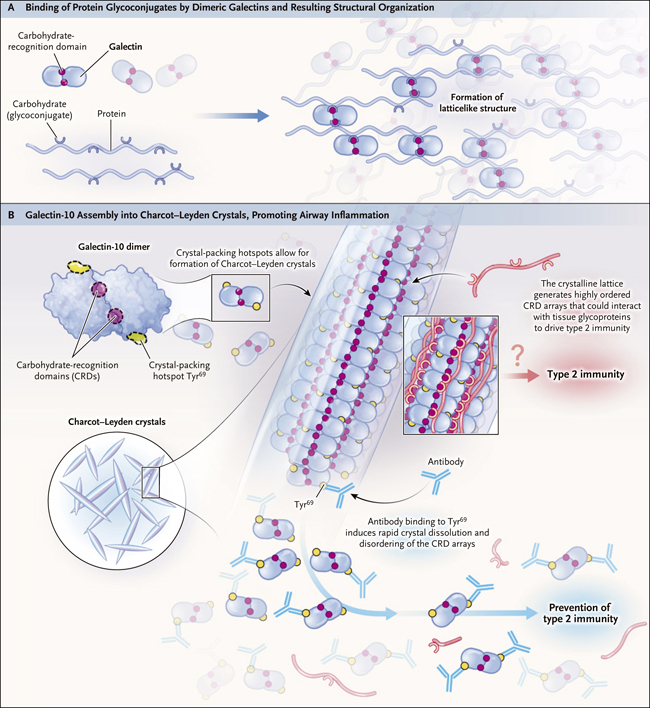
Figura 1. Cristales de Charcot-Leyden e inflamación de las vías respiratorias.
Las galectinas diméricas se unen a glicoconjugados de proteínas y confieren organización estructural (panel A). Las galectinas prototípicas utilizan dominios de reconocimiento de carbohidratos para entrecruzar glicoconjugados en proteínas intra y extracelulares, creando así estructuras críticas para la función de los tejidos. El ensamblaje de galectina-10 en cristales de Charcot-Leyden promueve la inflamación de las vías respiratorias (panel B). El residuo de tirosina en la posición 69 (Tyr69) de la galectina-10 promueve la organización simétrica espontánea en los cristales de Charcot-Leyden. La red cristalina genera matrices altamente ordenadas de dominios de reconocimiento de carbohidratos con el potencial de interacciones de alta viscosidad con las glicoproteínas tisulares. Persson y colaboradores (DOI: 10.1126/science.aaw4295) reportaron recientemente que la unión de anticuerpos a Tyr69 apicalmente expuesto interrumpe el punto crítico de empaquetamiento de los cristales, lo que lleva a la disolución de la red y al desorden de las matrices del dominio de reconocimiento de carbohidratos. Los autores usaron modelos de ratón para mostrar que los cristales de Charcot-Leyden provocan inmunidad tipo 2, mientras que los dímeros no tienen tal efecto, y que la disolución de los cristales disminuye la inflamación de las vías respiratorias - hallazgos que sugieren potenciales estrategias terapéuticas. La elucidación de los supuestos compañeros de unión tisular para el dominio de reconocimiento de carbohidratos de la galectina-10 puede aclarar aún más las vías inductivas del huésped que desencadenan la inmunidad tipo 2.
Los ratones no expresan galectina-10, pero sí expresan proteínas relacionadas con la galectina con especificidades alteradas de glicano, una propiedad que ahora se sabe que se comparte con la galectina-10. Una de estas proteínas es prominente en el cristalino de los roedores, donde se asocia con proteínas cristalinas que establecen el ambiente transparente y libre de orgánulos del cristalino curvado. La capacidad de las galectinas diméricas para establecer estructuras de forma latente permite una mayor avidez para la unión de baja afinidad aumentando el número de dominios de interacción a través de un proceso ordenado que se asemeja a la formación de cristales.
En una proteína relacionada con la galectina que se encuentra en hongos, el residuo clave en el dominio de reconocimiento de carbohidratos (que normalmente mediaría la unión con la galactosidasa) es la variante, que permite el reconocimiento de quitooligosacáridos, componentes repetitivos de la pared celular de hongos e insectos depredadores. La quitina es un andamiaje estructural insoluble de parásitos, insectos y hongos, y reúne numerosas glicoproteínas que pueden convertirse en alérgenos cuando entran o invaden la mucosa de los vertebrados. La respuesta inmune a las partículas de quitina inhaladas en ratones se asemeja a la respuesta inflamatoria mixta a los cristales de Charcot-Leyden en estos animales, descrita por Persson y sus colegas, lo que sugiere una vía generalizada para hacer frente a las partículas indigeribles. Tal vez la cristalización en células de mamíferos representa una respuesta análoga a la formación de quitina en invertebrados, un proceso que utiliza el ensamblaje reiterativo para generar un elemento estructural robusto al mismo tiempo que crea sitios repetitivos de alta validez que pueden ser reconocidos por las células y tejidos inmunes del huésped como parte de una reacción de barrera especializada (figura 1B).
La disolución de los cristales de Charcot-Leyden en pacientes con asma y en personas con rinosinusitis crónica con pólipos nasales puede tener beneficios terapéuticos. Actualmente existen tratamientos dirigidos a los eosinófilos. Sin embargo, en algunos casos, los cristales de Charcot-Leyden pueden persistir en los tejidos o pueden derivarse de los basófilos, y se carece de la disponibilidad de tratamientos dirigidos a estos cristales. En la medida en que estas estructuras representen un componente biofísico influyente en la mucosidad patológica de las vías respiratorias, la disolución de los cristales podría disminuir la elasticidad y mejorar la depuración. Los tapones de mucosidad persistente, ricos en eosinófilos, ocurren comúnmente en el asma severa, y se necesitan agentes terapéuticos que se dirijan a esta condición patológica. Además, la activación de las respuestas inmunitarias innatas y adaptativas en las vías respiratorias por los cristales de Charcot-Leyden puede disminuir por la disolución de los cristales, lo que podría resultar en efectos antiinflamatorios independientes de los efectos mucolíticos. Con este fin, los nanobodies derivados de camélidos presentan varias ventajas como terapéuticos inhalados, debido a su pequeño tamaño, estabilidad térmica, alta solubilidad y corta vida media sistémica. Aunque se necesita más trabajo para determinar el papel de los cristales de Charcot-Leyden en la enfermedad, la historia de estos cristales es fascinante, y tal investigación puede aportar información adicional sobre los mecanismos básicos que subyacen a la inmunidad de tipo 2.
Fuente bibliográfica
Making Asthma Crystal Clear
John V. Fahy, M.D., and Richard M. Locksley, M.D.
Department of Medicine, the Cardiovascular Research Institute and the Howard Hughes Medical Institute, University of California, San Francisco.
DOI: 10.1056/NEJMcibr1908064