Ritmo ultradiano, vital para el desarrollo pancreático
La ruta de Señalización Notch es un sistema de señalización celular altamente conservado en animales, cuyo propósito principal es controlar el destino celular. Por ejemplo, regula la proliferación de las células progenitoras pancreáticas multipotenciales (CPM) y su diferenciación en progenitores bipotenciales (BP) y células proacinares unipotentes (PAC). Recientemente se ha descrito que las rápidas oscilaciones ultradianas del ligando de la proteína receptora Notch, Dll1 y del efector transcripcional Hes1 son cruciales para la expansión de las CPM, y los cambios en los parámetros de oscilación de Hes1 se asocian con la adopción selectiva del destino de las BP o PAC. Por el contrario, Jag1, un ligando de Notch, pero de expresión uniforme, limita el crecimiento de las CPM. Anatómicamente, la morfogénesis ductal y la arquitectura de los órganos se ven mínimamente perturbadas cuando existe mutación en Jag1 hasta etapas posteriores del desarrollo, cuando falla la remodelación ductal y aparecen signos de metaplasia acinar-ductal. De esta forma se revela que la actividad oscilante de la señalización mediada por Notch en el páncreas en desarrollo es necesaria para coordinar el crecimiento y el destino de las células progenitoras pancreáticas.
Señalización celular
La diabetes tipo 2 (DT2) se origina típicamente en personas con resistencia a la insulina inducida por la obesidad, pero la afección se manifiesta clínicamente como hiperglucemia debido a la disminución de la capacidad de las células beta para adaptarse mediante el aumento de la secreción de insulina. La hiperglucemia crónica se acompaña de un riesgo tanto micro como macrovascular. De esta forma, la DT2 es la principal causa de ceguera y de enfermedad renal en fase terminal y contribuye de manera desproporcionada a los acontecimientos cardiovasculares. Junto con los enormes costos económicos (estimados en uno de cada cuatro dólares de atención de salud), la DT2 reduce sustancialmente la expectativa de salud (es decir, el período de vida con buena salud) como la esperanza de vida.
A medida que la incidencia de obesidad aumenta, se buscan nuevas vías terapéuticas que regulan la adaptación de las células beta para evitar o mejorar la enfermedad. En consecuencia, las terapias dirigidas a las células beta actualmente disponibles aumentan secreción de insulina. Otros aspectos biológicos de las células beta que están afectadas por la DT2 incluyen la pérdida de la madurez, la disminución funcional, mientras que la alteración de interacciones entre células y célula estroma, aún no se comprende en su totalidad. Por lo tanto, el estudio de estos aspectos puede ser clave para desarrollar tratamientos más efectivos.
Notch - una proteína receptora llamada así por un defecto característico del ala en la mosca de la fruta con mutaciones en el gen Notch - media las decisiones del destino celular coordinando las interacciones entre las células vecinas que expresan receptores y ligandos cognados (de un mismo origen). En los mamíferos, hay cinco ligandos de superficie de proteínas Notch: Las familias Jag1 y Jag2 y las familias tipo-Delta (Dll1, Dll3 y Dll4), cada una de las cuales se une a uno de los cuatro receptores Notch (Notch1 a 4) en una célula vecina.
La unión de los ligandos da como resultado el clevaje del receptor Notch mediado por un complejo proteolítico llamado γ-secretasa, que luego inicia una vía que culmina con la activación de un regulador transcripcional, Hes1, que refina la señal de Notch. Varios estudios previos en ratones han demostrado que la actividad de Notch es crítica para el desarrollo normal del páncreas, aunque las interacciones entre cada uno de los componentes de la señal de Notch son extremadamente complejas y varían a lo largo de la pancreagénesis.
En trabajos recientes, Philip Allan Seymour y colaboradores de la Universidad de Copenhague han diseccionado cuidadosamente estos acontecimientos con una impresionante gama de modelos de ratones manipulados genéticamente. Durante el desarrollo del páncreas, las células progenitoras pancreáticas multipotencialess adoptan uno de varios destinos celulares: una célula progenitora bipotencial (con capacidad posterior para entrar en un linaje endocrino o ductal) o una célula proacinar comprometida con un linaje exocrino.
Las células exocrinas constituyen aproximadamente el 90% del volumen pancreático. De acuerdo con la literatura, los hallazgos de Seymour y sus colegas, muestran que estos puntos de decisiones sobre el linaje celular son catalizados por activación diferencial de Notch. Sin embargo, la verdadera novedad de este estudio se basa en el hallazgo de una fascinante interacción de dos diferentes ligandos de Notch (Dll1 y Jag1) para coordinar las oscilaciones ultradianas de la expresión de Hes1. Estos tipos de oscilaciones reflejan relojes biológicos que fluctúan con una periodicidad más corta (normalmente de 2 a 4 horas) que el más comúnmente apreciado ritmo circadiano de 24 horas. Estudios previos han demostrado que las oscilaciones ultradianas de Hes1 inducidas por Notch regulan aspectos de la diferenciación neural.
Varias vías canónicas y clínicamente relevantes también oscilan de esta manera.4 Por ejemplo, la respuesta inflamatoria al factor de necrosis tumoral α (TNF-α) - y presumiblemente las acciones antiinflamatorias de los antagonistas del TNF-α - depende de las oscilaciones del factor nuclear κB (NF-κB), mientras que otros estímulos inflamatorios (por ejemplo endotoxina bacteriana) no inducen las oscilaciones del NF-κB y, por lo tanto, conducen a la inducción de un programa de expresión génica alternativo.
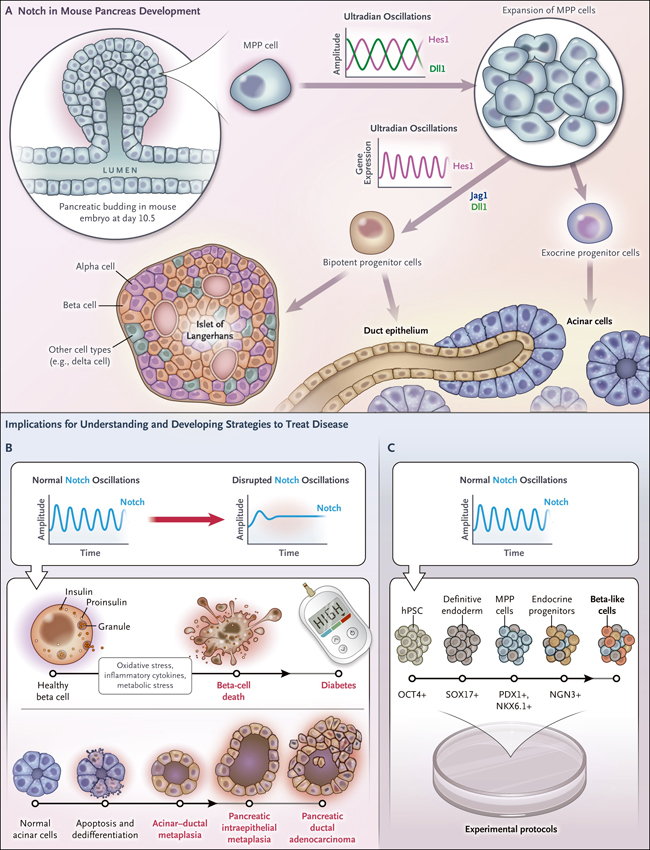
Figura 1 | Señalización de Notch durante el desarrollo del páncreas de ratón y posibles implicaciones clínicas.
El panel A muestra el desarrollo del páncreas del ratón en el día embrionario 10,5. Se requieren oscilaciones ultradianas recíprocas de Dll1 y Hes1 para promover la expansión de la población de células progenitoras pancreáticas multipotenciales (MPP). Dos días después, se requieren las funciones combinadas de Jag1, Dll1 y Hes1 oscilante para la diferenciación apropiada de la población de progenitores bipotenciales. En el recuadro B se muestran las consecuencias para los estudios en humanos. La interrupción de los componentes de señalización oscilante de Notch en las células beta adultas podría contribuir a su disfunción en personas con diabetes o iniciar la metaplasia acinar-ductal. El panel C muestra que en los protocolos experimentales para derivar células análogas a las células madre pluripotentes humanas (hPSC), la inducción de oscilaciones apropiadas en la señalización de Notch podría promover más eficazmente la diferenciación de los progenitores pancreáticos a los linajes de progenitores endocrinos.
En su estudio, Seymour y sus colegas demostraron que las oscilaciones de Dll1 y Hes1 son críticas para la adecuada expansión de los progenitores pancreáticos multipotenciales y que las oscilaciones de Hes1 influyen en la decisión del linaje de convertirse en un progenitor bipotencial o en una célula proacinar (figura 1A). Además, la eliminación de Jag1 en el páncreas en desarrollo provocó una alteración morfológica del conducto pancreático y la formación de estructuras que se asemejaban a la metaplasia acinarto-ductal.
Aunque la perturbación de la señalización de Notch se ha implicado en varios tipos de cáncer, queda por determinar si la alteración de la señalización oscilatoria de Notch contribuye a la formación de metaplasia acinar-ductal en el páncreas adulto. Sin embargo, como la reactivación de Notch se produce en el tejido epitelial pancreático metaplásico y neoplásico, es probable que las aberraciones en el flujo regulador a través de la vía de Notch contribuyan a la formación de tumores pancreáticos (figura 1B). Otra perspectiva planteada por estos estudios es que las oscilaciones en los componentes de señalización de Notch son importantes en las células beta maduras. Aunque se asumió que la actividad de Notch era inactiva en las células beta postnatales, trabajos recientes han demostrado que su actividad reactivada en la célula beta adulta contribuye a las alteraciones inducidas por la obesidad en la homeostasis de la glucosa.
La dilucidación de si la actividad oscilatoria de Notch es importante para las células beta adultas podría informar nuevas estrategias terapéuticas para la diabetes tipo 2 que se centren en el mantenimiento de la función celular. De manera similar, dado el papel recientemente demostrado de la señalización de Notch de los hepatocitos en la enfermedad de hígado graso no alcohólica, sería de potencial interés clínico determinar si las señales ultradianas regulan la actividad de Notch en el hígado y otros tejidos.
Aunque la mayoría de estos estudios se realizaron en ratones, la señalización de Notch también es necesaria para la diferenciación de las poblaciones de células madre pluripotentes humanas en un destino celular similar a las células beta (figura 1C). La capacidad de generar abundantes células productoras de insulina a partir de células madre pluripotentes humanas facilitaría las terapias de sustitución celular para los pacientes con diabetes.
Los inhibidores de Notch ya se están utilizando en estos protocolos, pero el estudio de Seymour y sus colegas sugiere que una comprensión más precisa de los matices de esta vía de señalización conduciría a una producción más eficiente de mejores células beta resistentes a la transdiferenciación en linajes no endocrinos. Por consiguiente, un mayor conocimiento de la señalización de Notch en las células madre pluripotentes humanas podría representar el avance crítico necesario para impulsar estas terapias a la clínica.
En conclusión, Seymour y colaboradores han aprovechado el poder de la genética animal para dilucidar el papel de las señales ultradianas de Notch en el control del desarrollo normal del páncreas. Dado el alcance de la señalización de Notch en la regulación de las decisiones sobre el destino de las células y sus funciones recientemente identificadas en los tejidos maduros, el legado de esta labor puede ser una mejor comprensión de los defectos pancreáticos asociados con una amplia gama de enfermedades metabólicas y neoplásicas.
Fuente bibliográfica
An Ultradian Notch in Beta-Cell Development
Utpal B. Pajvani, M.D., Ph.D., and Lori Sussel, Ph.D.
Department of Medicine and Institute of Human Nutrition, Columbia University, New York.
DOI: 10.1056/NEJMcibr2001628