Obesidad, inmunidad y cáncer
La obesidad está relacionada con el riesgo de padecer ciertos tipos de cáncer, como el de hígado y útero. Información actualizada proporciona algunas pistas del porqué.
La obesidad, que está aumentando hasta alcanzar proporciones epidémicas, está fuertemente asociada a mayor susceptibilidad a una serie de enfermedades. La diabetes y enfermedades cardiovasculares encabezan la lista, pero también se han puesto de manifiesto muchas más. Se reconoce que varios tipos de cáncer, como el de tiroides, útero e hígado, tienen una mayor incidencia o gravedad en las personas con obesidad. Aunque se ha demostrado que la dieta tiene efectos directos en la promoción del crecimiento tumoral, un vínculo clave entre la obesidad y cada una de estas enfermedades es el aumento de la inflamación crónica y los cambios en las poblaciones de células inmunitarias. Un estudio reciente de Ringel y colaboradores identifica las formas en que la inmunidad, tumores y microambientes tumorales cambian con la obesidad (figura 1).
La observación de que la obesidad puede promover inflamación fue comunicada por primera vez hace casi 30 años. Este hallazgo condujo al desarrollo del campo del inmunometabolismo, que busca comprender cómo el metabolismo sistémico y celular influye en la inmunidad e inflamación. Efectivamente, la obesidad y sus efectos sistémicos inducen cambios en las poblaciones de células T y macrófagos y promueven subconjuntos proinflamatorios de estas células. Además, los altos niveles de hormonas metabólicas que regulan la suficiencia o sobreabundancia de nutrientes, como la insulina y leptina, pueden promover estados inflamatorios en células T y macrófagos. Aunque este efecto es especialmente evidente en tejidos adiposos, la inflamación crónica e hiperlipidemia inducidas por obesidad actúan de forma sistémica y pueden exacerbar una amplia gama de enfermedades.
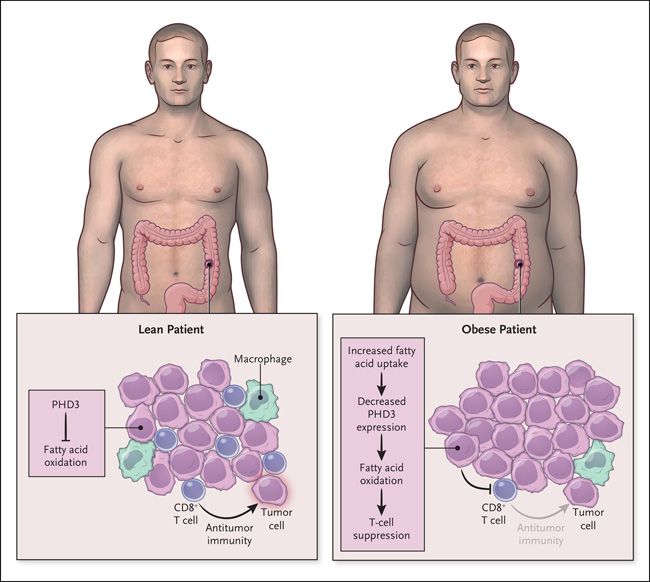
Figura 1: obesidad y microambiente inmunitario tumoral.
La obesidad modifica el metabolismo de las células cancerosas para perjudicar las funciones inflamatorias de las células T. La obesidad remodela el uso del combustible celular de los tumores para aumentar la oxidación de los ácidos grasos de las células cancerosas, al tiempo que reduce el número y posicionamiento espacial de las células T CD8+ para reducir la inmunidad antitumoral. Un enfoque "multiómico" mostró que PHD3 es un candidato para mediar estos efectos porque la disminución su expresión condujo a un mayor metabolismo de lípidos y la supresión de células T.
Se cree que el efecto de la obesidad sobre el cáncer y las células inmunitarias del microambiente tumoral es pleiotrópico. Por un lado, se definió el efecto Warburg de consumo y metabolismo elevados de la glucosa en las células cancerosas, pero también es utilizado por otros tipos de células prolifetivas; un programa metabólico similar para las células cancerosas e inmunitarias en el microambiente tumoral puede dar lugar a conflictos y competencia por nutrientes. La obesidad, sin embargo, es un escenario de abundancia de nutrientes, y las formas en que las células cancerosas y las células T se adaptan e interactúan con los nutrientes alterados, siguen siendo poco conocidos.
Dada la prevalencia de la obesidad y la incertidumbre sobre su efecto en el microambiente tumoral, Ringel y sus colegas han investigado la genética y fenotipos proteómicos, espaciales y metabólicos del cáncer y células inmunitarias en modelos animales de cánceres exacerbados por obesidad. La amplitud del enfoque, que incluye la generación de un atlas metabólico unicelular del paisaje inmunitario del tumor en contexto de obesidad, es un punto fuerte del estudio, que arrojo varios resultados claros. Los autores descubrieron que, aunque las células cancerosas adoptaron un metabolismo preferetemente basado en lípidos, las células T CD8+ eran menos abundantes, se desplazaban a fenotipos menos activados y fueron espacialmente excluidas de algunas regiones de los tumores. Un gen que destacó por estar selectivamente regulado a la baja en las células tumorales fue el PHD3, que codifica la prolilhidroxilasa-3. Es de interés que los experimentos con modelos de ratón mostraron que Phd3 regula la respuesta hipóxica y reprime la oxidación de los ácidos grasos; el rescate de la expresión de Phd3 en las células cancerosas restauró las funciones de las células T y relentizó el crecimiento del tumor. En consonancia con estos hallazgos, se observaron bajos niveles de PHD3 en muestras de tumores inmunológicamente "fríos" (tumores con bajo niveles de infiltrado inmunitario) en cinco de seis diferentes tipos de cáncer.
Este estudio plantea varias preguntas. Aunque las células T mostraron cambios sorprendentes en contexto de obesidad, las células mieloides aumentaron notablemente en el tejido adiposo de personas obesas y eran numerosas en tumores de animales obesos. Sin embargo, el papel de las células mieloides en la inmunosupresión inducida por obesidad, tal y como describen Ringel y colaboradores, sigue sin estar claro. Lo más importante es que aún no se han determinado las formas en que las vías descritas aquí influyen en la respuesta a la terapia y el papel más amplio de PHD3. Aunque han identificado un nuevo mecanismo por el que células cancerosas se adaptan metabólicamente para suprimir la función de las células T en la obesidad, otros datos apoyan la "paradoja de la obesidad", en que la obesidad puede sensibilizar a los tumores a la inmunoterapia. En ese escenario, se propone que el estado inflamatorio crónico de la obesidad prime una respuesta a la inmunoterapia, y que hormonas, como leptina, puedan desempeñar funciones proinflamatorias que, de otro modo, se mantienen bajo control.
A pesar de estas incógnitas, las consideraciones clínicas de estos hallazgos son múltiples a medida que vamos conociendo mejor el microambiente tumoral y el estado cada vez más prevalente de la obesidad. En términos generales, el enfoque "multiómico" proporcionará material para guiar estudios futuros que irán mucho más allá de estos resultados iniciales. De forma más directa, la regulación positiva de la vía PHD3 puede proporcionar una nueva diana terapéutica para frenar el crecimiento del tumor en pacientes obesos o, alternativamente, para potenciar los efectos de la inmunoterapia en pacientes no obesos.
El pefecto de las intervenciones dietéticas, como una dieta baja en grasas y carbohidratos, también se ha considerado ampliamente en el cáncer. El estudio de Ringel y colaboradores utilizó una dieta alta en grasas para proporcionar una nueva dirección y evidencias sobre cómo la sobrealimentación puede suprimir selectivamente las células T asociadas al tumor.
El papel relativo del metabolismo tumoral y PHD3 para suprimir directamente las células T dentro de tumores mientras sensibilizan la inmunidad antitumoral a través de un estado basal de bajos niveles de inflamación y altos niveles de leptina forma claramente una mezcla compleja. Dicho esto, la creciente comprensión de los efectos de la obesidad y la dieta en el microambiente tumoral está dando lugar a nuevos objetivos y enfoques para abordar la incidencia, progresión y tratamientos de los numerosos cánceres exacerbados por la epidemia de obesidad.
Fuente bibliográfica
Obesity, Immunity, and Cancer
Jeffrey C. Rathmell, Ph.D.
Vanderbilt Center for Immunobiology, Vanderbilt Ingram Cancer Center, Department of Pathology, Microbiology, and Immunology, Vanderbilt University Medical Center, Nashville.
N Engl J Med 2021; 384:1160-1162