Cerrando el círculo sobre inflamación, enfermedades y cáncer
La hematopoyesis clonal de potencial indeterminado (CHIP, por sus siglas en inglés) es relativamente común en personas mayores y es un factor de riesgo de enfermedades sanguíneas malignas y cardiovasculares. Un estudio reciente de un modelo de pez cebra proporciona información sobre cómo puede evolucionar la CHIP y la presencia de un ciclo de retroalimentación positiva.
El cáncer es causado por una mutación en una sola célula que inicia la proliferación seguida de la acumulación de mutaciones adicionales. Múltiples factores influyen en la frecuencia con la que ocurren las mutaciones iniciales y subsiguientes, y la propensión de una célula que ha adquirido una mutación a expandirse clonalmente. Estos incluyen la genética, efectos ambientales y características intrínsecas como la edad, obesidad, resistencia a la insulina y la inflamación.
Las excrecencias clonales premalignas de células se pueden distinguir en órganos que se biopsian fácilmente. En el cáncer colorrectal, por ejemplo, la mutación iniciadora da como resultado pólipos adenomatosos premalignos, de los cuales solo una fracción progresa a malignidad. En el sistema sanguíneo, los crecimientos clonales se identifican con el uso de enfoques basados en la secuenciación del ADN. Los crecimientos clonales en personas con características hematológicas normales se denomina hematopoyesis clonal de potencial indeterminado (CHIP) o hematopoyesis clonal relacionada con la edad. La CHIP se genera por una mutación en una célula madre hematopoyética (HSC) en la médula ósea que hace que las HSC mutadas aumenten en número en relación con sus contrapartes normales. El grado en que una HSC mutada se expande en la médula ósea se estima a partir de la fracción de ADN en la sangre periférica que contiene la mutación, la llamada frecuencia alélica variante (VAF). La prevalencia de CHIP (definida por una VAF ≥2%) aumenta con la edad; está presente en menos del 2 % de los individuos menores de 50 años, pero la persona promedio de 70 años tiene una probabilidad del 10 al 20% de tener una expansión clonal de lo que originalmente era una HSC única.
La CHIP eleva el riesgo de un cáncer de sangre, pero la mayoría de las HSC premalignas no progresarán a malignidad. La CHIP también aumenta el peligro de enfermedad cardiovascular y accidente cerebrovascular, porque las células sanguíneas maduras que contienen mutaciones inductoras de CHIP son más inflamatorias que las que se diferencian de las HSC no mutadas. El hallazgo de que una mutación inductora de CHIP introducida únicamente en las células mieloides resultó en una enfermedad cardiovascular en ratones propensos a la aterosclerosis respalda la probabilidad de que las unidades mieloides mutadas sean las principales culpables.
La inflamación también es un factor de riesgo bien conocido para el cáncer. Sin embargo, lo que no está claro es si el aumento de las propiedades inflamatorias de las células mutadas podría impulsar la expansión clonal de las células premalignas. Una reciente investigación muestra que este es el caso: las mutaciones que inducen la CHIP en las HSC incrementan las propiedades inflamatorias de las células mieloides que se diferencian de ellas y, al mismo tiempo, hacen que las HSC mutantes sean más resistentes a los efectos nocivos de las moléculas inflamatorias producidas por células mieloides que suprimen el crecimiento de HSC normales (no mutantes).
Los autores utilizaron un modelo de pez cebra en el que se diseñaron HSC para expresar diferentes colores de proteínas fluorescentes, lo que permitió identificar HSC individuales y su progenie clonal. Las células sanguíneas que se diferenciaron de estas HSC multicolores produjeron frotis de sangre espectacularmente coloridos. Los investigadores introdujeron mutaciones inductoras de CHIP conocidas en el grupo de HSC multicolores y observaron que una alteración en una sola HSC podría hacer que se expandiera clonalmente, lo que daría como resultado una cantidad desproporcionada de células sanguíneas de un solo color. Se confirmó que las células mieloides (granulocitos y macrófagos) que se habían diferenciado de las HSC mutadas habían aumentado la expresión de citocinas inflamatorias. Luego, los investigadores hicieron una pregunta simple pero fundamental: ¿qué tenían las mutaciones inductoras de CHIP que permitieron que las HSC se expandieran preferentemente en relación con sus contrapartes no mutadas? Encontraron que las HSC mutadas habían regulado al alza la expresión de genes antiinflamatorios, lo que, según la hipótesis de los investigadores, protegía a las HSC de los efectos nocivos del exceso de citocinas inflamatorias producidas a partir de las células mieloides mutadas. En un experimento clave, los investigadores probaron esta hipótesis eliminando genéticamente la respuesta antiinflamatoria de las HSC mutadas mediante la eliminación de uno de los genes antiinflamatorios (Nr4a1) y mostrando que estas células ya no podían expandirse en grandes clones de células (figura 1). Los resultados de este estudio sugieren que a medida que se expande un clon de HSC mutadas, la proporción de células mieloides inflamatorias en la médula ósea aumenta al mismo tiempo, lo que impulsa la expansión preferencial de las HSC mutadas al reprimir selectivamente el crecimiento de las HSC normales. ¡Un ciclo pernicioso de hecho!
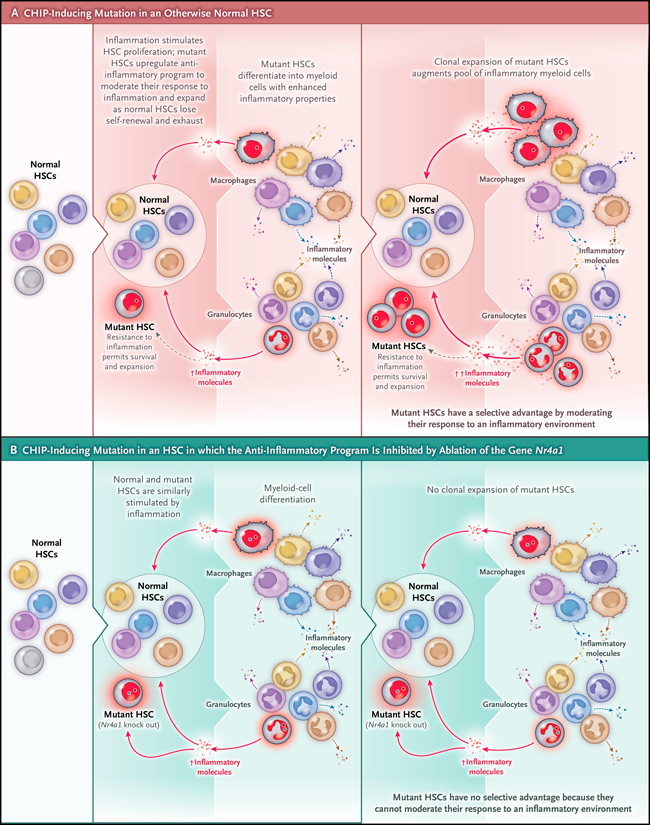
Figura 1: expansión clonal de HSC con promotores inductores de CHIP y resistencia a citocinas inflamatorias.
Se introdujeron mutaciones que inducían hematopoyesis clonal de potencial indeterminado (CHIP) en un grupo de células madre hematopoyéticas (HSC) marcadas individualmente con varios colores fluorescentes (panel A). Las células mieloides derivadas de las HSC mutadas produjeron mayores cantidades de citocinas inflamatorias, que a su vez reprimían el crecimiento de las HSC normales. Las HSC mutantes eran resistentes a los efectos nocivos de las moléculas inflamatorias y, por lo tanto, tenían una ventaja selectiva que conducía a la expansión clonal en la médula ósea y a una cantidad desproporcionada de células sanguíneas de un solo color. La ablación del programa antiinflamatorio mediante la eliminación de uno de los genes regulados al alza, Nr4a1, impidió la expansión selectiva de las HSC con la mutación inductora de CHIP (panel B).
Reducir la inflamación podría aminorar potencialmente el riesgo de enfermedad cardiovascular, accidente cerebrovascular y leucemia en personas con hematopoyesis clonal de potencial indeterminado. Los datos clínicos en estudios de cáncer de pulmón respaldan esta noción. El estudio de resultados de trombosis antiinflamatoria de canakinumab de fase 3 (CANTOS), diseñado para determinar si la incidencia de eventos cardiovasculares en pacientes con una respuesta proinflamatoria persistente podría reducirse mediante el tratamiento con canakinumab, un inhibidor de IL-1β mostró por casualidad que la incidencia de pulmonar el cáncer se reducía sustancialmente entre pacientes que recibieron canakinumab. Sin embargo, el anterior estudio sugiere que otra estrategia para reducir la expansión clonal de las HSC portadoras de mutaciones inductoras de CHIP y las secuelas posteriores es socavar la resistencia de las HSC mutantes a los efectos nocivos de la inflamación crónica, lo que las privaría de su ventaja competitiva sobre los HSC normales. Identificar fármacos que puedan hacer esto es el próximo problema para abordar.
Fuente bibliográfica
A Pernicious Cycle Affecting Premalignant Stem Cells
Nancy A. Speck,
Department of Cell and Developmental Biology, Perelman School of Medicine, University of Pennsylvania, Philadelphia.
N Engl J Med 2022; 386:596-598