Terapia génica restaura función inmunológica en niños con deficiencia de ADA
Los investigadores encontraron que 48 de 50 pacientes mantuvieron el desempeño de su sistema inmunológico dos a tres años después, y no requirieron tratamientos adicionales para su condición.
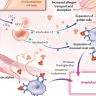
La inmunodeficiencia combinada grave debida al déficit de adenosina desaminasa (ADA) (ADA-SCID) es un error innato del metabolismo que provoca la acumulación de adenosina y desoxiadenosina, inhibición de la síntesis y reparación del ADN, así como importantes anomalías del desarrollo de los timocitos. Los pacientes con ADA-SCID tienen linfocitopenia profunda, función inmune deteriorada y retraso en el crecimiento y, sin tratamiento, mueren por infecciones a la edad de 2 años.
En este estudio, D.B. Kohn y colegas de la Universidad de California, evaluaron la seguridad y eficacia de una terapia génica con vectores lentivirales compuesta de células madre/progenitoras hematopoyéticas CD34+ (HSPC) que habían sido modificadas genéticamente ex vivo con EFS-ADA LV. Se trataron a 50 pacientes con ADA-SCID (30 de Estados Unidos y 20 del Reino Unido) y luego se analizaron los datos a partir de dos estudios norteamericanos (con formulaciones frescas y crioconservadas) a los 24 meses de seguimiento junto con otro ensayo del Reino Unido (con una nueva formulación) a los 36 meses de seguimiento.
La supervivencia general fue del 100% en todos los estudios hasta los 24 y 36 meses. La supervivencia sin eventos (en ausencia de reinicio de la terapia de reemplazo enzimático o de rescate con trasplante alogénico de células madre hematopoyéticas) fue del 97% (estudios de EE. UU.) y del 100% (estudio del Reino Unido) a los 12 meses; 97% y 95%, respectivamente, a los 24 meses; y del 95% (estudio del Reino Unido) a los 36 meses. El injerto de células HSPC modificadas genéticamente persistió en 29 de 30 pacientes en los estudios de EE. UU. y en 19 de 20 pacientes en el estudio de Reino Unido. Los pacientes presentaron una desintoxicación metabólica sostenida y una normalización de los niveles de actividad ADA. La reconstitución inmunitaria fue sólida: el 90% de los niños en los estudios de EE. UU. y el 100% del estudio del Reino Unido interrumpieron la terapia de reemplazo de inmunoglobulinas a los 24 y 36 meses, respectivamente. No se observaron evidencias de expansión monoclonal, complicaciones leucoproliferativas o aparición de lentivirus con capacidad de replicación, y no se produjeron eventos de autoinmunidad o enfermedad de injerto contra el huésped. La mayoría de los eventos adversos fueron de bajo grado.
Finalmente, el tratamiento de la ADA-SCID con terapia génica lentiviral HSPC ex vivo dio como resultado una alta supervivencia general, con expresión sostenida de ADA, corrección metabólica y reconstitución inmune funcional.