ProteĂnas chaperonas y medicina personalizada
Los efectos de una mutaciĂłn genĂŠtica causante de enfermedad pueden diferir entre individuos debido a diferencias genĂŠticas o a los diferentes entornos en que se encuentran las personas. Por ejemplo, cientos de mutaciones pueden causar anemia de Fanconi, una deficiencia de cĂŠlulas sanguĂneas que predispone al cĂĄncer. Sin embargo, el ser portador de la mutaciĂłn es un muy pobre predictor de si desarrollarĂĄ la versiĂłn leve o grave de la patologĂa. La comprensiĂłn sobre cĂłmo el contexto altera los resultados de esta manera se encuentra en el epicentro de la medicina personalizada. Dos recientes estudios (Cell 168, 856â866 (2017); Nature Struct. Mol. Biol. 24, 234â242 2017) proporcionan mecanismos convincentes por los cuales la proteĂna de choque tĂŠrmico 90 (HSP90) altera los resultados relacionados con las diferencias genĂŠticas. Sin embargo, sigue siendo desconocido si HSP90 influye en las consecuencias de las mutaciones en humanos, lo que podrĂa modificar el curso clĂnico de las enfermedades genĂŠticas.
ProteĂna de choque
HSP90 es una chaperona molecular que mantiene la integridad estructural de la las proteĂnas de seĂąalizaciĂłn celular. Los experimentos en moscas de la fruta hace casi 20 aĂąos atrĂĄs mostraron que la alteraciĂłn de la funciĂłn de HSP90 genera diversos resultados que son especĂficos de cada cepa, entre ellos defectos de los ojos en una cepa y alteraciones en las alas en otra cepa. Estudios posteriores en otros animales, plantas y hongos dieron resultados similares, lo que apoya la idea de que HSP90 modula las consecuencias de la variaciĂłn genĂŠtica en muchas especies, probablemente incluyendo a humanos. Pero cĂłmo funciona exactamente este mecanismo de HSP90 ha sido objeto de especulaciones y debates.
En el primero de los estudios, Karras y colegas (Cell. 2017 Feb 23;168(5):856-866) demostraron que HSP90 altera los efectos de las mutaciones genĂŠticas en humanos mediante la interacciĂłn directa con proteĂnas mutantes. Los autores estudiaron las mutaciones en FANCA, el gen comĂşnmente mutado en personas que tienen anemia de Fanconi. Las cĂŠlulas de estos pacientes son generalmente hipersensibles al daĂąo inducido al ADN por el agente mitomicina C. Debido a que la proteĂna FANCA participa en la reparaciĂłn del daĂąo al material genĂŠtico, mitomicina C se puede utilizar para diagnosticar la anemia de Fanconi y para medir cĂłmo una mutaciĂłn interrumpe la funciĂłn celular.
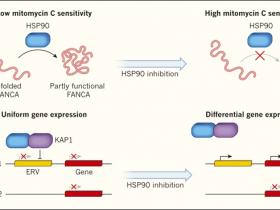
Karras y sus colegas encontraron que las proteĂnas FANCA mutantes muestran una mayor asociaciĂłn con HSP90 en comparaciĂłn a otras proteĂnas, y que, en general, estas proteĂnas mutantes se vinculaban con una alteraciĂłn menos grave de la funciĂłn celular. La inhibiciĂłn de HSP90 aumentĂł la susceptibilidad a mitomicina C por parte de las cĂŠlulas que producen mutantes FANCA, confirmando un mecanismo propuesto previamente acerca de HSP90. Conforme a esta hipĂłtesis, la chaperona estabiliza las proteĂnas defectuosas, permitiendo su plegamiento en una conformaciĂłn normal que les permite funcionar parcialmente (figura 1a). Notablemente, el efecto de la inhibiciĂłn de HSP90 en la sensibilidad a mitomicina C podrĂa ser imitado por un incremento de la temperatura - un estresor ambiental que afecta la funciĂłn de HSP90 y  que podrĂa ser experimentado si un paciente tiene fiebre. Por lo tanto, la capacidad de FANCA de interactuar con HSP90 puede influir en el curso de la enfermedad, y depende de un contexto genĂŠtico y ambiental.
En el segundo estudio, Hummel y colaboradores (Nature Struct. Mol. Biol. 24, 234â242 (2017)) mostraron un rol modulador de HSP90 sobre los efectos de retrovirus endĂłgenos (ERV) -secuencias de ADN derivadas de virus que insertan copias de su propio material genĂŠtico en las cĂŠlulas del hospedador. Los ERV pueden aumentar en nĂşmero en un genoma hospedero mediante reinfecciĂłn o mediante replicaciĂłn en cĂŠlulas sexuales, e incluso dan cuentas de aproximadamente el 5-10% de los genomas en humanos y en ratones. La presencia o ausencia de algunas inserciones de ERV difiere entre las personas y entre los ratones.
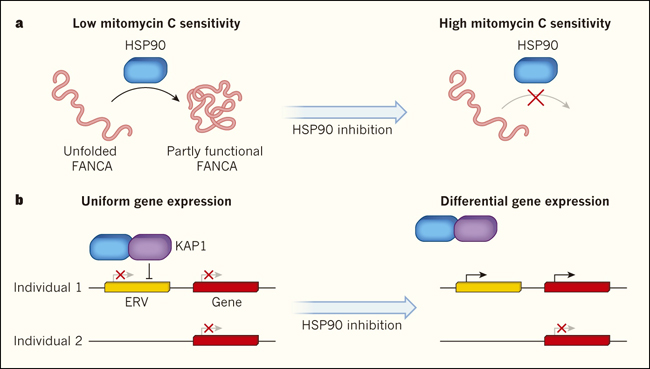
Figura 1: la proteĂna de choque tĂŠrmico 90 (HSP90) altera los efectos de las diferencias genĂŠticas.
HSP90 es una chaperona molecular que se une y estabiliza a otras proteĂnas. Mutaciones en la proteĂna FANCA causa el sĂndrome de la anemia de Fanconi. Karras y colegas mostraron que algunas proteĂnas FANCA mutadas interactĂşan fuertemente con HSP90. La proteĂna puede plegarse en formas normales y parcialmente funcionales, lo que implica que las cĂŠlulas que las albergan no pueden ser eliminadas por el fĂĄrmaco mitomicina C. La inhibiciĂłn de HSP90 (farmacolĂłgicamente o aumentando la temperatura) impide las interacciones normales de HSP90 con FANCA, lo que vuelve a las cĂŠlulas susceptibles a mitomicina C. b, secuencias de ADN llamadas retrovirus endĂłgenos (ERV) se insertan en todo el genoma, en sitios que difieren entre individuos. Hummel y colegas reportaron que HSP90 actĂşa con la proteĂna KAP1 para silenciar la transcripciĂłn de ERV, lo que normalmente activa los genes adyacentes. Por lo tanto, la presencia o ausencia de ERV cerca de genes que normalmente estĂĄn silenciados no tiene ningĂşn efecto sobre la expresiĂłn de estos genes en condiciones normales. La inhibiciĂłn de HSP90 conduce a diferentes patrones de actividad de esos genes.
La transcripciĂłn de ERV puede estimular la actividad de genes adyacentes. Hummel y sus colegas perfilaron patrones de expresiĂłn de genes en tres tipos de cĂŠlulas de ratĂłn despuĂŠs de la inhibiciĂłn de HSP90, lo cual revelĂł que HSP90 contrarresta esta tendencia activadora. Los investigadores demostraron que HSP90 interactĂşa con la proteĂna KAP1, la que dirige la deposiciĂłn de modificaciones moleculares represivas sobre el ADN de ERV para prevenir la transcripciĂłn. La inhibiciĂłn de HSP90 previene la represiĂłn de ERV mediada por KAP1.
Por lo tanto, los autores propusieron que la actividad de HSP90 permite la acumulaciĂłn de diferentes inserciones de ERV en individuos distintos. Estas diferencias de inserciĂłn serĂan intrascendentes bajo condiciones normales, pero podrĂan llevar a diversos resultados en momentos de estrĂŠs (figura 1b). Si esto es aplicable tambiĂŠn en humanos, serĂa previsible que la presentaciĂłn clĂnica de la enfermedad sea dramĂĄticamente diferente con las variaciones de inserciĂłn de ERV entre los individuos.
Estos dos estudios se suman a una creciente literatura que establece la abundancia de la variaciĂłn genĂŠtica crĂptica, lo cual no tiene efecto bajo condiciones normales, pero que se esconde en las poblaciones hasta que otras mutaciones o perturbaciones ambientales las revelen. HSP90 no sĂłlo suprime los efectos de las diferencias genĂŠticas, sino que puede tambiĂŠn provocar que proteĂnas mutantes adopten nuevas funciones, potenciando las diferencias. De manera similar, la represiĂłn de ERV mediada por HSP90 podrĂa potenciar, en lugar de suprimir, las diferencias de rasgos. Por ejemplo, si un ERV se ha insertado junto a un gen que debe ser activado, HSP90 podrĂa silenciar el gen en su lugar.
Finalmente, aĂşn se desconoce si en seres humanos HSP90 influye en las consecuencias de las mutaciones, lo que podrĂa modificar el curso clĂnico de las enfermedades genĂŠticas. Estos hallazgos proporcionan un mecanismo plausible para la expresividad variable y la sensibilidad ambiental de las enfermedades genĂŠticas.
Fuente bibliográfica
Molecular genetics: Chaperone protein gets personal
Mark L. Siegal
Center for Genomics and Systems Biology, Department of Biology, New York University.
doi:10.1038/nature22487