Nuevos blancos moleculares contra patologĂas
Las quimioquinas y sus receptores acoplados a proteĂna G juegan un papel diverso en las respuestas inmunitarias al controlar la migraciĂłn, activaciĂłn y supervivencia celular. TambiĂ©n están implicados en el ingreso de particulas virales, el crecimiento tumoral y metástasis, por lo tanto, son blancos importantes para el diseño de fármacos para una amplia gama de enfermedades. A pesar de los significativos esfuerzos de la industria farmacĂ©utica en el desarrollo de medicamentos dirigidos a esos receptores, sĂłlo dos compuestos se encuentran disponibles: maraviroc antagonista de CCR5 para la infecciĂłn por VIH y plerixafor, antagonista de CXCR4 para la movilizaciĂłn de cĂ©lulas madre. Sin embargo aĂşn existe una limitada comprensiĂłn del mecanismo de acciĂłn de los antagonistas de receptores de quimioquinas y una incapacidad para optimizar los compuestos en ausencia de informaciĂłn estructural.
Receptores celulares
Una familia de proteĂnas de membrana conocidas como receptores acoplados a proteĂna G, median un tipo de comunicaciĂłn celular basada en la transducciĂłn de señales transmembrana. Un subconjunto de esta familia, los receptores de quimioquinas, regulan la migraciĂłn celular y su activaciĂłn se ha vinculado con una serie de enfermedades,incluyendo trastornos inmunolĂłgicos y cáncer. Pero encontrar fármacos que inhiban estos receptores ha sido desafiante. Dos recientes estudios describen las estructuras cristalinas de dos receptores de quimioquinas en complejo con molĂ©culas pequeñas inhibidoras. Estos antagonistas se unen a los bolsillos cercanos a la parte intracelular de los receptores apuntando a un camino no identificado que puede ser el punto de partida para el descubrimiento de un nuevo medicamento.
La mayorĂa de las molĂ©culas de fármacos que se dirigen a receptores asociados proteĂna G (GPCR) imitan la actividad de uniĂłn de un activador nativo, potenciando o  inhibiendo la señalizaciĂłn del receptor para lograr un efecto terapĂ©utico. Los fármacos normalmente ocupan un bolsillo de denominado sitio ortostĂ©rico en la regiĂłn transmembrana del receptor que es accesible al exterior de la cĂ©lula. Pero la afinidad con la que los ligandos activadores se unen a receptores puede aumentarse por la uniĂłn de proteĂna G. Este fenĂłmeno, conocido como efecto alostĂ©rico, está bien establecido en la farmacologĂa de la GPCR y proporciona una alternativa para el descubrimiento de fármacos.
A diferencia de las proteĂnas G, que se unen al lado intracelular del receptor, Lado del receptor, otras molĂ©culas alostĂ©ricas tienden a unirse a sitios que están dentro la regiĂłn de la membrana o en la regiĂłn extracelular, incluso superpuestas al bolsillo ortostĂ©rico. Sin embargo, algunos fármacos candidatos y anticuerpos parecen unirse a la regiĂłn citoplasmática de los GPCR (incluyendo a receptores de quimioquinas) y afectan la funciĂłn. Hasta ahora, aĂşn no se ha descrito en detalle algĂşn fármaco alostĂ©rico que se una a la superficie citoplasmática de un GPCR.
En un primer estudio, Christine Oswald y colaboradores (Nature. 2016 Dec 15;540(7633):462-465) mostraron la estructura cristalina del receptor de quimioquinas CCR9 en complejo con una molécula pequeña llamado vercirnon, que actúa como antagonista frente a la actividad de CCR9 (figura 1a). La inhibición de CCR9 es una forma deseable de tratar la enfermedad inflamatoria intestinal, pero vercirnon no ha pasado de estudios de fase III en personas con enfermedad de Crohn. La cristalización del complejo CCR9-vercirnon requiere el uso de una variante de CCR9 con ocho sustituciones de aminoácidos y el truncamiento de los extremos amino y carboxilo, pero los autores confirmaron que ninguno de estos cambios afecta la unión de vercirnon.
La estructura revela los siete segmentos helicoidales transmembrana de CCR9 conectados por tres bucles citoplasmáticos, con una octava hélice que parece descansar sobre la región intracelular de la membrana. Vercirnon posee una estructura asimétrica, con forma de V invertida que se une en un bolsillo que comprende cinco de las siete hélices, y mira se orienta hacia fuera directamente en el citoplasma. Su sitio de unión está a unos 33 ångströms del supuesto bolsillo ortostérico, que se encuentra hacia la superficie extracelular de las siete hélices.
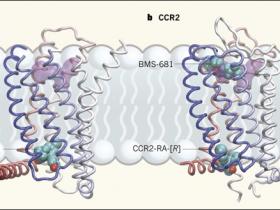
En el segundo estudio (Nature. 2016 Dec 15;540(7633):458-461),  Yi Zheng y colaboradores muestran la estructura de CCR2 - que ha vinculado con varias enfermedades inflamatorias y trastornos autoinmunes y en la actividad antitumoral- en complejo simultáneo con dos molĂ©culas pequeñas antagonistas CCR2 - RA- [R] y BMS - 681 (figura 1b). Los autores lograron la cristalizaciĂłn truncando el extremo carboxi-terminal de CCR2, y mediante la fusiĂłn de una proteĂna estabilizante llamada lisozima T4 en un tercer bucle citoplásmico alterado, que es una estrategia comĂşn para facilitar la cristalizaciĂłn de GPCR.
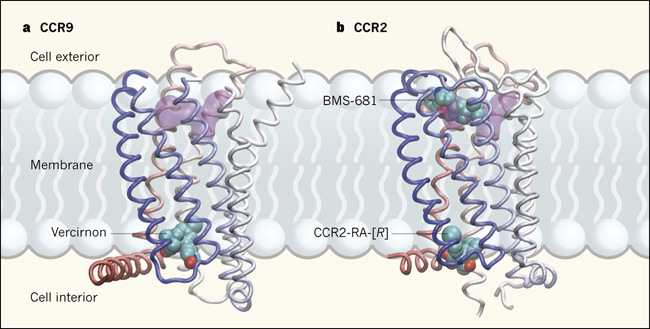
Figura 1: Visualización de la inhibición alostérica.
Dos estudios proveen dan a conocer las estructuras de las proteĂnas receptoras de quimioquinas en complejo con molĂ©culas pequeñas antagonistas que inhiben la actividad del receptor. En ambas estructuras, el receptor comprende siete dominios helicoidales transmembrana y una octava hĂ©lice localizada a lo largo de la regiĂłn citoplásmica de la membrana (diferentes dominios indicados por el cambio gradual de colores, de azul y blanco a rosado).A, Oswald y sus colegas reportan que la molĂ©cula pequeña vercirnon se une en un bolsillo en el lado intracelular del CCR9. El sitio de uniĂłn para el fármaco maraviroc en otro receptor de quimioquina, CCR5, se muestra en pĂşrpura para la comparaciĂłn. B, Zheng y colaboradores muestran la estructura de CCR2 en complejo simultáneo con dos diferentes antagonistas: BMS-681, que se une en un bolsillo que se superpone con el sitio de uniĂłn a maraviroc, y CCR2-RA- [R], que se une en un bolsillo intracelular casi idĂ©ntico al de CCR9.
BMS-681 se une en un bolsillo que se superpone con el supuesto sitio de uniĂłn ortostĂ©rico cerca de la superficie extracelular de CCR2, mientras que CCR2-RA- [R] se une en un sitio como el bolsillo alostĂ©rico de CCR9. La uniĂłn simultánea de los antagonistas provoca que CCR2 adopte una conformaciĂłn que parece estar completamente inactiva. Aunque vercirnon y CCR2-RA- [R] son diferentes entidades quĂmicas, ocupan sitios de uniĂłn que se encuentran en la misma ubicaciĂłn y poseen un revestimiento tridimensional formado por aminoácidos de las hĂ©lices 1, 2, 3, 6 y 7. Estas semejanzas indican que el sitio alostĂ©roco alostĂ©rico podrĂa estar presente en receptores de quimioquinas. Si esta suposiciĂłn es verdadera, se facilitarĂa el diseño de fármacos que se unan a estos sitios. Vercirnon, por ejemplo, no está optimizado para el bolsillo del CCR9, y es probable que algunas modificaciones menores pudiesen mejorar sus propiedades farmacolĂłgicas.
Las estructuras tambiĂ©n proporcionan pistas acerca de los mecanismos de antagonismo alostĂ©rico intracelular. Los antagonistas unidos previenen el movimiento hacia fuera y la rotaciĂłn de las hĂ©lices (especialmente la hĂ©lice 6), que es el sello distintivo de la estructura del estado activo. Particularmente en la estructura CCR9-vercirnon, en la que los loops citoplasmáticos no se modifican para la cristalizaciĂłn y están razonablemente bien resueltos, está claro que vercirnon ocupa un espacio que normalmente se llenarĂa con el extremo carboxi terminal de una proteĂna G unida durante la activaciĂłn del receptor. La uniĂłn por la proteĂna beta - arrestina, que inhibe la señalizaciĂłn y provoca la internalizaciĂłn del receptor, tambiĂ©n "chocarĂa" con la uniĂłn de vercirnon.
Sin duda que el progreso en el desarrollo de molĂ©culas pequeñas candidatos a fármacos para los receptores de quimioquinas es un camino lento. Ha habido sĂłlo dos Ă©xitos: el fármaco maraviroc, que media la inhibiciĂłn de CCR5 para prevenir el ingreso del VIH-1 a las cĂ©lulas y plerixafor, que apunta a CXCR4 para movilizar las cĂ©lulas madre de la mĂ©dula Ăłsea para trasplantes en personas con cáncer. Otra docena de receptores de quimioquinas son objetivos para el desarrollo de fármacos para enfermedades que van desde trastornos autoinmunitarios hasta las metástasis del cáncer. El sitio intracelular identificado en los estudios actuales podrĂa proporcionar una nueva estrategia para inhibir estos receptores, convirtiendo el descubrimiento de nuevos fármacos en un esfuerzo realizado de adentro hacia afuera de la cĂ©lula.
Fuente bibliográfica
Pharmacology: Inside-out receptor inhibition
Thomas P. Sakmar & Thomas Huber
Laboratory of Chemical Biology and Signal Transduction, The Rockefeller University, New York, New York 10065, USA.
doi:10.1038/nature20486