NanopartĂculas y ayuda antiviral contra el cáncer
Los Ăłrganos linfoides, en los que las cĂ©lulas presentadoras de antĂgenos (APC) están en estrecha proximidad a las cĂ©lulas T, son el microambiente ideal para la potenciaciĂłn y amplificaciĂłn de las respuestas de este tipo celular. Sin embargo, la administraciĂłn sistĂ©mica de vacunas contra antĂgenos tumorales para activar cĂ©lulas dendrĂticas se ve obstaculizada por varios retos tĂ©cnicos. Recientes investigaciones realizadas en ratones y en tres pacientes, muestran que esto puede ser logrado con precisiĂłn y eficacia mediante la administraciĂłn intravenosa de un complejo nanomolecular formado por lĂpidos y ARN, sin la necesidad de partĂculas como anticuerpos o ligandos adicionales. El ARN recubierto y protegido por la estructura lipĂdica, codifica antĂgenos tumorales capaces de estimular a las cĂ©lulas presentadoras de antĂgeno, simulando además las vĂas activadas mediante el transcurso de una infecciĂłn viral al impulsar a linfocitos T CD8 a ejercer su actividad citotĂłxica. Esta respuesta sumada a la producciĂłn y secreciĂłn de interferĂłn, constituye un enfoque promisorio para estudios clĂnicos más amplios que otorguen resultados positivos para la lucha contra el cáncer.
Vacuna antitumoral
Las vacunas preventivas son quizás la forma más eficaz de inmunoterapia. Sin embargo en un artĂculo reciente liderado por Lena M. Kranz, se describiĂł una estrategia de vacunaciĂłn contra el cáncer dirigida a tumores preexistentes mediante el reclutamiento de mecanismos que usualmente son usados durante el transcurso de una infecciĂłn viral. Los investigadores emplearon nanopartĂculas en cuyo interior llevan ARN tumoral para simular la intrusiĂłn de un patĂłgeno viral en el torrente sanguĂneo. Cuando las nanopartĂculas alcanzan los tejidos linfoides, como el bazo y los ganglios, activan los mecanismos de defensa antivirales en componentes del sistema inmunolĂłgicotales, como las cĂ©lulas dendrĂticas (CD). Estas cĂ©lulas, traducen el ARN proveniente de las nanopartĂculas para expresar y presentar antĂgenos tumorales (molĂ©culas utilizadas durante una respuesta inmunitaria como objetivos de ataque) a los linfocitos T, estimulando a estas cĂ©lulas para iniciar una respuesta antitumoral.
ÂżPor quĂ© es tan difĂcil obtener una vacuna efectiva contra el cáncer? Una razĂłn es que las cĂ©lulas cancerosas son similares en muchos aspectos a las normales y el sistema inmunitario evita atacar lo propio. Ăšnicamente se han alcanzado respuestas relativamente modestas con las vacunas que contienen antĂgenos tambiĂ©n expresados en tejidos sanos. Una respuesta de mayor intensidad solamente puede esperarse cuando las cĂ©lulas tumorales expresan antĂgenos que no son usualmente producidos en las cĂ©lulas adultas normales.
Otra razĂłn es que el crecimiento cancerĂgeno no se acompaña de fuertes señales inflamatorias, tales como las que ocurren durante una infecciĂłn microbiana, las que estimulan una fuerte respuesta inmune. Esto conduce a microambientes tumorales en los que las cĂ©lulas de defensa toleran, o incluso promueven, el crecimiento del tumor. Por lo tanto, las vacunas antitumorales deben trabajar cuando la enfermedad ya se ha afianzado, y a menudo, cuando se ha extendido por todo el cuerpo. Por Ăşltimo, y en un contraste clave para las vacunaciones preventivas contra los virus, la mayorĂa de los cánceres coexisten y han coevolucionado junto a nuestro sistema inmunolĂłgico a lo largo de los años, resultando en un microambiente tumoral inmunosuprimido que añade un obstáculo extra para la inmunoterapia.
En los enfoques vacunales contra una amplia gama de enfermedades, las cĂ©lulas presentadoras de antĂgeno (CPA) especializadas poseen un papel fundamental. Particularmente, las cĂ©lulas dendrĂticas están extremadamente bien adaptadas para el procesamiento y presentaciĂłn de antĂgenos para activar a los linfocitos T. Las CD de cultivo cargadas con antĂgenos bajo condiciones in vitro, pueden aumentar la inmunidad cuando se administran a pacientes con cáncer, pero hasta ahora la eficacia clĂnica de esta estrategia ha sido limitada. La mayorĂa de estas vacunas utilizan CD derivadas de un tipo particular de glĂłbulos blancos de la sangre llamados monocitos. Adicionalmente, tambiĂ©n ha sido investigada la activaciĂłn ex vivo de diferentes subconjuntos de CD que circulan de forma natural en la sangre, utilizando varios tipos celulares incluyendo a cĂ©lulas dendrĂticas plasmocitoides (CDp), que producen altos niveles de interferĂłn-α (IFN-α) tras una infecciĂłn viral.
Los inmunĂłlogos tambiĂ©n han explorado las vacunas destinadas a activar directamente las CD del propio paciente en condiciones in vivo, lo que evita el laborioso y costoso cultivo in vitro. Tal enfoque requiere al menos tres componentes: una "etiqueta de direcciĂłn" (un anticuerpo especĂfico para las CD o una molĂ©cula ligando como un hidrato de carbono dirigido a la CD); un antĂgeno tumoral; y un compuesto que prepara a las CD para activar completamente a los linfocitos T (por lo general un ligando para un receptor de tipo Toll,TLR). Las nanopartĂculas que contienen el antĂgeno y los ligandos de TLR, junto anticuerpos u otros ligandos, han demostrado su eficacia en modelos animales, y actualmente se están llevando a cabo ensayos clĂnicos incipientes utilizando conjugados de anticuerpos dirigidos a CD unidos a un antĂgeno tumoral.

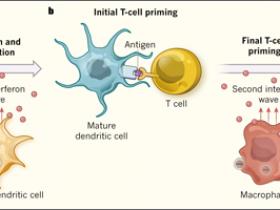
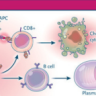
Figura 1. Una vacuna antitumoral de nanopartĂculas.
a, Kranz y colegas sintetizaron nanopartĂculas (complejos de lĂpidos que contienen ARN codificante para antĂgenos tumorales), y evidenciaron que son capaces de dirigirse a cĂ©lulas dendrĂticas y macrĂłfagos en ratones. La absorciĂłn de nanopartĂculas por parte de cĂ©lulas dendrĂticas precursoras promueve su maduraciĂłn a cĂ©lulas presentadoras de antĂgenos, con capacidad migratoria y estimuladora de linfocitos T. La incorporaciĂłn de las nanopartĂculas por cĂ©lulas dendrĂticas plasmocitoides promueve la secreciĂłn de una ola inicial de interferĂłn que ayuda a generar los primeros pasos de la activaciĂłn de cĂ©lulas T. b, Tras la traducciĂłn del ARN dentro de las nanopartĂculas, las cĂ©lulas dendrĂticas maduras son capaces de expresar antĂgenos tumorales y presentarlos a los linfocitos. Los macrĂłfagos, por su parte, al incorporar estos nanocomponentes producen una segunda oleada de interferĂłn, que "ceba" completamente a las cĂ©lulas T contra antĂgenos especĂficos. c, Finalmente, las cĂ©lulas T activadas atacan a las cĂ©lulas tumorales.
Kranz y sus colegas han desarrollado un tipo diferente de vacuna basadas en nanopartĂculas, que no requiere de anticuerpos o ligandos para dirigirse hacia las CD. En lugar de ello, sintetizaron nanopartĂculas consistentes en complejos lipĂdicos + ARN. A travĂ©s de este mĂ©todo, los autores demostraron que, al producir nanopartĂculas ligeramente cargadas en forma negativa (manipulando la proporciĂłn lĂpidos / ARN) pueden dirigirse a los compartimentos que contienen CD en el bazo y otros tejidos linfoides al inyectarlas por vĂa intravenosa en ratones. Mediante el uso de nanopartĂculas que llevan ARN que codifica una proteĂna fluorescente, los autores observaron que la distribuciĂłn dentro del cuerpo era más dependiente de la carga global de la nanopartĂcula que del tipo de lĂpido utilizado. La fluorescencia se observĂł en las CPA como macrĂłfagos y en las ya mencionadas CD (ambos capaces de expresar el marcador molecular CD11c) en la zona marginal del bazo y en otros Ăłrganos linfoides. La fluorescencia no se pudo apreciar en los ratones en los que se eliminĂł la poblaciĂłn de cĂ©lulas CD11c +. Además, las CDp no presentaron fluorescencia, pero evidenciaron otras respuestas de señalizaciĂłn que indicaron una incorporaciĂłn de las nanopartĂculas.Â
Los investigadores encontraron que la absorciĂłn de las nanopartĂculas de ARN se produjo por un proceso basado en la membrana celular denominado micropinocitosis. La incorporaciĂłn fue mayor en los macrĂłfagos. Sin embargo, la más alta expresiĂłn de marcador fluorescente codificado por el ARN ocurriĂł en las CD, lo que indica que son más eficaces que los macrĂłfagos en permitir el transporte del ARN hacia el citoplasma y en traducirlo en proteĂna.
Curiosamente, los autores observaron dos "ondas" transitorias de IFN despuĂ©s de la administraciĂłn de nanopartĂculas (figura 1): la primera fue producida por CDp y alcanzĂł un máximo a las 2-3 horas despuĂ©s de la inyecciĂłn. Esto fue seguido de un segundo evento, que fue producido por macrĂłfagos alrededor de 6-8 horas más tarde. Al poner a prueba una serie de ratones genĂ©ticamente modificados, los autores evidenciaron que la secreciĂłn de IFN era mediada por el receptor TLR y que la primera de las ondas es necesaria para que las CD precursoras maduren y migren para encontrarse con linfocitos T en el bazo y en los ganglios linfáticos. Esto conduce a una respuesta de cĂ©lulas T de una gran intensidad (ayudada por la segunda onda de liberaciĂłn de IFN) frente a una amplia gama de antĂgenos en ratones modelo de tumores, observándose además la generaciĂłn de una robusta y prolongada respuesta antitumoral.
Los autores extendieron su investigaciĂłn a un estudio clĂnico en pacientes con melanoma, usando nanopartĂculas que transportan ARN codificantes para antĂgenos tumorales, presentando los resultados de los primeros tres pacientes tratados. Sorprendentemente, se observĂł una respuesta inmunitaria, aunque todavĂa es pronto para asegurar el Ă©xito, por lo que se necesitan de ensayos más amplios y aleatorizados para validar estos hallazgos. Los tres pacientes produjeron IFN y desarrollaron fuertes respuestas por parte de linfocitos T contra los antĂgenos, incluso ocupando una dosis más baja que en el estudio en ratones. Las respuestas de las cĂ©lulas T involucraron a linfocitos CD4 y CD8. La activaciĂłn de estos Ăşltimos es tĂpico de una respuesta antiviral, por lo que al contar con ambos tipos de respuesta se mejora la actividad anticancerĂgena.
Los autores utilizaron una inyecciĂłn intravenosa para la entrega de las nanopartĂculas, pero serĂa interesante explorar otras vĂas de administraciĂłn, lo que podrĂa modificar su distribuciĂłn. TambiĂ©n serĂa relevante examinar la distribuciĂłn tisular de nanopartĂculas radiomarcadas en los pacientes como en los experimentos con ratones, para ver si tambiĂ©n se dirigen principalmente a cĂ©lulas que expresan CD11c. Otras cĂ©lulas del sistema inmunolĂłgico que tambiĂ©n poseen el marcador CD11c, tales como los neutrĂłfilos y monocitos, igualmente tienen una alta capacidad de fagocitosis, por lo tanto, podrĂan ser capaces de incorporar nanopartĂculas y activarse. Si esto es asĂ, no está claro aĂşn cuál es la contribuciĂłn de estos otros tipos celulares en cuanto a la producciĂłn de señales del sistema inmune, como las citoquinas.
El estudio de Kranz y sus colegas remarca el papel de IFN en la obtenciĂłn de una respuesta robusta por parte de los linfocitos T contra los tumores. Notablemente, se observĂł este tipo de respuestas en cĂ©lulas T CD8 y CD4, tanto en ratones como en humanos. A pesar de que se sabĂa con anterioridad que los linfocitos T CD8 son el principal tipo celular que actĂşa en la erradicaciĂłn tumoral, diferentes subtipos de CD estimulan diferentes tipos de linfocitos citotĂłxicos, por lo que la contribuciĂłn estos Ăşltimos puede estar subestimada. Las respuestas en los tres pacientes con cáncer son interesantes, dados los diferentes tipos de antĂgenos tumorales explorados (incluyendo antĂgenos que no son expresados generalmente en tejido adulto y nuevos antĂgenos que surgen como consecuencia de mutaciones en cĂ©lulas tumorales). Esta plataforma nanotecnolĂłgica puede dar un fuerte impulso al campo de las vacunas, y los resultados de los estudios clĂnicos venideros tendrán una gran relevancia.
Fuente bibliográfica
Immunotherapy: Cancer vaccine triggers antiviral-type defences
Jolanda de Vries and Carl Figdor.
Department of Tumor Immunology, Radboud Institute for Molecular Life Sciences, Radboud University Medical Center, 6525 GA Nijmegen, the Netherlands.
doi:10.1038/nature18443
Temas Relacionados