Metabolitos para controlar la inflamación cerebral
Algunos inmunólogos consideran el sistema nervioso central (SNC) como una tierra de nadie, evitada por las células inmunitarias y por lo tanto, poco interesante. Sin embargo, el SNC tiene un vigoroso potencial inmunológico que permanece latente en condiciones normales pero que se despierta después de una lesión. El interruptor que controla el microambiente inmunitario del cerebro involucra a las células no neuronales de la glía, microglía y astrocitos. Recientemente, se ha descrito cómo estos tipos celulares se comunican a nivel molecular para influir en la inflamación del SNC. Además, se plantea que esta interacción es controlada a distancia por metabolitos provenientes del metabolismo de microorganismos intestinales.
Regulación a distancia
Hace una década, el grupo que realizó el presente estudio, junto con otro grupo de investigación, descubrió un inesperado papel inmunorregulador para un factor de transcripción activado por ligando llamado receptor de hidrocarburos de arilo (AHR, por sus siglas en inglés), que en ese momento era mejor conocido como receptor de toxinas ambientales. Los dos grupos mostraron que AHR modula la progresión de la encefalomielitis autoinmune experimental (EAE, por sus siglas en inglés), una enfermedad autoinmune en ratones en la que el sistema inmunitario se vuelve hiperactivo y ataca al SNC. La EAE se utiliza a menudo como modelo de esclerosis múltiple (EM). Inicialmente, los grupos se centraron en la forma en que el AHR afecta a la EAE mediante la regulación de subconjuntos patógenos y protectores de células inmunitarias fuera del SNC. Pero más tarde se descubrió que el AHR también está fuertemente expresado en el SNC, particularmente en la microglia y astrocitos, lo que plantea la interrogante de si el AHR en el SNC tiene un papel en las enfermedades autoinmunes.
En el estudio actual, Rothhammer y colaboradores indujeron EAE en ratones que habían sido genéticamente modificados para que el AHR pudiera ser eliminado en la microglia (pero no en otras células cerebrales o inmunitarias) mediante un tratamiento farmacológico. La eliminación del AHR microglial exacerbó sustancialmente el EAE en los ratones sin AHR, pero dejó inalteradas las respuestas inmunitarias fuera del SNC. Este hallazgo sugiere que la activación de AHR en la microglia inhibe la inflamación en el SNC (DOI: 10.1038/s41586-018-0119-x).
Las células de la microglia rara vez actúan solas. Al contrario, a menudo se asocian con otros tipos celulares para responder a los estímulos que las activan. Por ejemplo, después de ser activada, la microglia puede instruir a ciertos astrocitos para que ataquen las neuronas locales. Rothhammer y sus colegas encontraron que la microglia deficiente de AHR activada por EAE desencadenaba respuestas inflamatorias exageradas en los astrocitos locales. A continuación, los autores utilizaron la bioinformática para analizar las vías de expresión génica alteradas en esta glía. Este análisis sugirió que proteínas inesperadas señalizan desde la microglia a los astrocitos.
Los sospechosos habituales en estos casos son las moléculas de señalización pro-inflamatorias, pero Rothhammer y colegas demostraron que el AHR en microglia regula directamente la expresión de genes que codifican las proteínas TGF-α y VEGF-B (figura 1) -ninguna de las cuales ha recibido mucha atención por parte de los neuroinmunólogos. Posteriormente, análisis detallados in vitro e in vivo confirmaron que el TGF-α y el VEGF-B regulan la reactividad pro-inflamatoria de los astrocitos. TGF-α amortigua las respuestas inflamatorias de los astrocitos frente a EAE, y su expresión en la microglia es inhibida por la supresión de AHR. Por el contrario, el VEGF-B mejora las respuestas a EAE, y su expresión es promovida por la eliminación de AHR.
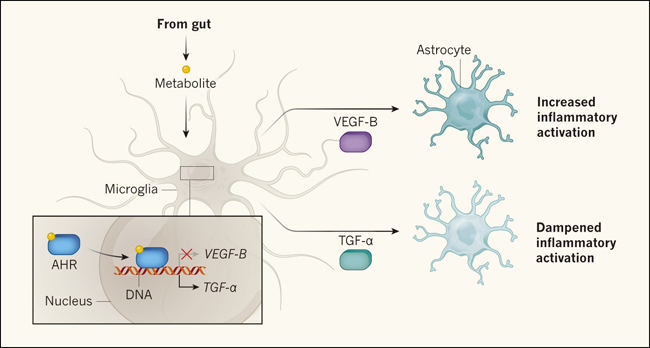
Figura 1. Regulación a distancia de las células inmunitarias sobre el cerebro.
Las bacterias intestinales procesan el componente dietético triptófano para producir metabolitos que ingresan al sistema nervioso central (SNC). En el cerebro, estos metabolitos actúan como ligandos para el receptor de hidrocarburos de arilo (AHR, por sus siglas en inglés), un factor de transcripción expresado en las células de la microglia y astrocitos que median las respuestas a la inflamación en el SNC. Rothhammer y colaboradores (DOI: 10.1038/s41586-018-0119-x) reportaron que, cuando se activa el AHR en la microglia, se une a los genes que codifican las proteínas VEGF-B y TGF-α, inhibiendo la expresión de la primera y promoviendo la de la segunda. Cualquier VEGF-B liberado por la microglia aumenta la capacidad de respuesta de los astrocitos a la inflamación del SNC. Por el contrario, el TGF-α amortigua la respuesta de los astrocitos.
De esta forma, la actividad de la microglia y los astrocitos es modulada por AHR durante la inflamación cerebral en la enfermedad autoinmune. ¿Pero qué señales podrían modular el AHR microglial? Además de las toxinas ambientales, el AHR está ligado a una amplia gama de moléculas, incluidos los derivados dietéticos. En particular, las plantas como el brócoli y otros miembros de la familia de las coles contienen componentes que se unen al AHR, ya sea directamente o después de haber sido transformados en moléculas de metabolitos, como los derivados del triptófano (Trp), por microbios intestinales. Rothhammer y colegas alimentaron a sus ratones con dietas agotadas o enriquecidas en Trp. La disminución de la cantidad de Trp exacerbó la EAE en ratones silvestres, mientras que el enriquecimiento mejoró los efectos de la enfermedad. Por el contrario, ninguna de las dos dietas tuvo ningún efecto en el progreso de EAE en animales con deficiencia de AHR, como podría haberse predicho - en estos animales, el Trp no puede unirse a AHR para amortiguar las respuestas inmunológicas.
Para determinar si era probable que su trabajo tuviera consecuencias para los seres humanos, los autores verificaron los elementos básicos de sus análisis en muestras de tejido de personas con EM, en las que un ataque autoinmune impulsa la inflamación glial, la destrucción de los procesos nerviosos y sus vainas aislantes de mielina y, en última instancia, la formación de cicatrices. El grupo encontró que AHR, TGF-α y VEGF-B se expresaron en células tipo microglia en los tejidos afectados por EM. Los niveles de las proteínas fueron más altos en las regiones recientemente inflamadas que en el tejido cicatrizado antiguo o en el tejido circundante no afectado. Esto sugiere (pero no prueba) que el TGF-α y el VEGF-B tienen un papel en la formación del tejido cicatrizado de la EM.
El trabajo de Rothhammer y sus colegas muestra la compleja regulación de la respuesta inflamatoria en el SNC y añade otra faceta a la comprensión de la conexión intestino-cerebro. La regulación robusta de la respuesta inflamatoria es esencial para el funcionamiento adecuado del SNC. Una regulación deficiente, con episodios inflamatorios desenfrenados, conduce a la enfermedad, pérdida irreversible de células y la formación de cicatrices, mientras que una reactividad inflamatoria comprometida puede dar lugar a la formación de tumores y a infecciones oportunistas. Por lo tanto, es probable que los hallazgos de los autores tengan implicaciones más allá de la esclerosis múltiple.
Fuente bibliográfica
Brain inflammatory cascade controlled by gut-derived molecules
Hartmut Wekerle
Max Planck Institute of Neurobiology, D-82152 Martinsried, Germany.
DOI: 10.1038/d41586-018-05113-0