Los caminos moleculares de la hipoxia
Importantes investigaciones han intentado dilucidar la base molecular de la regulaciĂłn de los niveles de oxĂgeno y su relaciĂłn con la expresiĂłn gĂ©nica. Tras dĂ©cadas de esfuerzos cientĂficos, se descubriĂł una vĂa celular en la que participa un heterodĂmero proteico que es esencial para la detecciĂłn del oxĂgeno en sistemas eucariontes: el factor inducible por hipoxia (HIF). Este factor transcripcional es capaz de modular la expresiĂłn de entre 500 a 1.000 genes, que median una diversidad de adaptaciones hipĂłxicas crĂticas para el desarrollo embrionario, y varias enfermedades y procesos, como el cáncer, inflamaciĂłn e isquemia tisular. Esto demuestra la gran relevancia de las rutas celulares que dependen de los niveles de oxĂgeno y de las macromolĂ©culas capaces de censar su disponibilidad biolĂłgica.
Detectores de oxĂgeno
Los cambios en la disponibilidad de oxĂgeno representan un estĂmulo fisiolĂłgico crĂtico para todos los organismos que necesitan igualar el suministro de oxĂgeno con las demandas de los tejidos. Más allá de la contribuciĂłn al mantenimiento de la bioenergĂ©tica tisular a travĂ©s de la producciĂłn de ATP, el oxĂgeno sirve como un aceptor universal de electrones en numerosas vĂas bioquĂmicas. No es sorprendente, por tanto, que las respuestas a la hipoxia sean casi instantáneas y altamente conservadas a lo largo de la evoluciĂłn. La hiperoxia, por su parte, es un evento del cual el organismo debe estar protegido, ya que puede causar daño a lĂpidos, proteĂnas y otras biomolĂ©culas. Las respuestas agudas suelen implicar cambios en la actividad de molĂ©culas como canales iĂłnicos, mientras que las adaptaciones a largo plazo Incluyen cambios robustos en los patrones globales de expresiĂłn gĂ©nica.Â
En la dĂ©cada de 1990, Gregg Semenza, una genetista de la Universidad Johns Hopkins, y Peter Ratcliffe, un nefrĂłlogo de la Universidad de Oxford, estaban investigando simultáneamente el control transcripcional de los niveles de eritropoyetina, los que varĂan en respuesta a las concentraciones de oxĂgeno. En 1995, Semenza y sus colegas (Proc Natl Acad Sci U S A 1995; 92: 5510-4.) reportaron la purificaciĂłn bioquĂmica de dos subunidades del factor transcripcional HIF-1: un heterodĂmero compuesto por la subunidad HIF-1β (de expresiĂłn constitutiva y previamente conocido como ARNT) y por HIF-1α (cuya expresiĂłn es regulada por oxĂgeno) (figura 1). La informaciĂłn de secuencias ha revelado que cada subunidad es tambiĂ©n un miembro de una superfamilia evolutivamente conservada  de sensores ambientales que responden a diversos estĂmulos, como la luz, xenobiĂłticos, estados redox y al oxĂgeno. Los equipos liderados por Semenza y Ratcliffe determinaron que HIF está activo en prácticamente todas las cĂ©lulas de mamĂferos y es conservado en especies primitivas que carecen de Ăłrganos de suministro de oxĂgeno. Esfuerzos más recientes han demostrado que HIF modula la expresiĂłn de aproximadamente 1.000 genes que implicados ampliamente en adaptaciones hipĂłxicas, incluidos aquellos que regulan el metabolismo, el crecimiento de los vasos sanguĂneos, asĂ como tambiĂ©n la divisiĂłn celular y la inflamaciĂłn.Â
En estudios aparentemente no relacionados, William Kaelin, un oncĂłlogo del Instituto para el Cáncer Dana-Farber, investigĂł cĂłmo las variantes patogĂ©nicas del gen supresor de tumores VHL que codifica para la proteĂna von Hippel-Lindau (pVHL), dan como resultado un sĂndrome de cáncer hereditario que causa tumores altamente vasculares en el ojo, sistema nervioso central y riñón. Además, junto a otros especialistas determinĂł que las cĂ©lulas que carecen de pVHL funcional, poseen elevados niveles transcripcionales de genes inducidos por hipoxia (por ejemplo VEGF)  independientemente de las concentraciones de oxĂgeno. Además, estudios de cristalografĂa de rayos X  mostraron que un complejo multiproteico que contiene pVHL se asemeja a la maquinaria dedicada a la degradaciĂłn de proteĂnas (a travĂ©s de la ubiquitination) en levaduras. En 1999, el grupo de Ratcliffe descubriĂł que cĂ©lulas de cáncer renal deficientes de pVHL no degradan HIF-1α ni HIF-2α, una subunidad α relacionada. Otros estudios realizados por mĂşltiples laboratorios mostraron que la eliminaciĂłn de HIF-α bajo condiciones de oxĂgeno normales requiere actividad de la ubiquitina ligasa mediada por un complejo de proteĂnas que incluye pVHL. Sin embargo, las "marcas" en las proteĂnas HIF-α que permiten el reconocimiento de pVHL y su posterior degradaciĂłn siguen siendo desconocidas.Â
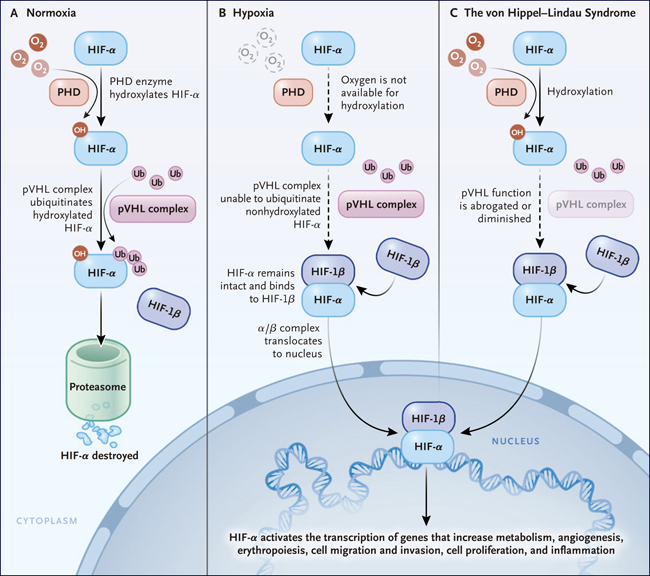
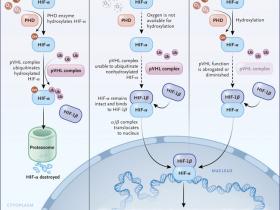
Figura 1: el sentido de la detecciĂłn del oxĂgeno.
La maquinaria molecular esencial para la detecciĂłn de oxĂgeno celular se activa cuando es abundante (Panel A): las subunidades del factor inducible por hipoxia α (HIF-α) de las que existen 2 tipos: HIF-1 α y HIF-2 α, son hidroxiladas en residuos de prolina altamente conservados por el dominio 2 de la enzima porlil hidroxilasa (PHD), permitiendo su reconocimiento por la proteĂna de von Hippel-Lindau (pVHL) que contiene complejos de ubiquitina ligasa. El HIF-α hidroxilado es posteriormente degradado por el proteasoma. A medida que disminuyen los niveles de oxĂgeno (panel B), la hidroxilaciĂłn de prolil HIF-α disminuye, permitiendo la estabilizaciĂłn reversible de HIF-α, la dimerizaciĂłn con HIF-1β (tambiĂ©n conocida como ARNT) y traslocarse al nĂşcleo para la estimulaciĂłn de la transcrpciĂłn gĂ©nica. Los genes regulados por HIF incluyen 500 a 1000 efectores , que median una diversidad de adaptaciones hipĂłxicas crĂticas para el desarrollo embrionario, una fisiologĂa normal y mĂşltiples enfermedades y procesos, como el cáncer, inflamaciĂłn e isquemia tisular. La estabilizaciĂłn de HIF-α y la activaciĂłn de los genes diana tambiĂ©n se producen en las cĂ©lulas de las personas con el sĂndrome de von Hippel-Lindau (panel C), que es causada por variantes de pĂ©rdida de funciĂłn.
Otros estudios han mostrado que las interacciones entre pVHL y las subunidades HIF-α dependen de la hidroxilaciĂłn mediada por oxĂgeno de dos residuos de prolina en cada una de las subunidades HIF-α. Utilizando un enfoque genĂ©tico en Caenorhabditis elegans, se evidenciĂł que los mutantes de vhl-1 expresaban constitutivamente HIF-1α, al igual que los gusanos deficientes de un gen que codifica una dioxigenasa. Se encontrĂł que esta enzima hidroxila un residuo de prolina altamente conservado en HIF-1α, promoviendo su inestabilidad cuando el oxĂgeno es relativamente abundante. TambiĂ©n se demostrĂł que la prolil hidroxilaciĂłn es rápidamente inhibida cuando bajan los niveles de oxĂgeno (figura 1). La secuencia de aminoácidos de la enzima dioxigenasa del gusano permitiĂł la identificaciĂłn de tres enzimas homĂłlogas en mamĂferos, denominadas "PHD" por proteĂnas que contienen dominios prolil hidroxilasa.
Colectivamente, los estudios dilucidaron un mecanismo por el que la disminuciĂłn de los niveles de oxĂgeno resultan en una reducciĂłn de la prolil hidroxilaciĂłn de HIF-α, debido a la inhibiciĂłn de PHD, la estabilizaciĂłn reversible de HIF-α, y la estimulaciĂłn de 500 a 1.000Genes regulados por oxĂgeno que intervienen en diversas adaptaciones a hipoxia a nivel celular, tisular y de organismo. Aunque muchos otros procesos intracelulares -como la actividad de canales iĂłnicos, la transducciĂłn de señales, y las reacciones bioquĂmicas dependientes de oxĂgeno- censan la disponibilidad de oxĂgeno, el eje HIF-PHD-pVHL tiene un rol fundamental en la comunicaciĂłn de las concentraciones de oxĂgeno a los programas de expresiĂłn gĂ©nica.Â
Claramente, la relevancia clĂnica de este sistema de detecciĂłn de oxĂgeno es sustancial: la hipoxia modula numerosos trastornos y procesos, como el cáncer, enfermedades cardiovasculares, hipertensiĂłn, accidente cerebrovascular, infecciones bacterianas, inflamaciĂłn y cicatrizaciĂłn de heridas.Â
Fuente bibliográfica
The Hypoxia Response Pathways — Hats Off!
M. Celeste Simon, Ph.D.
Abramson Family Cancer Research Institute and Department of Cell and Developmental Biology of the Perelman School of Medicine, University of Pennsylvania, Philadelphia.
DOI: 10.1056/NEJMcibr1610065