En el corazÃģn de la ediciÃģn gÃĐnica
La ediciÃģn del genoma tiene el potencial para corregir selectiva y especÃficamente mutaciones de la lÃnea germinal. Recientes publicaciones han mostrado el avance para reparar una alteraciÃģn heterocigÃģtica del gen MYBPC3 en embriones humanos mediante el mÃĐtodo CRISPR-Cas9, que se respalda en la precisiÃģn y alta eficiencia de la activaciÃģn de una respuesta endÃģgena de reparaciÃģn del ADN. Los quiebres inducidos en la doble hebra del ADN en el alelo paterno mutante fueron sorpresiva y predominantemente reparados usando el gen materno silvestre homÃģlogo como templado, en lugar de una plantilla de ADN sintÃĐtico introducido por los investigadores. Utilizando el mÃĐtodo, se logrÃģ evitar el mosaicismo durante la divisiÃģn embrionaria y se alcanzÃģ un alto rendimiento de embriones homocigotos portadores del gen silvestre sin evidencia de mutaciones fuera de objetivo. La eficacia, precisiÃģn y seguridad de este enfoque sugieren que tiene el valor para ser utilizado en la correcciÃģn de mutaciones hereditarias en embriones humanos complementando el diagnÃģstico genÃĐtico preimplantacional. Sin embargo, aÚn queda mucho por considerar antes de las aplicaciones clÃnicas, incluyendo la reproducibilidad de la tÃĐcnica con otras mutaciones heterocigotas.
ReparaciÃģn silvestre
La capacidad de editar selectivamente regiones del genoma utilizando una tÃĐcnica conocida como CRISPR-Cas ha transformado muchas ÃĄreas de la investigaciÃģn biolÃģgica. Estos avances han planteado la interrogante de si esta tÃĐcnica se utilizarÃĄ en el futuro para tratar o prevenir enfermedades. Los ensayos clÃnicos que han usado este mÃĐtodo para modificar cÃĐlulas humanas ya estÃĄn en marcha, por ejemplo se han probado cÃĐlulas inmunitarias editadas para tratar el cÃĄncer.
Actualmente existe un debate en curso sobre el uso potencial de CRISPR-Cas para modificar el genoma de un individuo, tema que plantea muchos cuestionamientos ÃĐticos y reglamentarios. Sin embargo si se llegase a implementar ÂŋquÃĐ otras investigaciones extra cientÃficas debiesen ser necesarias para llegar a aplicarse en la clÃnica? En un reciente artÃculo Hong Ma y colaboradores reportaron el uso de CRISPR-Cas para reparar una alteraciÃģn genÃĐtica asociada con la enfermedad cardÃaca, en un estudio de embriones humanos cultivados in vitro. Los autores analizaron minuciosamente los embriones modificados, demostrando que algunos de los obstÃĄculos tÃĐcnicos asociados a menudo con el uso de esa tecnologÃa de ediciÃģn del genoma podrÃan ser superados.
La condiciÃģn conocida como cardiomiopatÃa hipertrÃģfica  es una enfermedad cardÃaca hereditaria. Puede ser causada por mutaciones en muchos genes diferentes, incluyendo el gen de la proteÃna C de uniÃģn a  miosina cardÃaca (MYBPC3). Este gen codifica una proteÃna que contribuye al mantenimiento estructural del mÚsculo cardÃaco y a la regulaciÃģn de su contracciÃģn y relajaciÃģn. La presencia de una copia mutante de MYBPC3 causa sÃntomas que generalmente se manifiestan como insuficiencia cardÃaca. Aunque los tratamientos existentes pueden disminuir los sÃntomas, no hay manera de hacer frente a la causa genÃĐtica subyacente en un paciente. Hong Ma y sus colegas investigaron el uso de la ediciÃģn gÃĐnica para corregir esta mutaciÃģn.
Una opciÃģn para prevenir la heredabilidad de algunas mutaciones asociadas a la condiciÃģn es utilizar pruebas genÃĐticas durante la fecundaciÃģn in vitro (FIV) para superar la fertilidad. Esto permite la selecciÃģn de embriones que no contienen la mutaciÃģn especÃfica. Si uno de los padres que participan en el tratamiento de FIV tuviera una copia mutante de MYBPC3, el 50% de los embriones fecundados heredarÃan la enfermedad. Los autores propusieron un escenario hipotÃĐtico en el que su enfoque podrÃa permitir que un individuo con cardiomiopatÃa hipertrÃģfica aumente el porcentaje de embriones disponibles para la implantaciÃģn de FIV que no heredasen la enfermedad.
En los Últimos aÃąos, CRISPR-Cas ha sido desarrollado para editar de manera eficiente y precisa el genoma humano. Aunque este mÃĐtodo ha sido ampliamente adoptado en sistemas de cultivo de cÃĐlulas de mamÃferos y modelos de embriones animales, tan sÃģlo tres estudios publicados reportan el uso de esta tÃĐcnica en embriones humanos.
El sistema de ediciÃģn CRISPR-Cas necesita sÃģlo dos componentes para modificar el ADN: una guÃa correspondiente a una secuencia de ARN y una enzima nucleasa Cas, siendo Cas9 la mÃĄs utilizada. El objetivo genÃģmico especÃfico se determina mediante el mÃĐtodo de guÃa de ARN, que forma un complejo con Cas9, permitiendo que la enzima se una al sitio que contiene una complementaridad de bases. En este sitio es donde Cas9 corta el ADN, causando un quiebre de la doble hebra.
La formaciÃģn de quiebres en la doble hebra puede activar uno de los dos principales mecanismos de reparaciÃģn del ADN celular: vÃas en la cÃĐlula: la recombinaciÃģn no homÃģloga o uniÃģn de extremos no homÃģlogos (NHEJ) o el de reparaciÃģn directa por homologÃa (HDR). La vÃa de NHEJ repara una rotura aÃąadiendo o eliminando nucleÃģtidos al azar, lo que resulta en cambios en la secuencia de ADN, por lo que no es adecuado para fines de correcciÃģn gÃĐnica. Por lo tanto, los enfoques se centran en la HDR, que utiliza secuencias homÃģlogas (complementarias) para reparar las roturas de ADN, lo que hace posible introducir secuencias especÃficas para permitir reparaciÃģn a medida.
Una entrega oportuna de los componentes CRISPR en un punto apropiado en el ciclo de divisiÃģn de la cÃĐlula ya sea en la transiciÃģn entre G1 y S, o en la transiciÃģn entre G2 y la fases mitÃģtica, puede conducir a un uso preferencial del camino HDR. Desafortunadamente, en trabajos anteriores la eficiencia de la reparaciÃģn de HDR despuÃĐs de la acciÃģn de CRISPR-Cas9 ha sido indeseablemente baja tanto en cultivo de cÃĐlulas madre de embriones humanos (eficiencia de aproximadamente del 2%) como en  embriones humanos (14,3 - 25% de eficiencia).
Hong Ma y colegas diseÃąaron constructos de  CRISPR-Cas9 para la ediciÃģn de MYBPC3, y verificaron la uniÃģn al gen usando cÃĐlulas madre humanas. Posteriormente empezaron a trabajarcon embriones humanos. Uno de los principales retos de usar CRISPR-Cas9 para editar estos genomas ha sido el fenÃģmeno de mosaicismo, en el que las ineficiencias en la ediciÃģn de genes resulta en embriones que contienen cÃĐlulas modificadas y no modificadas (figura 1a). Esto puede llevar a una mezcla de cÃĐlulas sanas y enfermas en varios tejidos y Ãģrganos, posiblemente causando sÃntomas patolÃģgicos.
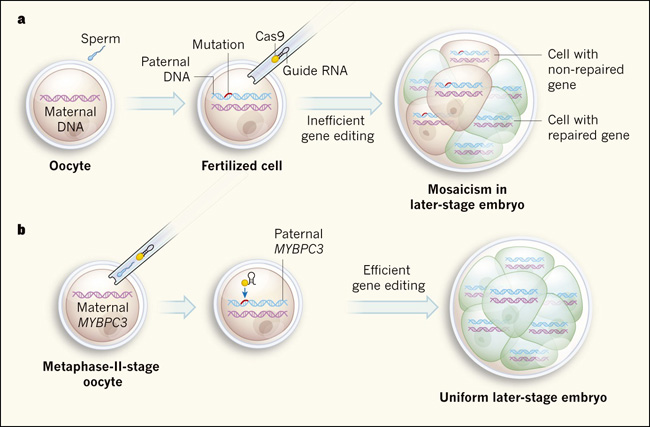
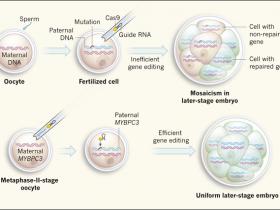
Figura 1. La ediciÃģn gÃĐnica en embriones.
a, El sistema de ediciÃģn gÃĐnica, CRISPR-Cas, puede reparar una mutaciÃģn en un gen. En tres estudios previos publicados utilizando esta tÃĐcnica en embriones humanos cultivados in vitro, un Ãģvulo (ovocito) fue fecundado y luego se inyectaron los componentes de ediciÃģn en la cÃĐlula. Estos incluyen la enzima Cas9 y una guÃa de secuencia de ARN que ayuda a dirigir la maquinaria de modificaciÃģn hacia una localizaciÃģn especÃfica del genoma, por ejemplo para reparar una mutaciÃģn heredada del padre. Sin embargo, la ediciÃģn es a menudo ineficaz, y los embriones en la etapa posterior pueden contener una mezcla de cÃĐlulas reparadas y no reparadas - un fenÃģmeno conocido como mosaicismo. b, Hong Ma y colaboradores (Nature. 2017 Aug 24;548(7668):413-419) asumieron un enfoque alternativo para corregir una mutaciÃģn en el gen MYBPC3 (que estÃĄ asociado con la enfermedad cardÃaca) en embriones humanos cultivados in vitro. Inyectaron componentes de ediciÃģn gÃĐnica y espermatozoides en ovocitos que contenÃan versiones no mutadas de MYBPC3. La mitad de los espermatozoides utilizados tenÃan una mutaciÃģn MYBPC3. Los ovocitos fueron inyectados en metafase II, una fase de su ciclo celular. Los investigadores reportaron que 42 de los 58 embriones examinados (72,4%) no tenÃan el MYBPC3 mutante, y su anÃĄlisis sugiere que la copia materna del gen se utiliza como modelo para guiar la reparaciÃģn. Este enfoque dio lugar a una ediciÃģn de genes eficiente y uniforme en los embriones, que progresÃģ hasta llegar a una fase posterior del desarrollo embrionario.
Los autores investigaron una situaciÃģn en la que el padre tenÃa una copia mutante de MYBPC3 y la madre sÃģlo tenÃa copias silvestres del gen. En los experimentos control, el 47,4% (9 de 19) de embriones fecundados in vitro no heredaron la copia mutante de MYBPC3, la proporciÃģn esperada dado que la mitad de los espermatozoides deberÃa tener la copia silvestre del gen. Los autores demostraron que, si los componentes de la ediciÃģn eran inyectados juntos con los espermatozoides en un Ãģvulo humano (ovocito) en una etapa en el ciclo celular como metafase II (figura 1b), un 72,4% de los embriones resultantes (42 de 58) heredaban solamente la versiÃģn silvestre de MYBPC3. Los otros 16 embriones tenÃan copias de MYBPC3 con signos de ediciÃģn mediada por NHEJ que se dirigÃa a la versiÃģn mutante del gen pero que no lo reparaba a la versiÃģn normal. Â
Curiosamente, cuando los autores analizaron la correcciÃģn de MYBPC3 en los embriones, encontraron que sÃģlo uno de los 42 embriones que tenÃan tipo MYBPC3 silvestre habÃa utilizado el mÃĐtodo CRISPR para su reparaciÃģn. Sus resultados indican que la copia materna silvestre de MYBPC3 probablemente otorgÃģ la plantilla de reparaciÃģn, en lugar de la copia introducida. Esto contrasta con las observaciones en cÃĐlulas madre, en las que se utilizÃģ la plantilla de nucleÃģtidos introducida por los investigadores para el proceso de reparaciÃģn. Los autores proponen que el mecanismo de reparaciÃģn del ADN que opera en un embriÃģn temprano difiere de aquel que ocurre en cÃĐlulas madre. En el embriÃģn en el que se pudo detectar la correcciÃģn utilizando la plantilla de reparaciÃģn, la secuencia de templado se encontrÃģ solo en un subconjunto de cÃĐlulas, mientras que las restantes probablemente se habÃan corregido usando la versiÃģn materna de este gen.
Aunque los autores demostraron que se mantiene la integridad del genoma embrionario despuÃĐs de que la ediciÃģn por CRISPR-Cas9, lo que es algo sumamente prometedor, se deben realizar mÃĄs estudios y optimizaciones a esta tecnologÃa. Estos tendrÃĄn que confirmar que el enfoque es seguro en tÃĐrminos de criterios como el mosaicismo, ediciÃģn fuera de objetivo, y detecciÃģn de anomalÃas en la ediciÃģn de embriones, todo antes que pueda ser utilizado como terapia para enfermedades hereditarias. Sin embargo, este estudio pavimenta el camino para que las investigaciones con CRISPR-Cas9 lleguen a la clÃnica a futuro. Hasta entonces, las pruebas genÃĐticas embrionarias durante la FIV siguen siendo el mÃĐtodo estÃĄndar para prevenir la transmisiÃģn de enfermedades hereditarias.
Fuente bibliográfica
Biotechnology: At the heart of gene edits in human embryos.
Nerges Winblad and Fredrik Lanner
Department of Clinical Science, Intervention and Technology, Karolinska Institutet, Stockholm, Sweden.
doi:10.1038/nature23533